תַקצִיר
תקציר מאמר זה מבוסס על ריאיון שנערך בין שני הכותבים.
ביולוגיה מִבנִית היא תחום שמטרתו לגַלות את המִבְנֶה של כל הרכיבים שמהם מורכבים החיים – החל מהמולקולות הקיימות בבני אדם ובחיות אחרות, דרך מולקולות הנמצאות במִיקְרוֹאוֹרְגָנִיזְמִים זעירים, ועד למולקולות המרכיבות את הצמחים. כדי להבין את המבנים הללו, מדענים העוסקים בביולוגיה מִבנִית משתמשים בטכניקות הדמיה מתוחכמות המחדדות מאוד את ה''ראייה'', שהיא היְכולת לקבוע את המִבְנֶה של מולקולות קטנות ומגוונות. מיקרוסקופ אלקטרונים הוא אחד מטכניקות ההדמיה המתקדמות והעוצמתיות ביותר. בטכניקה זו האלקטרונים נשלחים דרך דגימות קפואות כדי לקבוע את מִבְנֶה המולקולות הבודדות. ההגדלה היא כֹּה עוצמתית, שאפשר לראות את האטומים המרכיבים את המולקולות. התמונות הללו עוזרות לנו להבין את המִבְנֶה ואת התפקוד של אבני הבניין היסודיות של החיים. במאמר זה נְסַפֵּר לכם על אודות הפיתוחים שהובילו למהפכת הרֶזוֹלוּצְיָה של מיקרוסקופ האלקטרונים. בזכות תרומתו של ד''ר הֶנְדֶרְסוֹן לתהליך, הוא נבחר לקבל עם מדענים אחרים את פרס הנובל לכימיה לשנת 2017.
ד''ר ריצ'רד הֶנְדֶרְסוֹן (Richard Henderson) זכה בפרס נובל לכימיה לשנת 2017 עם פרופ' ז'אק דוּבּוֹשֶה (Jacques Dubochet) ופרופ' יוֹאָכִים פְרָאנְק (Joachim Frank) , על פיתוח מיקרוסקופ קריו- אלקטרונים לקביעת מִבְנים של מולקולות ביולוגיות בתמיסה.
מבט עומק: מְגַלים את מבנה המולקולות הביולוגיות
גופים חיים מכילים מִבְנִים רבים, ומתרחשים בהם תהליכים חשובים. אנחנו יודעים שבגוף האדם ישנם איברים העשויים מִתָאִים, ושבתוך התאים הללו יש אֶבְרוֹנִים ומולקולות רבים, הממלאים את כל התִפקודים הנחוצים לשמירה על החיים, כמו ייצור אנרגיה, סילוק פסולת, תנועה, והגנה מפני גורמים מזיקים (איור 1). כדי להבין כיצד פועלים יצורים חיים, בתקווה לשפר את חייהם, עלינו לדעת אֵילו מִבְנִים קיימים במערכת ביולוגית נתונה, ומהן הפעילויות שמִבְנִים אלה מְבַצעים. הביולוגיה המִבְנִית היא תחום שמטרתו להתבונן במִבְנִים של רכיבים ביולוגיים. בעָבָר המדענים חיפשו תחילה פעילויות מסוימות, שהם יָדעו שמתרחשות במערכת ביולוגית, כמו המרת מקור אנרגיה אחד לסוג אחֵר של אנרגיה שאֶפשר לאחסן. לאחר שמצאו את הפעילות, הם זיהו את המולקולות שהשתתפו בפעילות – בדרך כלל היו אלה חלבונים ואֶנְזִימִים – ורק אז קבעו את המִבְנִים של אותן המולקולות.
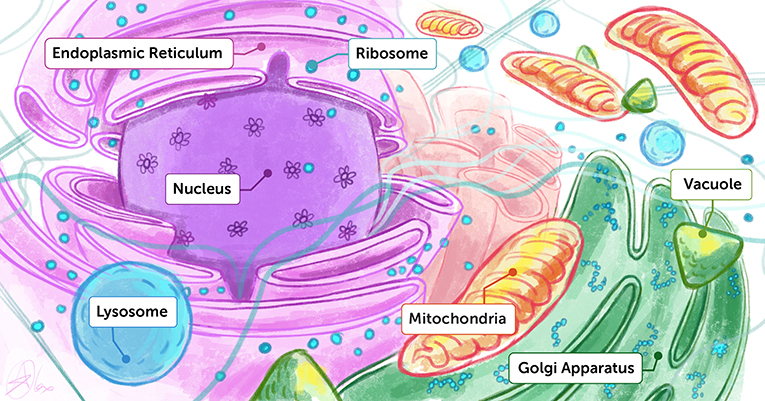
- איור 1 - פרשנות אומנותית של פְּנים התא.
- תוכלו לחשוב על שפְּנים כמגרש משחקים המכיל מגוון רחב של מולקולות ושל אֶברונים בצפיפות – ולכל אחד מהם תפקיד מיוחד. כדי להבין כיצד החיים פועלים, אנחנו שואפים להכיר הן את המִבנים הן את התִפקודים של כל אחת מאבני הבניין הביולוגיות. Endoplasmic Reticulum = רִשְׁתִּית פְּלַזְמַת הַתָּא Nucleus = גרעין התא Lysosome = לִיזוֹזוֹם Ribosome = רִיבּוֹזוֹם Mitochondria = מִיטוֹכוֹנְדְּרִיּוֹן Golgi Apparatus = מערכת גוֹלְג'י Vacuole = חָלוּלִית.
בשנת 2000 התרחשה בעולם מהפכה בהבנת המידע הגנטי (DNA) – המידע המאוחסן בתאים שלנו שאנחנו יורשים מהורינו. מדענים הרכיבו את ''מִקְבָּץ ההוראות'' המלא הראשון (הנקרא רֶצֶף בסיסֵי ה-DNA) של כל המידע הגנטי האנושי. מאז, בִּמְקום לחפש פעילות, ואחר כך למצוא מולקולה, ואז לקבוע את המבנה שלה, ביולוגים מִבניים יכולים להשתמש במידע הגנטי שמְסַפֵּר על כל האנזימים והחלבונים בגוף. בשנת 2000, כאשר הגֶנוּם האנושי נקבע, גילינו רק כ-20% מהמולקולות המקודדות ב-DNA האנושי! עם התגלית הזאת נפתח נתיב חדש לגמרי בתחום הביולוגיה המבנית. כעת אנחנו יכולים לגַלות את מִבְנֶה המולקולות מבלי שנצטרך קודם לדעת מה תפקידן. איך אנחנו חוקרים את המִבְנִים של המולקולות הללו? בעזרתם של חלקיקים זעירים הנקראים אלקטרונים!
אלקטרונים והמיקרוסקופ האלקטרוני
אלקטרונים הם חלקיקים זעירים הנמצאים בכל אטום בעלי מִטען חשמלי. האלקטרונים הם מקור של אור ושל צורות אחרות של קרינה אלקטרומגנטית, כמו קרני רנטגן, ותנועתם יוצרת חשמל. האם אתם מאמינים שעד שנת 1895 אף אחד לא ידע על קיומם של האלקטרונים? באותה השנה האלקטרונים זוהו לראשונה על ידי ג'וזף ג'ון תוֹמְסוֹן (Joseph John Thompson), מדען במחלקה לפיזיקה באוניברסיטת קיימברידג' שבאנגליה. ארבעים שנה לאחר מכן, ב-1935, ג'ורג' פָּגֶ'ט תומסון (George PagetThompson, בנו של ג'וזף ג'ון תומסון) הֶראה שהאלקטרונים מתנהגים הן כחלקיקים והן כגלים – יש להם תדירות ואורך גל, בדיוק כמו גלים אחרים. גם ג'וזף ג'ון תוֹמְסוֹן וגם בנו ג'ורג' פָּגֶ'ט תוֹמְסוֹן זכו בפרסי נובל על שגילו שהאלקטרון מתנהג כחלקיק ועל שגילו שהאלקטרון מתנהג כגַל.
זמן קצר לאחר מכן, מדענים הבינו שאם האלקטרונים מתנהגים כמו גלים, במובן מסוים הם חייבים להתנהג כמו אור, משום שגם אור יכול להתנהג כמו גל. לכן מדענים ניסו להשתמש באלקטרונים כדי להאיר דגימות זעירות. הרעיון זֵהֶה לדרך שבה אנחנו משתמשים בעיניים, במצלמה או במיקרוסקופ רגיל כדי להסתכל על דברים – אך בִּמְקום להיעזר באור נראה, עושים זאת באמצעות אלקטרונים. זו הייתה ראשית דרכו של מיקרוסקופ האלקטרונים, שהוא טכניקת הדמיה עוצמתית ביותר. לאלקטרונים יש אוֹרֶךְ גל קצר פי 100,000 בערך מאוֹרֶךְ הגל של האור. אפשר לחשוב על אוֹרֶךְ הגל כפרמטר ''התמקדות'' – ככל שאוֹרֶךְ הגל קטן יותר, כך נוכל ''להתקרב'' יותר לדגימה שלנו. כלומר התמונות שצולמו בעזרת אלקטרונים הן מפורטות מאוד, או במילים אחרות, הן ברֶזוֹלוּצְיָה גבוהה. הודות לרזולוציה הגבוהה שלו, מיקרוסקופ האלקטרונים מסייע בגילוי מִבְנִים של מולקולות זעירות באופן שלא היה אפשרי לראות קודם לכן.
כיצד פועל מיקרוסקופ האלקטרונים?
במיקרוסקופ אלקטרונים קרן אנרגיה של אלקטרונים יוצאת ממקור אלקטרוני ועוברת דֶרֶךְ הדגימה הנחקרת (איור 2A). כאשר אלקטרונים עוברים דרך הדגימה, הם מקיימים אינטראקציה עם האטומים שלה ועוברים תהליך של דִיפְרָקְצִיָה, כלומר אותם האלקטרונים נזרקים או סוטים ממסלולם. כשהאטומים נִקרים בדרכם של האלקטרונים, האלקטרונם מסתדרים בצורה ייחודית בהתאם למִבְנֶה האטומים שהם עוברים דרכו. אחרי שהאלקטרונים עוברים דיפרקציה, עדשות הנמצאות במיקרוסקופ (הדומות לעדשות של מצלמה) אוספות וממקדות את האלקטרונים. לאחר מכן, הם מתועדים על ידי גלאי אלקטרונים. בשלב זה למדענים יש תמונה של האלקטרונים שעברו דיפרקציה מהדגימה, ועליהם להמיר אותה לתמונה של הדגימה עצמה. המרה זו מבוססת על פיזיקה פשוטה המתארת את הקֶשֶר בין מה שאנחנו מודדים לבין התמונה שאנחנו מקבלים. ההמרה תלויה בגורמים רבים, ביניהם אורך הגל של האלקטרונים והעדשות שבהן משתמשים., מומחים למיקרוסקופיה מוודאים את ההמרה.

- איור 2 - מיקרוסקופ אלקטרונים.
- (A) במיקרוסקופ האלקטרונים מקור האלקטרונים משחרר קרן של אלקטרונים חמים וטעונים באנרגיה. הקרן הזאת עוברת דרך דגימה שנמצאת בתוך תא רִיק (ואקום). כאשר האלקטרונים מקיימים אינטראקציה עם הדגימה, הם עוברים דיפרקציה (מתפזרים). אז, עדשות מיוחדות אוספות וממקדות אותם, ולאחר מכן גלאי האלקטרונים קולט אותם. (B) מיקרוסקופ אלקטרוני מאוניברסיטת קיימברידג' (אנגליה) המאפשר למדענים לצלם דגימות ביולוגיות קפואות (איור: https://www.cambridgein-dependent.co.uk/business/astrazeneca-and-lmb-in-cambridge-use-one-of-world-s-most-advanced-microscopes-to-make-breakthrough-9052845/ אוניברסיטת קיימברידג').
- Electron source = מקור אלקטרונים
- Electron beam = קרן אלקטרונים
- Vacuum chamber = תא רִיק
- Sample = דגימה
- Diffracted beams = קרניים מפוזרות
- Focusing lens = עדשת מיקוד
- Electron detector = גלאי אלקטרונים.
אתגרי השימוש במיקרוסקופ אלקטרונים
אף על פי שהאלקטרונים יכולים לעזור לנו לראות תמונות יוצאות דופן של מולקולות, עלינו להתגבר על אתגרים משמעותיים כשמשתמשים בהם להדמיה של מולקולות ביולוגיות. ראשית, לפי פיזיקת הַקְּוַנְטִים, אלקטרונים בודדים אינם ''הגיוניים''. כאשר שואלים אותם שאלה (לדוגמה, מה קורה כשהם פוגשים מולקולה ספציפית?), הם לא משיבים תשובה ברורה כפי שאנשים עושים. בִּמְקום זאת, יש הִתָּכְנוּת (הסתברות) מסוימת של התנהגות האלקטרונים בכל אחת מהתוצאות השונות. בעולם האלקטרונים כל מה שיכול היה לקרות אכן קרה, עם הסתברות מסוימת לכל אפשרות. המשמעות היא שהמדענים חייבים לאסוף תשובות רבות מאלקטרונים רבים, ולשלב את המידע בתבונה כדי לקבל את התשובה הכוללת. כדי לעשות זאת, אנחנו מאירים את הדגימה במיליוני אלקטרונים ובעזרת חישוב הממוצע הכולל של תכונותיהם, אנחנו מקבלים תשובה הגיונית.
שנית, האלקטרונים עלולים לפגוע בדגימה, כיוַון שיש בהם אנרגיה גבוהה מאוד והם חייבים לעבור דרך כל הדגימה כדי להגיע לגלאי. הטמפרטורה שלהם יכולה להגיע לכאלפיים מיליון מעלות צלזיוס; לשם השוואה: מים רותחים ב-100 מעלות צלזיוס! האלקטרונים הללו, שהם אנרגטיים מאוד, כמו גם כל סוג אחר של קרינה אנרגטית, יכולים ''למשוך'' אלקטרונים מתוך מולקולות הדגימה. תהליך זה מְשַׁנֶּה את הצורות ואת המאפיינים של מולקולות הדגימה, משום שהמולקולות הביולוגיות עדינוֹת יחסית. מסיבה זו, קשה למדענים לקבל מספיק מידע על המִבְנֶה של מולקולה ביולוגית בודדת לפני שהיא מושמדת. אחת הדרכים להתמודד עם האתגר הזה היא לבצע הדמיה של הרבה מולקולות זהות ובודדות – לפחות 500 כשרוצים להתבונן במולקולות ביולוגיות במיקרוסקופ אלקטרונים – ולייצר ממוצע של התמונות כדי לקבוע את המִבְנֶה של מולקולה טיפוסית. דרך נוספת להתמודדות עם האתגר הזה היא לקרר את הדגימה בצורה מיוחדת שתגביר את עמידוּתה בפני נזקי אלקטרונים. נתאר זאת בחלק הבא.
אתגר נוסף נובע מהעובדה שהאלקטרונים מתפזרים ברגע שהם נמצאים ליד אטומים כלשהם. לכן חייב להיות מסלול פנוי לחלוטין בין מקור האלקטרונים לבין הדגימה, כדי שהאלקטרונים יגיעו למולקולות הרצויות, ולא יתפזרו בגלל מולקולות אחרות שנמצאות בדַרכם, אפילו מולקולות של חמצן וחנקן הנמצאות באוויר. במילים אחרות, המדענים חייבים ליצור רִיק סביב הדגימה שבמיקרוסקופ האלקטרונים. כיוַון שמולקולות ביולוגיות נמצאות תמיד בתמיסות המכילות מים (למשל, מולקולות בדם שלכם), הבעיה היא שהמים מתאדים ברִיק והדגימה מתייבשת. לעיתים קרובות ההתייבשות הזאת פוגעת במולקולות הביולוגיות שבדגימה. כדי להתגבר על אתגר זה, מדעני הביולוגיה המבנית נאלצו לרתום את היצירתיות שלהם במטרה לנצל את התכונות הייחודיות של המים.
האם מים יכולים להישאר במצב צבירה נוזלי כשקר מאוד?
הנה ניסוי חביב שתוכלו לעשות בבית כדי להבין את אחת התכונות הייחודיות של המים (איור 3). קחו צנצנת רֵיקה עם מִכְסֶה ומִלאו אותה במים. הַבריגו את המִכְסֶה בחוזקה כדי לוודא שלא ייכנסו לתוכה בועות אוויר, והכניסו את הצנצנת למקפיא. השאירו את הצנצנת במקפיא למשך יום שלם – עד אז טמפרטורת המים תרד לטמפרטורה של C10°- או C20°- (מים בדרך כלל הופכים לקרח ב-0 מעלות צלזיוס). למוחרת הוציאו את הצנצנת מהמקפיא ובִדקו: האם המים הפכו לקרח מוצק, או שהם נשארו במצב צבירה נוזלי?
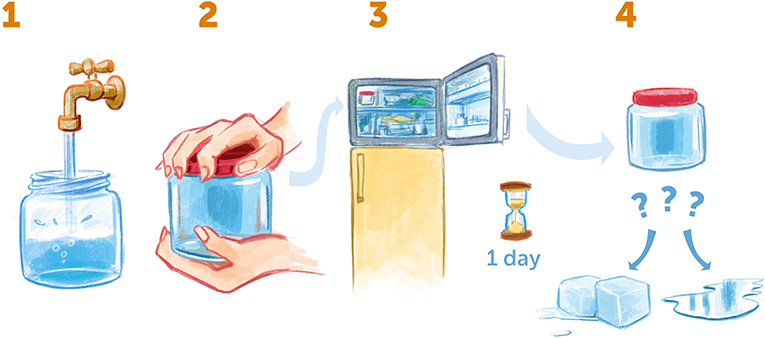
- איור 3 - קירור-על של מים בבית.
- (1) קחו צנצנת ריקה, מלאו אותה לגמרי במים, וּוַדאו שאין בתוכה בועות אוויר. (2) אטמו את הצנצנת לגמרי. (3) שימו אותה במקפיא למשך יום שלם. (4) לאחר מכן הוציאו את הצנצנת. האם המים קפואים, או שהם עדיין נוזליים? אם הם עדיין נוזליים, יצרתם מים בקירור-על!
ברוב המקרים תגלו שהמים עדיין נוזליים – הם עברו קירור-על, כלומר הם התקררו לטמפרטורה נמוכה מטמפרטורת הקיפאון (0°C) אך מבלי להפוך לקרח. בניסויים שלנו אנחנו רוצים לקרר מים עוד יותר, עד מתחת לטמפרטורה של C170°-, משום שבטמפרטורה זו הם נעשים יציבים מאוד וללא תזוזה. כמו כן, אנחנו רוצים להימנע מהיווצרות של גבישי קרח, כי הם מפריעים למדידות שלנו. כדי להצליח בכך, עלינו להשתמש בשיטת קירור מיוחדת שפותחה במעבדתו של ז'אק דוּבּוֹשֶה (Jacques Dubochet), שחָלַק את פרס הנובל לכימיה לשנת 2017 עם יוֹאָכִים פְרָאנְק (Joachim Frank) ועימי - ריצ'רד הֶנְדֶרְסוֹן. בשיטה זו אנחנו משתמשים באֶתָאן או בפְּרוֹפָּאן נוזליים (אלה חומרים המצויים בגז טבעי, עשויים מפחמן ומֵימָן), המקוררים לטמפרטורה של C185°-. לאחר מכן, אנחנו טובלים שִׁכְבַת מים דקה מאוד בנוזל המקורר של האתָאן או הפְּרוֹפָּאן. המים מתקררים כֹּה מהר – בערך תוך אלפית השנייה – כך שגבישי קרח מאורגנים לא מספיקים להיווצר, והם נשארים בצורתם הנוזלית הלא-מאורגנת [1]. אנחנו קוראים לסוג הקרח הזה ''קֶרַח אַמוֹרְפִי'' (חסר צורה) [1], וכך אנחנו מקבלים מים בקירור-על.
נוסחת הקֶסֶם של אלקטרונים חמים ודגימות קרות
מתברר ששכבות מים דקות שעברו קירור-על תומכות בצורה טובה להפליא במולקולות הביולוגיות שאנחנו רוצים לְדַמּוֹת באמצעות מיקרוסקופ האלקטרונים. כאשר לתהליך ההדמיה מתווסף גם שלב הקירור, הטכניקה נקראת מיקרוסקופ אלקטרונים בטמפרטורות נמוכות (בלועזית: מיקרוסקופ אלקטרונים קְרִיוֹגֶנִי. ''קריוגני'' הוא המונח המתייחס לקירור). טכניקה זו מאפשרת לנו להתמודד עם שני האתגרים שהוזכרו לעיל: היא מאפשרת לייצב את הדגימה, שהופכת עמידה בפני נזקים הנגרמים מאלקטרונים עתירי אנרגיה. כמו כן, הטכניקה מאפשרת לנו לבחון את המולקולות הביולוגיות בסביבתן המֵימית הטבעית, ללא אידוי של מים, כיוַון שהמים נמצאים בסביבה של רִיק. ישנו יתרון חשוב נוסף: בניגוד לרוב הנוזלים האחרים, המים מתפשטים כשהם מגיעים לטמפרטורה של מתחת ל-C4°. תכונה זו של המים מונעת פגיעה במולקולות הביולוגיות כשהן נמצאות במים שעברו קירור-על. אם המים היו מתכווצים בקירור, המולקולות היו נלחצות ואולי אף נשברות.
שיטת ההדמיה של מיקרוסקופ האלקטרונים הקְרִיוֹגֶנִי פשוטה למַדַי, אך יעילה ביותר. היא מאפשרת לנו לְדַמּוֹת מולקולות ביולוגיות ברזולוציה שלא הייתה אפשרית בעבר, ולכן יש המכנים אותה ''מהפכת הרֶזוֹלוּצְיָה''.
באיור 4 נוכל לראות דוגמאות לתמונות יפות שהתקבלו בשימוש במיקרוסקופ האלקטרונים הקְרִיוֹגֶנִי. מדובר בִּקְנֵה מידה זעיר – עשיריות של ננומטרים, שהם פחות מאַלְפִּית של רוחב של שַׂעֲרָה אנושית! האם גם אתם מבינים את הפלא הגדול שנקרא ''מיקרוסקופ האלקטרונים הקְרִיוֹגֶנִי''?
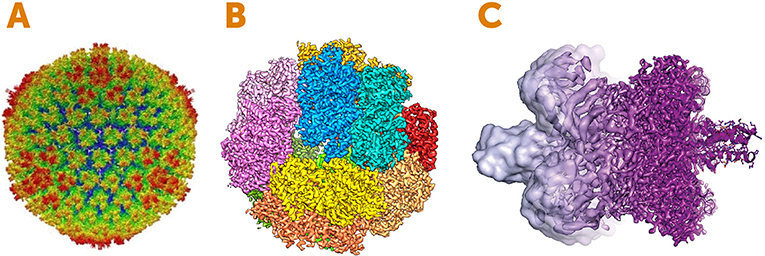
- איור 4 - תמונות שהתקבלו ממיקרוסקופ האלקטרונים הקְרִיוֹגֶנִי.
- (A) מבנה של נגיף מחולל מחלה בשם נגיף אָדֶנוֹ (Adenovirus). התמונה מראָה את המעטפת החיצונית הנקראת קפסיד (קוּפְסִית הנגיף), שהיא חלבון העוטף את החומר הגנטי של הנגיף. הצבעים מייצגים את המרחק ממרכז הכדור: החלקים הרחוקים ביותר מהמרכז מסומנים באדום, והחלקים הקרובים ביותר למרכז מסומנים בכחול. (האיור נלקח מ-[2]). (B) אנזים המשתתף בייצור אנרגיה במיקרובים. הצבעים מייצגים את תת־היחידות (החתיכות) הבודדות של האנזים. (האיור נלקח מ-[3]). (C) דוגמה לשיפור הרזולוציה של מיקרוסקופ האלקטרונים הקְרִיוֹגֶנִי בין 2013 (משמאל, בצבע סגול בהיר) לבין 2017 (מימין, בצבע סגול כהה). (איור: Martin Högbom, Stockholm University, מבוסס על איור מאת V. Falconieri).
מה צופן העתיד למיקרוסקופ האלקטרונים הקְרִיוֹגֶנִי?
האלקטרונים הם החלקיקים שֶיכולים לסייע לנו לדַמות מולקולות ביולוגיות זעירות בצורה הטובה ביותר. כדי שנוכל להבין עד כמה הם יעילים, הבה נשווה אותם לשני חלקיקים אחרים שנהוג להשתמש בהם לאותה המטרה: פּוּטוֹנים של קרני רנטגן (הדומים לחלקיקי האור, אך בעלי אורכי-גל קצרים), ונֵיטְרוֹנִים (חלקיקים הנמצאים בגרעין האטום). כאשר אנחנו מְחַשבים את כמות המידע שאנחנו מקבלים משימוש בחלקיק מסוים לעומת הנזק שאותו חלקיק מֵסֵב לדגימה, נוכל להעריך את מידת ההתאמה של החלקיק למטרת ההדמיה. בהשוואה זאת גילינו שהיעילות של אלקטרונים היא פי 1,000 לעומת קרני הרנטגן, והם טובים פי שלושה מהנֵיטרונים! לכן עמיתיי ואני התחלנו להשתמש באלקטרונים בִּמְקום בחלקיקים אחרים. כיום מיקרוסקופ האלקטרונים הקְרִיוֹגֶנִי מצליח מאוד, ומדענים רבים בתחום הביולוגיה המִבְנִית משתמשים בו.
עם זאת, עלינו לערוך עוד שיפורים משמעותיים במיקרוסקופ האלקטרונים הקְרִיוֹגֶנִי. אחד מהם הוא שיפור גלאֵי האלקטרונים, שעדיין אינם מספיק גדולים או יעילים, ודורשים מאיתנו להשתמש בְּמִספר גבוה של אלקטרונים יותר ממה שנדרש באופן תיאורטי. בנוסף, נוכל להתייעל אם נגביל עוד יותר את תנועת הדגימה (הן של מולקולות המים הן של המולקולות הביולוגיות) במפגש בֵּינה לבין קֶרֶן האלקטרונים [4, 5]. אנחנו מאמינים שתוך כ-5 שנים נוכל להתקדם משמעותית לעֵבר פתרון האתגרים הללו. משנעשה זאת, יהיה ברשותנו כלִי חזק עוד יותר מהקיים כיום, שבעזרתו נוכל לענות בדיוק רב יותר על שאלות ביולוגיות רבות, כמו איך פועל מנגנון החיים, וכיצד מִתְרַבִּים יְצוּרים חיים. המידע שאנחנו משיגים יכול לסייע לנו לשמור על בריאותם של אנשים, של בַּעֲלֵי החיים ושל הצמחים. אנחנו צופים למיקרוסקופ האלקטרונים הקְרִיוֹגֶנִי עתיד מזהיר!
המלצות למוחות צעירים
אני, ריצ'רד, רוצה לחלוק עימכם עצה מעשית שליוותה אותי לאורך הקריירה שלי, שאותה ניסח בכתביו פיטר מֶדָוָואר (Peter Medawar), שזכה בפרס נובל בתחום של פיזיולוגיה או רפואה בשנת 1960. לאחר שזכה בפרס הנובל, פיטר מדוואר פרסם שני ספרים: ''האומנות של מציאת הפתרונות'' ו''עצות למדענים צעירים''.
בספריו מדוואר אמר שיש הרבה דברים מעניינים במדע ובחיים. הוא טען שעלינו להתעניין בכל דבר, אך שצריך לבחוֹר משהו שאנחנו מתעניינים בו במיוחד ולהתמחות בו. יתרה מכך, הוא אמר שמדענים צריכים לעסוק בתחום שיצליח לייצר יֶדַע חדש בקרוב ולא בעוד 100 שנים, כי זה כבר יהיה מֵעֵבֶר לזמן חייהם. לדעתו המדע הוא אומנות הדברים הפְּתִירים, כלומר סוגיות שאפשר לפתור, ועל המדענים לערוך ניסויים שעובדים עכשיו, ולהיעזר בטכניקות עדכניות.
כשהייתי סטודנט צעיר לפיזיקה, תהיתי באיזה כיווּן הפיזיקה מתפתחת. אני זוכר שהכנתי רשימה של כל נושאי העתיד המעניינים. הרשימה כללה מחקר בנושא היתוך, הכולל הפקת כוח בלתי מוגבל מהיתוך מֵימָן. היא כללה גם פיזיקת חלקיקים באנרגיה גבוהה, שהובילה לגילוי של חלקיקים חדשים, למשל בוזון היגס (Higgs boson) וחלקיקים אחרים. ברשימה שלי הופיעה גם הפיזיקה של המצב המוצק, שקידמה את תעשיית המַחְשֶבִים ואת פיתוח המיקרו-שְבָבִים שֶמזינים מַחְשֶבִים. הנושאים המעניינים אותי כללו, בין השאר, גם ביו-פיזיקה, אסטרופיזיקה, קוסמולוגיה, חורים שחורים וכוכבי נויטרונים (איור 5). כל נושא שהייתי בוחר מבין כולם, היה מעניין ומלהיב באותה המידה. לכן, אם תחליטו לבחוֹר בקריירה מדעית, עליכם לבחור במשהו שמעניין אתכם, כדי שתהיה לכם מוטיבציה להמשיך במחקר ובעבודה מבלי שאף אחד יכריח אתכם לעשות זאת. כשאנחנו מתעניינים במשהו ועוסקים בו מתוך רצון פנימי, הקשיים שאנחנו נתקלים בהם בדרך לא יעצרו אתכם מלהתקדם – אפשר לראות אותם כאתגרים, ולהמשיך הלאה. משבחרתם נושא מעניין, ולפני שאתם ממשיכים לצעוד בַּשביל הזה, עדיף לברר כמה שיותר על הפעולות השונות שבהן תוכלו לנקוט כדי לחקור את הנושא. אם לאחַר חצי שנה או שנה של עבודה מאומצת תגלו שהרעיון שלכם לא היה כל כך מוצלח, אל תהססו לשקול שוב ו''לחשֵב מסלול מחדש''.

- איור - 5 כיצד בוחרים תחום מדעי?
- כשהייתי סטודנט לפיזיקה התעניינתי בנושאים רבים שהיו פרוסים בפניי. במבט לאחור, אני מבין שכולם היו ודאי מעניינים אותי באותה המידה. כשאתם בוחרים תחום, וַדאו כי אתם בוחרים בתחום שמעניין אתכם ושֶיספק לכם מוטיבציה לאורך זמן.
כיום המדע מתקדם במהירות רבה בהשוואה לְמה שהיה בעבר. לפני מאה שנה אפילו לא ידענו על קיוּמם של קרני רנטגן ואלקטרונים, ועכשיו יש ברשותנו מידע על כל הגֵנוּם האנושי, שיטות מתוחכמות לעבודה עם DNA, ויכולת להבין כמעט כל מִבְנֶה שנרצה. מאה השנים הבאות יהיו תקופה טובה מאוד לחיות בה, וכדאי לכם להיות מדענים! תיהנו מחייכם, והשקיעו בתחומים שהכי מעניינים אתכם!
חומרים נוספים
הרצאת הנובל של ריצ'רד הֶנְדֶרְסוֹן, שנת 2017. https://www.nobelprize.org/prizes/chemistry/2017/henderson/lecture/
מיקרוסקופ האלקטרונים הקְרִיוֹגֶנִי - ריצ'רד הֶנְדֶרְסוֹן ב-''Serious Science''.
https://www.youtube.com/watch?v=L6U–sYUF9s&t=262s
מסבירים: מהו מיקרוסקופ האלקטרונים הקְרִיוֹגֶנִי? (Chemistry World).
https://www.chemistryworld.com/news/explainer-what-is-cryo-electron-microscopy/3008091.article
מילון מונחים
ביולוגיה מבנית (Structural Biology): ↑ תחום בביולוגיה שעוסק באפיון המבנים של הרכיבים שמהם מורכבים החיים.
חלבון (Protein): ↑ מכוֹנָה ביולוגית זעירה המבצעת תפקידים חיוניים רבִּים בגוף.
אֶנְזִים (Enzyme): ↑ מולקולה ביולוגית המאיצה את התגובות הכימיות בגוף.
מידע גנטי (DNA) (Genetic Information): ↑ מידע שעובר מהורים לצאצאיהם, המכתיב את מאפייניו ואת התנהגותו של האורגניזם.
תֶּדֶר (Frequency): ↑ מִסְפָּר הפעמים שגל חוזר על עצמו בשנייה אחת.
אורך גל (Wavelength): ↑ המרחק שלאורכו צורת הגל חוזרת על עצמה.
מיקרוסקופ אלקטרונים (Electron Microscopy): ↑ טכניקה שמשתמשת באלקטרונים לדימוּת של מִבְנִים קטנים, ובכלל זה, של מולקולות ביולוגיות.
דיפרקציה (Diffraction): ↑ הדרך שבה חֶפֶץ גורם לפיזור של גל; לדוגמה, דגימה שגורמת לפיזור של אלקטרונים.
קירור-על (Supercooled): ↑ קירור מתחת לטמפרטורת הקיפאון תוך שמירה על מצב צבירה נוזלי וללא היווצרות גבישים.
מיקרוסקופ אלקטרונים בטמפרטורות נמוכות (Electron Cryomicroscopy): ↑ נקרא גם ''מיקרוסקופ אלקטרונים קְרִיוֹגֶנִי''. טכניקה שבה משתמשים באלקטרונים לצורך דימוּת של מולקולות ביולוגיות הנמצאות במים, תוך קירורן במהירות לטמפרטורות נמוכות.
הצהרת ניגוד אינטרסים
המחברים מצהירים כל המחקר נערך בהעדר כי קשר מסחרי או פיננסי שיכול להתפרש כניגוד אינטרסים פוטנציאלי.
תודות
ברצוננו להודות לאלכס ברנשטיין עבור האיורים, ולסוזן דיבד (Susan Debad) על עריכת הלשון של כתב היד באנגלית.
מקורות
[1] ↑ Dubochet, J., Lepault, J., Freeman, R., Berriman, J. A., and Homo, J.-C. 1982. Electron microscopy of frozen water and aqueous solutions. J. Microscopy 128:219–37. doi: 10.1111/j.1365-2818.1982.tb04625.x
[2] ↑ Liu, H., Jin, L., Koh, S. B. S., Atanasov, I., Schein, S., Wu, L., et al. 2010. Atomic structure of human adenovirus by cryo-EM reveals interactions among protein networks. Science 329:1038–43. doi: 10.1126/science.1187433
[3] ↑ Allegretti, M., Mills, D. J., McMullan, G., Kühlbrandt, W., and Vonck, J. 2014. Atomic model of the F420-reducing [NiFe] hydrogenase by electron cryo-microscopy using a direct electron detector. Elife 3:e01963. doi: 10.7554/eLife.01963
[4] ↑ Vinothkumar, K. R., and Henderson, R. 2016. Single particle electron cryomicroscopy: Trends, issues and future perspective. Q. Rev. Biophys. 49:e13. doi: 10.1017/S0033583516000068
[5] ↑ Henderson, R. 2015. Overview and future of single particle electron cryomicroscopy. Archiv. Biochem. Biophys. 581:19–24. doi: 10.1016/j.abb.2015.02.036
