ملخص
يستند هذا المقال إلى مقابلة أُجريت بين المؤلفَين. البيولوجيا البنيوية هي مجال يسعى إلى اكتشاف بِنى جميع المكونات التي تتكون منها الكائنات الحية؛ بدءًا من الجزيئات الموجودة في البشر والحيوانات الأخرى، مرورًا بالجزيئات الموجودة في الكائنات الحية الدقيقة، ووصولًا إلى الجزيئات التي تتكون منها النباتات. ولتحديد هذه البِنى، يستخدم علماء البيولوجيا البنيوية تقنيات تصوير متطورة أصبحت أكثر دقة في «رؤية» أو تحديد بنية الجزيئات الأصغر والأكثر تنوعًا. ويُعد الفحص المجهري الإلكتروني فائق البرودة أحد تقنيات التصوير المتقدمة والفعالة. ففي هذه التقنية، تُرسَل الإلكترونات عبر عينات مجمدة لتحديد بِنى الجزيئات المفردة، بمستويات تكبير كافية لرؤية الذرات. وتأخذنا هذه الصور خطوة إلى الأمام نحو فهم بنية اللبنات الأساسية للحياة ووظيفتها. في هذا المقال، سنعرّفك بالتطورات التي أدت إلى ما يُسمى «ثورة الاستبانة» في الفحص المجهري الإلكتروني فائق البرودة، التي كان الدكتور Henderson جزءًا منها والتي سمحت له في النهاية بتقاسم جائزة نوبل في الكيمياء في عام 2017.
فاز الدكتور Richard Henderson والأستاذ Jacques Dubochet والأستاذ Joachim Frank بجائزة نوبل في الكيمياء في عام 2017 لتطويرهم الفحص المجهري الإلكتروني فائق البرودة لتحديد البنية عالية الاستبانة للجزيئات الحيوية في المحلول.
عندما تتجلى أهمية النظرات: اكتشاف بِنى الجزيئات البيولوجية
تحتوي الكائنات الحية على العديد من البِنى التي تقوم بعمليات مهمة؛ ففي جسم الإنسان -مثلًا- نعرف أن ثمة أعضاء مصنوعة من الخلايا، وداخل هذه الخلايا العديد من العضيات والجزيئات التي تؤدي جميع الوظائف اللازمة للحفاظ على الحياة؛ مثل إنتاج الطاقة والتخلص من الفضلات والحركة والدفاع ضد العوامل الضارة (الشكل 1). ولفهم كيفية عمل الكائنات الحية وربما تحسين حياتها، علينا معرفة البِنى الموجودة في النظام البيولوجي والأنشطة التي تؤديها تلك البِنى. والبيولوجيا البنيوية هي المجال الذي يسعى إلى ملاحظة بِنى المكونات البيولوجية؛ ففي الماضي، كان العلماء سيبحثون أولًا عن الأنشطة المحددة التي كنا نعلم أنها تحدث في النظام البيولوجي، مثل تحويل مصدر واحد للطاقة إلى نوع آخر من الطاقة قابل للتخزين. وبعد أن نجد النشاط، كنا سنحدد الجزيئات التي شاركت فيه، والتي عادةً ما تكون بروتينات وإنزيمات، وعندها فقط نحدد بِنى تلك الجزيئات.
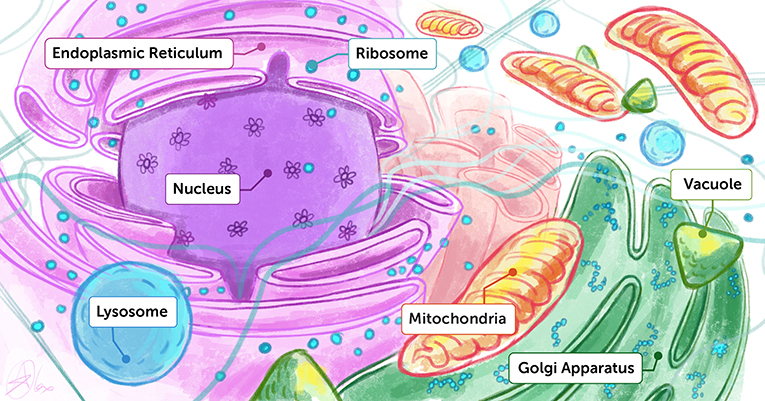
- شكل 1 - تأويل فنان للجزء الداخلي من الخلية.
- يمكنك التفكير في الجزء الداخلي من الخلية على أنه ملعب كثيف يحتوي على العديد من الجزيئات والعضيات المختلفة، كلٍ منها يؤدي وظائفه الفريدة. ونريد أن نعرف بِنى كلٍ من هذه اللبنات الأساسية البيولوجية ووظائفها حتى نفهم كيف تسير الحياة.
في عام 2000، شهد العالم ثورة في فهم المعلومات الجينية (الحمض النووي) وهي المعلومات المُخزنة في خلايانا، التي نرثها من آبائنا.
وقد جمع العلماء أول «مجموعة تعليمات» كاملة (تُسمى تسلسل قواعد الحمض النووي) للحزمة الكاملة من المعلومات الوراثية البشرية. ومنذ ذلك الحين، بدلًا من البحث عن نشاط، ثم العثور على جزيء، ثم تحديد بنية ذلك الجزيء، يمكن لعلماء البيولوجيا البنيوية استخدام المعلومات الجينية، التي تخبرهم عن جميع الإنزيمات والبروتينات الموجودة في الجسم. وفي عام 2000، عندما حدد العلماء الجينوم البشري، لم يكونوا حتى قد اكتشفوا حوالي 80% من الجزيئات المُشفرة في الحمض النووي البشري! وقد فتح هذا مسارًا جديدًا بالكامل في البيولوجيا البنيوية؛ فيمكننا الآن العثور على بِنى الجزيئات دون الحاجة إلى معرفة وظائفها أولًا. ولكن، كيف نعثر على بِنى هذه الجزيئات؟ الإجابة هي: باستخدام جزيئات صغيرة تسمى الإلكترونات!
الإلكترونات والفحص المجهري الإلكتروني
والإلكترونات هي جسيمات صغيرة مشحونة كهربائيًا موجودة في كل ذرة. وحركة هذه الإلكترونات هي التي تولّد الكهرباء، والإلكترونات هي أيضًا مصدر الضوء والأشكال الأخرى من الإشعاع الكهرومغناطيسي مثل الأشعة السينية. هل تصدق أنه حتى عام 1895 لم يكن أحد يعلم بوجود الإلكترونات؟ في ذلك العام، تعرّف العلماء لأول مرة على الإلكترونات وأطلق عليها جيه جيه طومسون هذا الاسم، وهو عالم في قسم الفيزياء بجامعة كامبريدج في المملكة المتحدة. وبعد ثلاثين عامًا، في عام 1935، أوضح جي بي طومسون (ابن جيه جيه طومسون) أن الإلكترونات تتصرف كجسيمات وموجات؛ فهي لها تردد وطول موجي، تمامًا مثل الموجات الأخرى. وقد حاز جيه جيه وجي بي طومسون على جائزتي نوبل: لاكتشاف دور الإلكترون كجسيم واكتشاف دوره كموجة.
وبعد ذلك بفترة قصيرة، أدرك العلماء أنه إذا كانت الإلكترونات تتصرف مثل الموجات، فإنها بطريقةٍ ما يجب أن تتصرف مثل الضوء؛ لأن الضوء يمكنه أيضًا التصرف كموجة. لذا، فكّر العلماء أنه ربما يمكنهم استخدام الإلكترونات لإضاءة العينات متناهية الصغر التي أرادوا النظر إليها، بالطريقة نفسها التي يمكننا بها النظر إلى جسمٍ ما بأعيننا أو بالكاميرا أو بالمجهر العادي، ولكن باستخدام الإلكترونات بدلًا من الضوء المرئي. وقد كانت هذه بداية الفحص المجهري الإلكتروني. يُعد الفحص المجهري الإلكتروني تقنية تصوير فعالة للغاية. فللإلكترونات طول موجي قصير للغاية، أقصر 100.000 مرة تقريبًا من الطول الموجي للضوء. ويمكنك التفكير في الطول الموجي على أنه معيار «تكبير»؛ فكلما كان الطول الموجي أصغر، زادت قدرتنا على «تكبير» العينة. ويعني هذا أن الصور المُلتقطة بالإلكترونات تمتاز بمستوى عالٍ جدًا من التفاصيل، وهو ما يُسمى بالاستبانة العالية. ولما كان الفحص المجهري الإلكتروني يتسم باستبانته العالية، فيمكن استخدامه لاكتشاف بِنى الجزيئات متناهية الصغر بطريقة لم تكن ممكنة من قبل.
كيف يعمل الفحص المجهري الإلكتروني؟
في الفحص المجهري الإلكتروني، يظهر شعاع نشط من الإلكترونات من مصدر إلكترونات ويمر عبر العينة الخاضعة للدراسة (الشكل 2A).

- شكل 2 - الفحص المجهري الإلكتروني.
- (A) في المجهر الإلكتروني، يطلق مصدر الإلكترونات شعاعًا من الإلكترونات الساخنة النشطة التي تمر عبر عينة موجودة داخل حجرة تفريغ. وعندما تتفاعل الإلكترونات مع العينة، تنعرج (تتبعثر) ثم تُجمع وتُركز بواسطة عدسات خاصة قبل أن تُكتشف بواسطة كاشف الإلكترون. (B) مجهر إلكتروني من جامعة كامبريدج (المملكة المتحدة)، يسمح للعلماء بتصوير العينات البيولوجية المجمدة (حقوق الصورة: University of Cambridge).
عندما تمر الإلكترونات عبر العينة، تتفاعل مع ذراتها و تنعرج أو تنحرف عن مسارها بطريقة خاصة بترتيب الذرات التي تصادفها. وبهذه الطريقة، «تلتقط» الإلكترونات بنية المادة أثناء عبورها فيها. وبعد انعراج الإلكترونات، تُجمع وتُركز باستخدام العدسات (مثل العدسات الموجودة داخل الكاميرا)، ثم تُسجل بواسطة كاشف الإلكترون. وفي هذه المرحلة، يكون لدى العلماء صورة للإلكترونات التي انعرجت عن العينة، وعليهم أن يحولوها إلى صورة للعينة نفسها. ويستند هذا التحويل إلى فيزياء بسيطة تصف العلاقة بين جسم مُقاس والصورة الناتجة. ويعتمد التحويل على العديد من العوامل، منها الطول الموجي للإلكترونات والعدسات المُستخدمة؛ ولكن كل هذا يعتني به خبراء الفحص المجهري.
التحديات التي ينطوي عليها الفحص المجهري الإلكتروني
يمكن للإلكترونات أن تساعدنا في الحصول على صور مميزة للجزيئات، غير أن ثمة تحديات كبيرة ينبغي التغلب عليها عند استخدامها لتصوير الجزيئات البيولوجية. أولًا، كما تخبرنا فيزياء الكم، فإن الإلكترونات الفردية ليست «منطقية»؛ فعندما تطرح عليها سؤالًا (مثلًا، ماذا يحدث عندما تلتقي بجزيء معين)، فإنها لا تقدم إجابة محددة مثل الإنسان. بل لديها احتمالية (إمكانية) للمشاركة في كل نتيجة محتملة؛ ففي عالم الإلكترونات، يحدث كل ما يمكن أن يحدث، مع وجود احتمال معين لكل خيار. ويعني هذا أن العلماء عليهم جمع العديد من الإجابات من العديد من الإلكترونات، والجمع بين المعلومات بذكاء للحصول على الإجابة الشاملة. ولتحقيق ذلك، نضيء العينة بملايين الإلكترونات ونستخدم المتوسط العام لخصائصها للحصول على إجابة معقولة.
ثانيًا، يمكن للإلكترونات أن تتلف العينة، لأنها نشيطة للغاية وعليها أن تمر عبر العينة للوصول إلى الكاشف. ويمكن أن تصل درجات حرارتها إلى ألفي مليون درجة مئوية؛ وعلى سبيل المقارنة يغلي الماء عند 100 درجة مئوية!
ويمكن لهذه الإلكترونات فائقة النشاط وأي نوع آخر من الإشعاع النشط سحب الإلكترونات من جزيئات العينة. ويؤدي هذا إلى تغيير أشكال جزيئات العينة وخصائصها، لأن الجزيئات البيولوجية حساسة نسبيًا. وبالتالي، من الصعب على العلماء الحصول على معلومات كافية عن بنية جزيء بيولوجي قبل تدميره. وتتمثل إحدى طرق التغلب على هذا التحدي في التقاط صور للعديد من الجزيئات المتطابقة المنفصلة-500 على الأقل في حالة الفحص المجهري الإلكتروني- وحساب متوسط الصور للحصول على بنية الجزيء النموذجي. ومن الطرق الأخرى التي يمكننا التعامل بها مع هذا التحدي هي تبريد العينة بطريقة خاصة تجعلها أكثر مقاومة لتلف الإلكترون؛ وسيرد وصفها في القسم التالي.
ولكن ثمة تحدٍ آخر ينبع من حقيقة أن الإلكترونات تنعرج بمجرد اقترابها من أي ذرات. ويعني هذا أنه يجب أن يكون ثمة مسار واضح بين مصدر الإلكترونات والعينة، بحيث تصل الإلكترونات إلى الجزيئات المطلوبة ولا تتشتت بسبب الجزيئات الأخرى -حتى الأكسجين والنيتروجين في الهواء- الموجودة في الطريق. وبعبارةٍ أخرى، يجب على العلماء إنشاء فراغ حول العينة في المجهر الإلكتروني. ولما كانت الجزيئات البيولوجية موجودة دائمًا في محاليل تحتوي على الماء (فكّر مثلًا في الجزيئات الموجودة في دمك)، فالمشكلة هي أن الماء يتبخر في الفراغ، وتجف العينة. وغالبًا ما يؤدي هذا إلى تلف الجزيئات البيولوجية في العينة. للتغلب على هذا التحدي، استغل علماء البيولوجيا النووية الخصائص الفريدة للماء.
هل يمكن أن يظل الماء سائلًا في حالة البرودة الشديدة؟
ها هي تجربة رائعة يمكن أن تجربها في المنزل لفهم أحد الخصائص الفريدة للماء (الشكل 3). خذ جرة فارغة بها غطاء واملأها بالماء. حاول التأكد من عدم وجود فقاعات هواء في الجرة من خلال شد الغطاء بإحكام تحت الماء وضعها في المجمد. اترك الجرة في المجمد لمدة يوم، حينئذ ستكون درجة حرارة الماء قد انخفضت إلى-10 درجاتمئوية أو-20 درجةمئوية (يصبح الماء عادةً مثلجًا عند درجة حرارة 0 درجة مئوية). وفي اليوم التالي، اخرج الجرة من المجمد وألقِ نظرة عليها؛ هل تحول الماء إلى ثلج صلب، أم ظل سائلًا؟
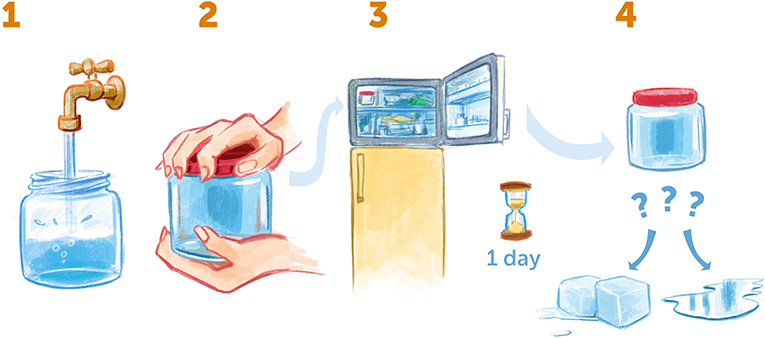
- شكل 3 - التبريد الفائق للمياه في المنزل.
- (1) خذ جرة فارغة واملأها تمامًا بالماء وتأكد من عدم وجود فقاعات هواء في الداخل. (2) اغلق الجرة بإحكام و(3) ضعها في المجمد لمدة يوم. (4) ثم أخرج الجرة. هل تجمد الماء أم لا يزال سائلًا؟ إذا كان لا يزال سائلًا، فقد صنعت ماءً فائق البرودة!
في أغلب الأحيان، ستجد أن الماء ما زال سائلًا—فهو مُبرد تبريدًا فائقًا، مما يعني أنه مُبرد إلى درجة حرارة أقل من درجة حرارة التجمد (0 درجة مئوية)، ولكن دون أن يتحول إلى ثلج. وفي تجاربنا، نريد أن نبرد الماء بدرجة أكبر، إلى أقل من-170 درجة مئوية، لأنه يصبح ثابتًا ومستقرًا تمامًا عند درجة الحرارة هذه. ونريد أيضًا أن نتجنب تكوين بلورات الجليد، لأنها تتداخل مع قياساتنا. ولتحقيق هذا، علينا استخدام طريقة تبريد خاصة طُورت في مختبر Jacques Dubochet، الذي تقاسم جائزة نوبل في الكيمياء معي، أنا Richard Henderson وJoachim Frank في عام 2017. في هذه الطريقة، نستخدم الإيثان أو البروبان السائل شديد البرودة (وهما مادتان موجودتان في الغاز الطبيعي، مصنوعتان من الكربون والهيدروجين)، المبردين إلى درجة حرارة-185 درجة مئوية.
ثم نغمس غشاءً مائيًا رفيعًا للغاية في سائل الإيثان/البروبان المبرد، وسيبرد الماء بسرعة كبيرة في حوالي 1/1.000 من الثانية؛ أي أنه ليس لديه وقت لتشكيل بلورات جليدية منظمة ويظل في شكل سائل غير منظم [1] وهو ما نطلق عليه الجليد غير المتبلور. وبهذه الطريقة، نحصل على ماء فائق البرودة.
الصيغة السحرية للإلكترونات الساخنة والعينات الباردة
وقد تبين أن الأغشية المائية الرفيعة فائقة التبريد رائعة لتعليق الجزيئات البيولوجية التي نريد تصويرها بمجاهر إلكترونية. وعندما نضيف خطوة التبريد هذه إلى عملية التصوير، تُسمى الفحص المجهري الإلكتروني فائق البرودة. يسمح الفحص المجهري الإلكتروني فائق البرودة لنا بالتعامل مع اثنين من التحديات المشار إليها أعلاه: فهو يساعد على استقرار العينة، مما يجعلها أكثر مرونة في مواجهة التلف بواسطة الإلكترونات عالية الطاقة، ويسمح للجزيئات البيولوجية بأن تكون في بيئتها المائية الطبيعية، دون تبخير الماء بسبب الفراغ. وثمة ميزة أخرى مهمة: فعلى عكس معظم السوائل الأخرى، يتمدد الماء عندما يُبرد إلى أقل من 4 درجات مئوية. وتساعد هذه الميزة الجزيئات البيولوجية على أن تظل غير تالفة عندما تكون في الماء فائق البرودة. وإذا تقلص الماء عند تبريده، فسوف يضغط على الجزيئات وربما يكسرها.
وتسمح لنا طريقة التصوير بالفحص المجهري الإلكتروني فائق البرودة البسيطة إلى حدٍ ما على الرغم من فعاليتها الشديدة، بتصوير الجزيئات البيولوجية باستبانة كانت بعيدة المنال في السابق. ولهذا السبب يُشار إليها أحيانًا بـ «ثورة الاستبانة».
ويوضح الشكل 4 أمثلة على الصور الجميلة التي حصلنا عليها باستخدام الفحص المجهري الإلكتروني فائق البرودة؛ فنحن نتعامل مع مقاييس صغيرة للغاية تعادل -10 من النانومتر، وهي أقل من 1/1.000 من عرض شعرة الإنسان! ونأمل أن تكون الآن قد بدأت في تقدير أعجوبة الفحص المجهري الإلكتروني فائق البرودة.
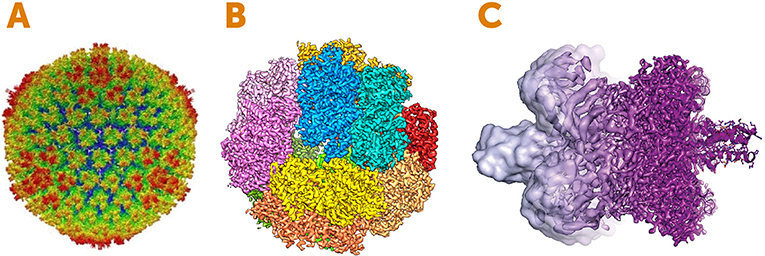
- شكل 4 - صور أُنشأت باستخدام الفحص المجهري الإلكتروني فائق البرودة.
- (A) بنية فيروس مسبب للأمراض يُسمى الحمى الغُدية. توضح الصورة السطح الخارجي المُسمى القفيصة، وهي غلاف البروتين الذي يلف المادة الوراثية للفيروس. وتمثل الألوان المسافة من مركز الكرة: فالأحمر هو الأبعد عن المركز والأزرق هو الأقرب. (B) إنزيم له دور في توليد الطاقة في الميكروبات. وتمثل الألوان الوحدات الفرعية الفردية (قطع) للإنزيم.
(C) مثال على مدى تحسن استبانة الفحص المجهري الإلكتروني فائق البرودة بين عام 2013 (اليسار، الأرجواني الفاتح) وعام 2017 (اليمين، الأرجواني الداكن). (حقوق الصور:
الصورة (A) مُعدلة من [2]؛
الصورة (B) مُعدلة من [3]؛
الصورة (C) Martin Högbom, Stockholm University, استنادًا إلى صورة لـV. Falconieri.
ما الذي يحمله المستقبل للفحص المجهري الإلكتروني فائق البرودة؟
الإلكترونات هي أفضل جسيمات يمكن استخدامها لتصوير الجزيئات البيولوجية الدقيقة. ولإعطائك فكرة عن مدى جودتها، دعنا نقارنها بجسيمين آخرين شائعي الاستخدام: فوتونات الأشعة السينية (تشبه جسيمات الضوء ولكنها ذات أطوال موجية قصيرة)، والنيوترونات (جسيمات من نوى الذرات). وعندما نحسب كمية المعلومات التي نتلقاها من استخدام جسيم معين مقارنةً بالتلف الذي يحدثه الجسيم في العينة، نحصل على قياس لمدى جودة الجسيم في التصوير. وباستخدام تلك العملية الحسابية، تكون الإلكترونات أفضل 1000 مرة من الأشعة السينية، وأفضل ثلاث مرات من النيوترونات! ولهذا السبب بدأت أنا وزملائي في استخدام الإلكترونات بدلًا من الجسيمات الأخرى منذ سنوات عديدة. وفي الوقت الحاضر، أصبح الفحص المجهري الإلكتروني فائق البرودة ناجحًا للغاية لدرجة أن عدد علماء البيولوجيا النووية الذين يستخدمونه مرتفع ويتزايد بسرعة.
ولكن ما زالت توجد تحسينات مهمة يلزم إجراؤها في الفحص المجهري الإلكتروني فائق البرودة؛ أحدها هو تحسين كاشفات الإلكترونات، التي لا تزال غير كبيرة ولا فعالة بما فيه الكفاية وتتطلب منا استخدام عدد من الإلكترونات أكثر مما هو مطلوب نظريًا. وسيكون من المفيد أيضًا تقليل حركة العينة (كل من جزيئات الماء والجزيئات البيولوجية) عندما تتلامس مع حزمة الإلكترون [4, 5]. ونعتقد أنه في غضون 5 سنوات تقريبًا، سيكون ثمة تقدم كبير لمواجهة هذه التحديات. وستتكون لدينا حينها أداة أقوى ستسمح لنا بفهم العديد من الأسئلة البيولوجية بصورة أفضل، مثل كيف تسير الحياة وكيف تعيد إنتاج نفسها. وقد تساعدنا المعلومات التي نحصل عليها في الحفاظ على صحة الأشخاص والحيوانات والنباتات. ويمكننا توقع مستقبل مشرق للغاية للفحص المجهري الإلكتروني فائق البرودة!
نصائح للعلماء الصغار
أريد أنا -Richard- أن أخبركم ببعض النصائح العملية التي اتبعتها طوال مسيرتي المهنية. وهي مستقاة من مؤلفات بيتر مدور، الحائز على جائزة نوبل في علم وظائف الأعضاء أو الطب في عام 1960.
بعد حصوله على جائزة نوبل، نشر بيتر مدور كتابين بعنواني «The Art of the Soluble»، و«Advice to a Young Scientist». وقد قال في كتابه إن ثمة العديد من الأشياء المثيرة للاهتمام في العلم والحياة، وأن علينا الاهتمام بكل شيء. ولكن ينبغي لنا أيضًا أن نختار شيئًا يثير اهتمامنا بشكل خاص للعمل عليه. وعلاوةً على ذلك، أشار إلى أن العلماء عليهم العمل على شيء من شأنه أن ينجح في إنتاج معرفة جديدة على المدى القريب، وليس في غضون 100 عام، لأن هذا يتجاوز عمر العالم. فقد كانت فكرته أن العلم هو فن ما يمكن حله، أي المشكلات التي يمكن حلها. فينبغي للعلماء إجراء تجارب تؤتي أكلها الآن، بالتقنيات الحالية.
فعندما كنت طالبًا شابًا في الفيزياء، تساءلت إلى أين تتجه الفيزياء، وأتذكر أنني أعددت قائمة بجميع الموضوعات المثيرة للاهتمام في المستقبل. كان ثمة بحث عن الاندماج، تضمن إنتاج طاقة غير محدودة من اندماج الهيدروجين. ثم ظهرت فيزياء الجسيمات عالية الطاقة، التي أدت إلى اكتشاف جسيمات جديدة، منها بوزونات هغز وغيرها الكثير. وكان لدينا فيزياء الجوامد، التي طورت صناعة الكمبيوتر والرقائق الدقيقة التي تغذي أجهزة الكمبيوتر. ومن الموضوعات الأخرى التي كانت مثيرة للاهتمام -على سبيل المثال لا الحصر- الفيزياء الحيوية والفيزياء الفلكية وعلم الكونيات والثقوب السوداء والنجوم النترونية (الشكل 5). إذا كنت قد اخترت أيًا من تلك الموضوعات لدراستها، كنت سأجدها مشوقة ومثيرة للاهتمام أيضًا. لذلك، إذا قررت خوض غمار العلم، فعليك أن تختار شيئًا يثير اهتمامك، بحيث تتابع دراسته والعمل عليه دون أن يجبرك أي شخص على ذلك. فعندما تكون مهتمًا ولديك دوافع ذاتية، لن تنزعج بشدة إذا واجهتك صعوبات؛ بل ستعتبرها مجرد تحدٍ وتتجاوزها. وبمجرد أن تختار موضوعًا مثيرًا للاهتمام، وقبل أن تسلك بالفعل هذا الاتجاه، من الأفضل أن تعرف قدر الإمكان عن الأنشطة المختلفة التي يمكنك متابعتها لدراسة الموضوع. وإذا اتضح لك بعد 6 أشهر أو سنة من بذل قصارى جهدك أن فكرتك لم تكن جيدة للغاية، فلا تتردد في التفكير مرة أخرى والبحث عن اتجاه جديد.

- شكل 5 - اختيار مجال علمي.
- عندما كنت طالبًا للفيزياء، كان ثمة العديد من الموضوعات المثيرة للاهتمام التي يمكنني الاختيار منها. وبعد فوات الأوان، أدركت أن جميعها كانت ستثير اهتمامي بالقدر نفسه. لذا، عندما تختار مجالًا، تأكد من اختيار شيء تجده مثيرًا للاهتمام ويبقيك متحفزًا لفترة طويلة.
يتحرك العلم اليوم بسرعة كبيرة مقارنةً بالماضي. فقبل 100 عام فقط، لم نكن نعرف حتى عن وجود الأشعة السينية والإلكترونات، والآن لدينا معلومات عن الجينوم البشري بأكمله، ولدينا طرق متطورة للعمل مع الحمض النووي، ويمكننا اكتشاف بنية أي شيء نريده تقريبًا. وستكون الـ100 عام القادمة عصرًا جيدًا للبقاء على قيد الحياة ولتكون عالمًا. فاستمتع بحياتك واستثمر نفسك فيما تراه مثيرًا للاهتمام!
مواد إضافية
Richard Henderson Nobel Lecture 2017
Electron Cryomicroscopy—Richard Henderson at Serious Science
Explainer: What is cryo-electron microscopy (Chemistry World)
مسرد للمصطلحات
البيولوجيا البنيوية (Structural Biology): ↑ هي أحد مجالات علم الأحياء التي تصف بِنى المكونات التي تتكون منها الكائنات الحية.
البروتين (Protein): ↑ هو آلة بيولوجية صغيرة تؤدي العديد من الأدوار الأساسية في الجسم.
الإنزيم (Enzyme): ↑ هو جزيء بيولوجي يسرِّع التفاعلات الكيميائية في الجسم.
المعلومات الجينية (الحمض النووي) Genetic Information (DNA): ↑ هي المعلومات التي تنتقل من الآباء إلى نسلهم، والتي تحدد خصائص الكائن الحي وسلوكه.
التردد (Frequency): ↑ هو عدد المرات التي تكرر فيها الموجة نفسها في ثانية واحدة.
الطول الموجي (Wavelength): ↑ هو المسافة التي يكرر فيها شكل الموجة نفسه.
الفحص المجهري الإلكتروني (Diffraction): ↑ هو تقنية تستخدم الإلكترونات لتصوير البِنى الصغيرة، بما في ذلك الجزيئات البيولوجية.
الانعراج (Supercooled): ↑ هو تشتت الموجة بواسطة جسمٍ ما؛ مثل تشتت الإلكترونات بواسطة عينة.
فائق التبريد (Supercooled): ↑ مُبرد تحت درجة حرارة التجمد مع بقاء السائل (أي بدون تبلور).
الفحص المجهري الإلكتروني فائق البرودة (Electron Cryomicroscopy): ↑ هو تقنية تستخدم الإلكترونات لتصوير الجزيئات البيولوجية الموجودة في الماء والتي تُبرد إلى درجات حرارة منخفضة بسرعة كبيرة.
إقرار تضارب المصالح
يعلن المؤلفون أن البحث قد أُجري في غياب أي علاقات تجارية أو مالية يمكن تفسيرها على أنها تضارب محتمل في المصالح.
إقرار
نتوجه بالشكر لأليكس بيرنشتاين على توفير الأشكال وسوزان ديباد على تحرير المقال.
المراجع
[1] ↑ Dubochet, J., Lepault, J., Freeman, R., Berriman, J. A., and Homo, J.-C. 1982. Electron microscopy of frozen water and aqueous solutions. J. Microscopy 128:219–37. doi: 10.1111/j.1365-2818.1982.tb04625.x
[2] ↑ Liu, H., Jin, L., Koh, S. B. S., Atanasov, I., Schein, S., Wu, L., et al. 2010. Atomic structure of human adenovirus by cryo-EM reveals interactions among protein networks. Science 329:1038–43. doi: 10.1126/science.1187433
[3] ↑ Allegretti, M., Mills, D. J., McMullan, G., Kühlbrandt, W., and Vonck, J. 2014. Atomic model of the F420-reducing [NiFe] hydrogenase by electron cryo-microscopy using a direct electron detector. Elife 3:e01963. doi: 10.7554/eLife.01963
[4] ↑ Vinothkumar, K. R., and Henderson, R. 2016. Single particle electron cryomicroscopy: Trends, issues and future perspective. Q. Rev. Biophys. 49:e13. doi: 10.1017/S0033583516000068
[5] ↑ Henderson, R. 2015. Overview and future of single particle electron cryomicroscopy. Archiv. Biochem. Biophys. 581:19–24. doi: 10.1016/j.abb.2015.02.036
