תַקצִיר
החושים שלנו מעצבים את חוויית החיים שלנו. אנו רואים, שומעים, מריחים, נוגעים בדברים שסביבנו וטועמים מְהם. כך אנו מתוודעים לעולם. במחקר שלי אני חוקר קולטנים – מבנֵי חישה קטנים הנמצאים על קרום התא (מֶמְבְּרַנָה), המגיבים לגירויים מהסביבה או מתוך הגוף. במאמר זה אספר לכם על קולטנים הרגישים לכאב ולחוֹם, שמגיבים גם לטמפרטורות גבוהות וגם לחומרים חריפים, כמו פִּלפל חריף. אנו מאמינים שככל שנמשיך לחקור את מבנֵי הקולטנים הללו ולהבין באופן טוב יותר את צורת פעולתם , נוכל לפתח ביעילות ובבטיחות תרופות חדשות לטיפול בכאב מתמשך (כרוני). קִראו את המאמר הזה כדי ללמוד כיצד הפִּלפל החריף פתח לנו את הצוהר לפתרון כמה מהתעלומות הגדולות של תחושת הכאב. תגלית זו סללה את הדרך לפיתוח עתידי של טיפולי כאב חדשניים.
כחומרי רקע למאמר זה מומלץ לקרוא שני מאמרים שפורסמו בעבר על טכניקת הרישום התוך-תאי (Patch clamp) ועל מיקרוסקופ האלקטרונים הקריוגני.
פרופסור דייוויד ג’וּלְיוּס זכה בפרס נובל לפיזיולוגיה או לרפואה לשנת 2021 עם פרופסור אָרְדֶם פָּטָפּוּטְיָאן (Ardem Patapoutian) עבור גילוי קולטנים לטמפרטורה ולמגע.
האם יש סיבה לכאב?
עבור כל בעלי החיים, ובכלל זה בני האדם, הכאב הוא תחושה חשובה מאוד. הכאב מאותת לנו שנפצענו ושעלינו לטפל בעצמנו, ומתי עלינו לחדול מפעילוּת שעלולה להזיק לנו, או להימנע ממנה כליל. במונחים מדעיים הכאב הוא חלק מחוש המישוש – הוא היכולת לחוש מגע, טמפרטורה, כאב, את מיקום הגפיים שלנו ואת התנועה במרחב שסביבנו. יכולת החישה מתבצעת על ידי מבנֵי חישה קטנים הפזורים בכל הגוף, אותם אנו מכנים קולטנים (רצפטורים). הקולטנים ממוקמים על קרום התא של תאֵי העָצָב, ומגיבים לגירויים מהסביבה (למשל, נוזל חם בכוס השתייה). כתוצאה מכך, תאֵי העָצָב החישתיים הללו שולחים אותות לאזורי המוח הרלוונטיים, שם אותם האותות עוברים תהליכים של עיבוד ופענוח (איור 1).
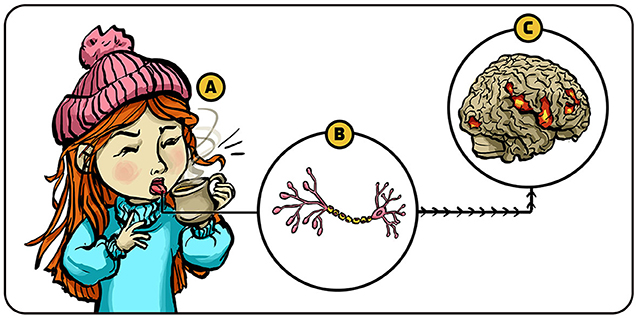
- איור 1 - חוש המישוש.
- (A) אנו מרגישים גירויים, כמו טמפרטורה וכאב, באמצעות מִבְנים זעירים הנקראים קולטנים. הקולטנים ממוקמים על פני קרום התא של תאֵי עָצָב מיוחדים (הממוקמים בלשון שלנו, לדוגמה). (B) כאשר הקולטנים הללו חווים גירוי רלוונטי הם מייצרים בתא העָצָב אותות חשמליים הנשלחים למוח. (C) אזורים מסוימים במוח מפענחים את האותות הללו – בדוגמה זו הם ”מודיעים” לילדה שהיא שותה נוזל חם.
במאמר זה נתמקד בסוג אחד של קולטנים הנקראים קולטנים של תעלות יוֹנִים. קולטנים אלה משתמשים בתעלות יוֹנִים – ”מנהרות” קטנות או ”שערים” הקיימים בקרום התא – כדי ליצור אותות חשמליים בתגובה לגירויים מהסביבה (למידע נוסף על תעלות יוֹנִים, קִראו את המאמר הזה באוסף הנובל). קולטנים של תעלות היוֹנִים הם מכונות איתות מסובכות ומרתקות, שיש להן תפקיד מרכזי ביכולתנו לחוש את הסביבה הפנימית והחיצונית שלנו. במרוצת השנים המדענים פיתחו כלים מתקדמים לחקר המבנים והתפקודים של קולטני תעלות היונים. לדוגמה, אנו יכולים להשתמש בשיטת הדמיה מיוחדת הנקראת מיקרוסקופיה אלקטרונית קְרִיוֹגֶנִית, שבה אנו שולחים אלקטרונים דרך דגימות קפואות ומצלמים תמונות מפורטות ביותר של הקולטנים הללו. בעזרת תמונות אלו ביכולתנו לִבנות מודלים תלת־ממדיים של הקולטנים. אנו יכולים גם להשתמש בשיטה מתוחכמת בשם טכניקת רישום תוך-תאי (Patch Clamp) כדי למדוד מטענים חשמליים הזורמים דרך תעלות יונים אלו – כך אנו יכולים לחקור את ההתנהגות החשמלית של קולטני תעלות יונים.
שיטות אלו עוזרות לנו לענות על שאלות מדעיות בסיסיות על אודות הכאב: איך אנשים חשים כאב, ומה יכול לעזור לנו לפתח תרופות חדשות לשיכוך הכאב? כאשר הקולטנים של תעלות היונים הרגישים לכאב פועלים כראוי, הם עוזרים לאנשים להגן על עצמם מפני נזק גופני. עם זאת, מִדֵי פעם משהו משתבש במנגנון ההגנה הזה, והוא יוצא משליטה, ואז אנשים עלולים לחוות כאב כְרוֹנִי – זהו כאב מתמשך שלא נראה שיעיל בהגנה עלינו. עד כה, תרופות קוֹנְבֶנְצְיוֹנָלִיוֹת לשיכוך כאבים, הנקראות מְשַׁכְּכֵי כאבים (כגון אַסְפִּירִין), היו יעילות מאוד בטיפול בכאב חריף, אך לא בכאב מתמשך. בנוסף לכך, מְשַׁכְּכֵי כאבים נפוצים כמו מוֹרְפְיוּם הם ממַכְּרִים ועלולות להיות להם תופעות לוואי שאינן רצויות, כולל סחרחורת, בחילות והקאות [1].
שימוש יתר במשככי כאבים ממַכְּרִים תרם לְמה שמכוּנֶה משבר האוֹפִּיוֹאִידִים, במהלכו אנשים רבים התמכרו למְשַׁכְּכֵי כאבים, השתמשו בהם באופן לא נכון ופגעו בבריאותם. אנו מקווים שהבנה טובה יותר של קולטני הכאב – ובמיוחד של קולטני הכאב של תעלות היונים – תעזור לנו לפתח מְשַׁכְּכֵי כאבים חדשים שיטפלו בכאב מתמשך ביעילות רבה יותר. תרופות כאב חדשות כאלה יעזרו לנו ככל הנראה להתמודד עם משבר האופיואידים. לפני שנבחן את התרופות החדשות, שעשויות להתפתח בעקבות הגילויים מהמחקר על קולטני הכאב, אספר לכם קצת על משפחת קולטני הכאב שאני ועמיתיי גילינו.
פלפלים חריפים וקולטני כאב
תמיד הוקסמתי מהדרך שבה החושים פועלים, ומהצורות שבהן כימיקלים מסוימים, במיוחד אלו הנמצאים בחומרים טבעיים, משפיעים על המוח ועל הגוף. במחקר שלי שילבתי את שני הנושאים המרתקים הללו במטרה להבין טוב יותר את חוש המישוש. ענייֵן אותי במיוחד להבין כיצד בני אדם מְזַהִים גירויים שעלולים להזיק לגוף באמצעות תהליך שנקרא נוֹצִיצֶפְּצִיָה.
בשנות של המאה הקודמת המדענים גילו שהקָפְּסָאִיצִין – המרכיב בפִּלפל החריף הגורם לתחושת הצריבה – מעורר תחושת כאב בעיניים של חולדות על ידי הפעלת קולטני נוֹצִיצֶפְּצִיָה בקצוותיהם של עצבים תחושתיים מסוימים [2]. עשור לאחר מכן, המדענים העלו השערה שהקפסאיצין מעורר כאב בכך שהוא מאפשר ליונים, כולל יוני סידן, לזרום לתוך תאֵי העָצָב התחושתיים המעורבים בנוֹצִיצֶפְּצִיָה [3]. ממצא זה העניק לי ולתלמידים שלי את הרמזים הדרושים לנו כדי להתמודד עם השאלות הבאות: האם יש קולטן מסוים לקפסאיצין בתאֵי עָצָב תחושתיים? אם כן, איך הוא נראה, ואיזה תפקיד יש לו ביכולת לחוש כאב?
כדי לענות על השאלות הללו, תלמידיי ואני החלטנו לחפש את הגֵן המקודד לחלבון המסוים של הקולטן לקפסאיצין. כיוון שלא ידענו איך נראה הקולטן הזה – או הגֵן המתאים לו – נאלצנו להסתפק ברמזים ספורים בלבד שהִנְחו אותנו בתהליך החיפוש. הדוֹגְמָה המרכזית של הביולוגיה המולקולרית גורסת שכדי לייצר כל חלבון שהוא, ובכלל זה את החלבונים של קולטני כאב, צריך לייצר מולקולה בשם mRNA, המכילה את ההוראות לייצור החלבון המסוים מהדנ”א. החלטנו לקחת תאֵי עָצָב המגיבים לכאב (איור 2A), לבודד את ה-mRNA המקוֹדֵד לקולטני הכאב (איור 2B), ולאחר מכן להפוך את ה-mRNA הזה בחזרה להוראות הדנ”א (הגֵן) המקוֹדֵד לקולטן הכאב (איור 2C) [4] (למידע נוסף על mRNA, קִראו את המאמר הזה באוסף הנובל; כדי ללמוד עוד על האופן שבו אפשר להפוך mRNA לדנ”א, קִראו את המאמר הזה באוסף הנובל).
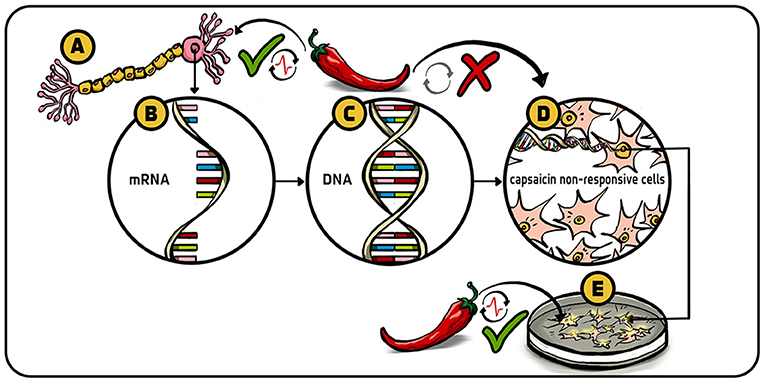
- איור 2 - החיפוש אחר גן הקולטן של הקָפְּסָאִיצִין.
- (A) תא העָצָב הקולט, מגיב לקפסאיצין ובסופו של דבר מעביר מידע על כאב למוח. (B) הסרנו מהַתאים הללו את ה-mRNA ששיערנו שעשוי להיות מעורב בקידוד הקולטן הרגיש לקָפְּסָאִיצִין. (C) לאחר מכן הפכנו כל אחת ממולקולות ה-mRNA הרבות שבדקנו בחזרה לדנ”א (לגֵנים) שמהם נוצרו בתחילה. חשבנו שבספריית הדנ”א הזאת יימצא מקְטע דנ”א או מספר מקטעי דנ”א המקודדים לחלבון המגיב לקפסאיצין. (D) הכנסנו את מקטעי הדנ”א לתאים שבדרך כלל אינם מגיבים לקפסאיצין. (E) התאים שהגיבו לקפסאיצין לאחר שהכנסנו אליהם את הדנ”א, היו אֵלו שהכילו את הגֵן קפסאיצין. לאחר בדיקות רבות, זיהינו גֵן יחיד המקוֹדֵד לקולטן הקפסאיצין. Capsaicin non-responsive cells = תאים שאינם מגיבים לקפסאיצין.
לשם כך, יצרנו ספרייה של מיליוני מקטעים של דנ”א התואמים לגֵנים שמתבטאים בתאֵי העָצָב התחושתיים שיכולים להגיב לכאב, לחוֹם ולמגע. כדי למצוא את הגֵן המסוים שחיפשנו, נאלצנו לסנן מאות אלפי חתיכות דנ”א שהופקו מ-mRNA שונים ורבים שאספנו מתאֵי העָצָב המגיבים לכאב. זה היה תהליך מפרך שבו נאלצנו לחלק בצורות מתוחכמות את המספר העצום של חלקי הדנ”א שיצרנו לקבוצות קטנות יותר ויותר, עד שלבסוף יכולנו לזהות את הגֵן המדויק שחיפשנו.
כדי לבדוק אם מצאנו את הגֵן הנכון, בודדנו את מקטעי הדנ”א המסוימים שחשבנו שמקוֹדדים לקולטן הכאב, והכנסנו אותם לתוך תאים שבמקור לא הגיבו לקפסאיצין (איור 2D). לאחר מכן, השתמשנו בשיטה שהומצאה על ידי זוכה פרס נובל המנוח, רוג’ר טְסְיֶין (Roger Tsien), כדי לבדוק אם הַתָאים הללו פיתחו רגישות לקפסאיצין. בעזרת שיטה זו יכולנו לראות הבזק אור שנפלט מהתאים בכל פעם שיונֵי סידן נכנסו לתא (איור 2E). בשלב הבא השתמשנו בטכניקת הרישום התוך-תאִי (Patch clamp) כדי לתעד את זרם החשמל על פני פיסות קטנות של קרום תא מהתאים הזוהרים הללו והראינו שהם הגיבו לקפסאיצין, בכך שאפשרו זרימת יונים לתוך התא. בינגו! הצלחנו במשימה!
התוצאות שלנו הצביעו על כך שיש קולטן לקפסאיצין, ושהקולטן הזה הוא למעשה תעלת יונים. קראנו לה קולטן TRPV1 (איור 3A), כיוון שהיא משתייכת לקבוצה של תעלות יונים הנקראות תעלות פוטנציאל הקולטן החולף (TRP). מאוחר יותר מצאנו שהקולטן הזה לא מגיב רק לקפסאיצין (איור 3B) אלא גם לחוֹם מזיק, ושהוא מופעל בטמפרטורות הגבוהות מ-43 מעלות צלזיוס (איור 3C) [4].
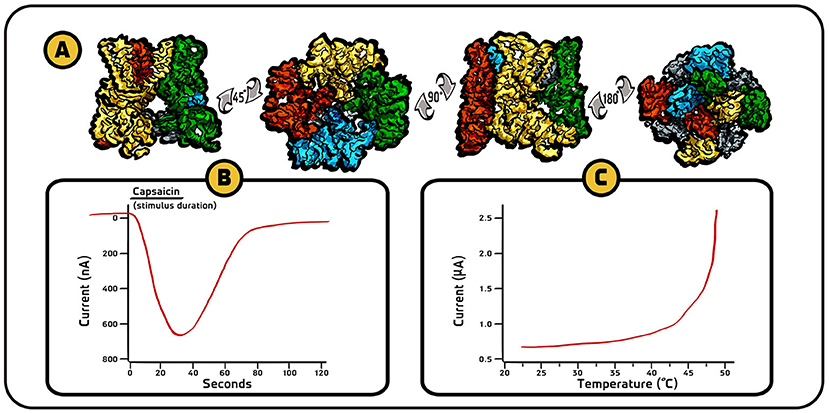
- איור 3 - קולטן TRPV1 – מבנה והתנהגות.
- (A) ארבע תצוגות שונות ברזולוציה גבוהה של תעלת הקולטן TRPV1 (שרטוטים תלת־ממדיים). התצוגות נוצרו על בסיס תמונות שהתקבלו ממיקרוסקופ אלקטרוני קריוגני (התמונות נלקחו מ-[5]). (B) בתגובה לקפסאיצין, קולטני TRPV1 מאפשרים ליונים של סידן (בעלי מטען חשמלי חיובי) להיכנס לתא. דבר זה בא לידי ביטוי בשינוי בזרם החשמלי. כאשר מטען חיובי זורם לתוך התא, נהוג לייצג את הזרם בגרף כמגמת ירידה (גרף נלקח מ-[4]). (C) בתגובה לטמפרטורות גבוהות, קולטני ה-TRPV1 מאפשרים ליונים של סידן ושל נתרן (מטען חיובי) לזרום לתוך התא. תוצאות אלו מצביעות על כך שאותם הקולטנים מגיבים גם לכימיקלים (קפסאיצין במקרה זה) וגם לטמפרטורות גבוהות שעלולות להזיק לגוף.
- Current = זרם;
- Capsaicin = קָפְּסָאִיצִין;
- Stimulus duration = משך הגירוי;
- Temperature = טמפרטורה;
- Seconds = שניוֹת.
לאחר שמצאנו את הקולטן TRPV1, היה לנו קל יותר לגַלוֹת קולטנים נוספים ממשפחת ה-TRP, כמו TRPM8 המגיב למנטול ולטמפרטורות קרות [6], ו-TRPA1 (הנקרא לפעמים קולטן הוואסאבי), המגיב לחומרים ”עוקצניים” כמו חרדל ושום, וכן לגירויים אחרים, כגון חומרים המיוצרים על ידי הגוף בזמן דלקת [7]. תעלות TRP נמצאות ברקמות חישתיות רבות, למשל בעיניים, בלשון ובעור. רבות מהן מעורבות באיתור אותות חיצוניים הקשורים לחושים שלנו, וחלקן מזַהוֹת אותות מתוך הגוף (כגון אותות המיוצרים על ידי איברים פנימיים). כיום אנו מבינים טוב יותר את המבנים ואת התפקודים שלהם, אך עדיין נשארו חידות שטרם פתרנו.
עתידו של מחקר הכאב
אחת החידות העיקריות שאנו עדיין מנסים לפתור היא כיצד חוֹם וקור מפעילים את קולטני ה-TRP. נכון לעכשיו איננו מבינים כיצד קולטני TRP ”חשים” טמפרטורה. אנו חושבים שבניגוד לכימיקלים כמו קפסאיצין, הטמפרטורה אינה משפיעה רק על חלק אחד מסוים של קולטן ה-TRP, אלא היא פועלת על מספר חלקים בו־זמנית. כדי לחקור זאת, אנו מנסים להקפיא ולצלם קולטנים (באמצעות מיקרוסקופ אלקטרונים קריוגני) כשהם מגיבים לטמפרטורות חמות או קרות, ולאחר מכן, אנו מנסים להבין איך הטמפרטורות הללו משפיעות על הקולטנים.
כדי לפתח תרופות טובות יותר לכאב חריף ולכאב מתמשך (כרוני), שבאמצעותן נוכל לנסות לטפל במשבר האופיואידים, אני מאמין שעלינו להבין את סוגי הכאב השונים, וכן את המולקולות, את סוגי הַתָאים ואת המסלולים העיקריים בכל סוג של כאב (למשל, אנו יודעים שהכאב המורגש בעור, הנקרא כאב עוֹרִי, שונה מאוד מתחושת הכאב הנוצרת באיברים הפנימיים, הנקראת כאב פנימי). לדעתי לא נוכל לפתור את כל סוגי הכאב השונים בעזרת גישה אחת, אז כנראה שנצטרך לפתח גישות ייחודיות לכל סוג של כאב. עלינו גם לפתח דרכים טובות יותר למדידת כאב, כיוון שכל אחד מרגיש כאב בצורה שונה. מדידות כאב מדויקות יאפשרו לנו להעריך בצורה טובה יותר את פעולתן של תרופות חדשות.
ברצוני להתעמק בהבנת המבנה האטומי של קולטני ה-TRP, ולהשתמש בידע הזה כדי להבין טוב יותר כיצד הם פועלים. ככל שנבין טוב יותר כיצד פועלים קולטני ה-TRP, נוכל לפתח תרופות חדשות המְכֻוָנוֹת רק לחלקים או למנגנונים ייחודיים של הקולטנים הללו. מְשַׁכְּכֵי כאבים רבים הנמצאים כיום בשימוש חוסמים את קולטני הכאב לחלוטין, וכתוצאה מכך משבשים את יכולתם של הקולטנים להזהיר אנשים מפני פגיעות. לדוגמה, חלק מהתרופות המכוונות לקולטן TRPV1 מצמצמות את יכולתם של אנשים לחוש בכאב כתגובה לחוֹם, וכך מטופלים עלולים להיכוות ללא ידיעתם כשהם נוגעים במשהו חם, או כשהם שותים נוזלים חמים [8].
האם אפשר לפתח תרופות שאינן ”מכבות” את קולטני ה-TRP, אלא משנות את האופן שבו הקולטנים מִתקשרים עם גירוי מסוים? במקרה של TRPV1 אנו מחפשים דרכים לחסום את יכולתם של חומרים הגורמים לדלקת להגביר את הרגישות של הקולטן, בלי לחסום את יכולתו לזַהוֹת חוֹם בתנאים רגילים. זוהי משימה מאתגרת, ויש עבודה רבה לפנינו – אך יש בה גם פוטנציאל אדיר לעזור לאנשים רבים הסובלים מכאבים כרוניים, ולכן מאמצינו אינם מושקעים לשווא.
המלצות למוחות צעירים
המדע במהותו זהֵה לסוגים אחרים של עשייה יצירתית – אתם חופשיים ללכת בעקבות הסקרנות שלכם, אך קשה מאוד לחזות מה יקרה לאורך הדרך. אתם יכולים לפלס את דרככם ולהפיק הנאה רבה מעבודתכם, אבל יש גם תקופות של תסכול וחרדה, שבהן אתם לא מבינים את התוצאות שלכם, או מה הדבר הבא שעליכם לעשות. אם תבחרו בקריירה מדעית, הדברים שצריכים להניע אתכם הם סקרנות ותשוקה. עליכם להיות אנשים שאוהבים להבין כיצד דברים עובדים, ועם מוטיבציה אמיתית לפתרון חידות. לעיתים קרובות תצטרכו פשוט להניח עקב בצד אגודל, להתרכז בדברים המתרחשים בטווח הקצר, ולהפיק הנאה מעבודה במעבדה ומעריכת הניסויים שלכם.
פעמים רבות אני אומר לתלמידיי שההתמדה משתלמת. עליכם למצוא דרך להמשיך להתקדם לעבר מטרה מדעית שבעיניכם היא מרגשת, מעניינת ומשמעותית. בקריירה שלי התמקדתי בשאלות גדולות שבמשך שנים רבות נותרו ללא מענה. ידעתי שיהיה מרגש מאוד לפתור אותן, ושהפתרונות שאני עשוי למצוא יוכלו לפתוח אפשרויות חדשות בתחום המחקר שלי. כשהדברים לא עבדו, ניסיתי להבין למה, וחיפשתי גישה חדשה. כל עוד הצלחתי לחשוב על דרך חדשה לגשת לבעיה, הרגשתי טעון באנרגיה הדרושה לחזור למעבדה ולהסתכל על הבעיה בצורה אחרת. הדרך הייתה מאתגרת, אבל ההתמדה שלי השתלמה.
לסיום, ברצוני להדגיש עוד היבט יוצא דופן ומרגש של המדע, והוא שהמדענים משתייכים לקהילה בין־לאומית (איור 4); אני מכיר אנשים מכל העולם, ומבקר אותם לעיתים קרובות. זהו דבר ייחודי שהרחיב את אופקיי והוסיף עניין רב לחיי.

- איור 4 - המדענים הם חלק מקהילה בין־לאומית.
- בהיותי מדען אני חלק מקהילה בין־לאומית ענֵפה. אחד היתרונות מבחינתי במקצוע זה הוא ההיכרות עם אנשים מכל העולם שמעשירה אותי ומוסיפה עניין רב לחיי.
מילון מונחים
חוש המישוש (Somatosensation): ↑ היכולת לחוש מגע, טמפרטורה וכאב, כמו גם את המיקום ואת התנועתיות של הגוף במרחב.
קולטנים (Receptors): ↑ יחידות חישה קטנות, בדרך כלל חלבונים בקרום התא, המגיבות לגירויים (כגון כימיקלים מסוימים או טמפרטורה).
קולטני תעלות יוֹנִים (Ion Channel Receptors): ↑ קולטנים היוצרים אותות חשמליים בתגובה לגירויים, בכך שהם מאפשרים ליונים (חלקיקים בעלי מטען חשמלי) לזרום לתוך תאי עצב ומחוצה להם.
כאב כְרוֹנִי (Chronic Pain): ↑ כאב שנמשך לפרקי זמן ארוכים (יותר מ-12 שבועות), גם לאחר שהגורם המקורי נעלם. דוגמאות: כאבי בטן כרוניים או כאבי מִפְרָקים כרוניים.
מְשַׁכְּכֵי כאבים (Analgesics): ↑ תרופות המיועדות להקל על כאבים.
כאב חריף (Acute Pain): ↑ כאב פתאומי שנמשך זמן קצר יחסית וחולף כאשר הגורם המקורי שלו נעלם (למשל, הכאב שחשים כשנפצעים באצבע).
נוֹצִיצֶפְּצִיָה (Nociception): ↑ תהליך במערכת החישה המאפשר לזהות גירויים מזיקים.
קָפְּסָאִיצִין (Capsaicin): ↑ החומר בפִּלפל החריף הגורם לתחושת הצריבה.
תודות
ברצוני להודות לנועה שגב על עריכת הריאיון שהיווה את הבסיס למאמר זה, ועל כתיבה משותפת של המאמר. תודה לאיריס גת עבור האיורים ול- Susan Debad על העריכה הלשונית של כתב-היד.
הצהרת ניגוד אינטרסים
המחברים מצהירים כל המחקר נערך בהעדר כי קשר מסחרי או פיננסי שיכול להתפרש כניגוד אינטרסים פוטנציאלי.
מקורות
[1] ↑ Benyamin, R., Trescot, A. M., Datta, S., Buenaventura, R. M., Adlaka, R., Sehgal, N., et al. 2008. Opioid complications and side effects. Pain Phys. 11:S105. doi: 10.36076/ppj.2008/11/S105
[2] ↑ Szolcsányi, J., and Jancso-Gabor, A. 1975. Sensory effects of capsaicin congeners I. Relationship between chemical structure and pain-producing potency of pungent agents. Arzneimittel Forschung. 25:1877–81.
[3] ↑ Wood, J. N., Winter, J., James, I. F., Rang, H., Yeats, J., and Bevan, S. 1988. Capsaicin-induced ion fluxes in dorsal root ganglion cells in culture. J. Neurosci. 8:3208–20. doi: 10.1523/JNEUROSCI.08-09-03208.1988
[4] ↑ Caterina, M. J., Schumacher, M. A., Tominaga, M., Rosen, T. A., Levine, J. D., and Julius, D. 1997. The capsaicin receptor: a heat-activated ion channel in the pain pathway. Nature. 389:816–24. doi: 10.1038/39807
[5] ↑ Liao, M., Cao, E., Julius, D., and Cheng, Y. 2013. Structure of the TRPV1 ion channel determined by electron cryo-microscopy. Nature. 504:107–12. doi: 10.1038/nature12822
[6] ↑ Bautista, D. M., Siemens, J., Glazer, J. M., Tsuruda, P. R., Basbaum, A. I., Stucky, C. L., et al. (2007). The menthol receptor TRPM8 is the principal detector of environmental cold. Nature. 448:204–8. doi: 10.1038/nature05910
[7] ↑ Bautista, D. M., Jordt, S. E., Nikai, T., Tsuruda, P. R., Read, A. J., Poblete, J., et al. 2006. TRPA1 mediates the inflammatory actions of environmental irritants and proalgesic agents. Cell. 124:1269–82. doi: 10.1016/j.cell.2006.02.023
[8] ↑ Moran, M. M., and Szallasi, A. 2018. Targeting nociceptive transient receptor potential channels to treat chronic pain: current state of the field. Br. J. Pharmacol. 175:2185–203. doi: 10.1111/bph.14044
