תַקצִיר
האם ידעתם כי ההחלטות שאתם מקבלים בחיי היומיום, כמו באיזו מידה אתם עוסקים בפעילות גופנית; מה אתם אוכלים; ואפילו הדרך שבה אתם חושבים, יכולות לשנות את היחידות הבסיסיות המצויות בתאֵי הגוף? במאמר זה, אספר לכם על אודות הטֵֶּלוֹמֵרִים. אלו הם הקצוות המגינים של מולקולות הדנ''א – המולקולות המאחסנות את הגֶּנים של כל אורגניזם. אציג בפניכם גם אֶנְזים שגילינו, בשם טֶלוֹמֵרָאז, האחראי על הוספַת הטלומרים ועל תחזוקתם. לאחר שנצלול לפרטים המולקולריים של הטלומרים ושל הטלומראזים, אחשוף בפניכם כמה קשרים מעניינים מאוד בין הטלומרים לבריאות האדם. אני מקווה כי עד לסיום קריאת המאמר, גם אתם תתרשמו כי הדרך שבה הגורמים הפסיכולוגיים, הסביבתיים והחברתיים יכולים להשפיע על יסודות הביולוגיה שלנו – היא ללא ספֵק מדהימה.
הפרופסורית אליזבת בְּלַקְבְּרְן זכתה בפרס נובל לפיזיולוגיה או לרפואה לשנת 2009, במשותף עם הפרופסורית קָרוֹל גְרָיידֶר והפרופסור ג'ק שוֹסְטָק, עבור הגילוי כיצד הטלומרים מגינים על הכרומוזומים, ועל גילוי האנזים טלומראז.
הקצוות המגינים של הדנ''א
החיים, על מורכבותם הרבָּה, הם חידה עצומה. אנשים סקרנים, כמוכם וכמוני, נוטים לשאול שאלות כמו 'מה זה?' 'מה מתרחש כאן?', ו'מדוע זה קורה כך?'. בחרתי לתעֵל את הסקרנות הבלתי נדלית הזו למחקר בתחום הביולוגיה – מדעי החיים. היות שביולוגיה היא דבר כה מורכב, עליכם לשאול את עצמכם תמיד: מָהֵם הדברים שבאפשרותי להבין, ובמה עליי למקֵּד את המחקר שלי? אחרת, כל פרטֵי התופעות הביולוגיות שאתם חוקרים עלולים להציף אתכם ברגע. אחד מנתיבי המחקר שאתם עשויים לבחור בתחום הביולוגיה מכונה ביולוגיה מולקולרית. במסגרת תחום זה אנו בוחנים תהליכים ביולוגיים באמצעות מחקר המולקולות השונות ויחסי הגומלין ביניהן. עבורי, הביולוגיה המולקולרית היא תחום מדעי מספֵּק מאוד, כיוון שבמובנים רבים היא מאפשרת לנו לענות על שאלות פרטניות ובסיסיות הנוגעות לתעלומות החיים. במאמר זה אספר לכם לגבי התגליות שאליהן הגענו באמצעות הביולוגיה המולקולרית. על אודות מנגנון ההגנה החשוב המצוי בקצוות מולקולות הדנ''א – המולקולות המכילות את ההוראות הגֶּנטיוֹת (הקוד) המועברות מהורים לילדיהם. אך ראשית, עלֵינו להניח את היסודות שלנו.
דנ''א, כרומוזומים ושִׁכפוּל
כל תא חי מכיל מִבנים בשם כְרוֹמוֹזוֹמִים. כל כרומוזום מכיל פּוֹלימֶר (מולקולה גדולה מאוד) בשם חומצה דֶאוֹקְסִירִיבּוֹנוּקְלֵאִית, או בקיצור, דנ''א. יחד, כל הדנ''א הוא כמו ספרייה של הוראות המנחה את התא עצמו, וכל אורגניזם הבנוי מִתָּאים כאלו, איך לתפקד. מולקולת הדנ''א היא בצורת סליל כפול המורכב משני גְּדִילִים לִינֵאָרִיּים (קָוִויּים). הגדילים הללו מקבילים זה לזה ומסתלסלים זה סביב זה, כך שהם יוצרים את מבנה הסליל הכפול (איור 1). בכרומוזומים, הדנ''א מגולגל ודחוס בצפיפות בתוך התאים (איור 1). בתאים של בני אדם, לדוגמה, ישנם 23 זוגות של כרומוזומים המכילים את כל הדנ''א שלנו. הכרומוזומים הללו ממוקמים בגרעין התא ומכונים כרומוזומים ליניאריים, כיוון שלכל אחד מהם יש שני קצוות. זה נכון עבור כל התאים האֵיקַרְיוֹטִיּים, שהם תאים בעלי גרעין. אורגניזמים בעלי תאים המכילים גרעין כוללים את כל החיות, הצמחים והפטריות, וכן את רוב האצות. מנגד, אורגניזמים שבתאיהם אין גרעין מכונים פְּרוֹקַרְיוֹטִיּים (חיידקים למשל), ולהם כרומוזומים עגולים ללא קצוות (צורה דמוית מעגל).
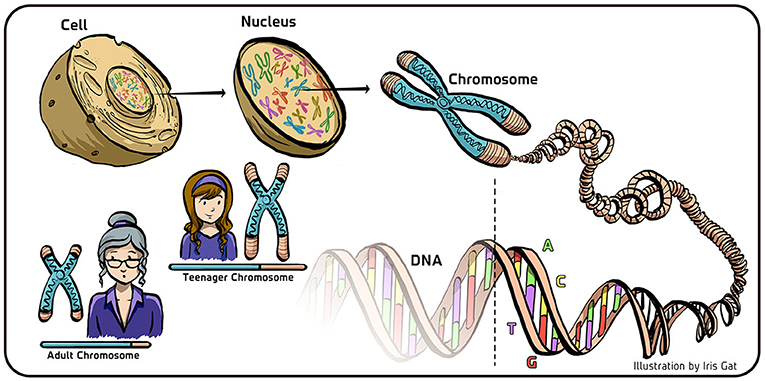
- איור 1 - דנ''א וכרומוזומים בתאים אֵיקַרְיוֹטיים.
- באיקריוטים, הדנ''א (DNA) מאוחסן בגרעין התא (Nucleus), שבו הוא מגולגל ודחוס במבנים המכונים כרומוזומים (Chromosomes). הדנ''א מופיע בצורת סליל כפול המורכב מארבעה בסיסים (G, T, A ו-C). באיור, הם מסומנים בארבעה צבעים המרכיבים את הדנ''א. כאשר התאים (Cells) משתכפלים מתרחשת העתקה של הדנ''א, שבה נוצרים שני סלילים כפולים חדשים מהסליל הכפול המקורי. המנגנון המולקולרי שמעתיק את הדנ''א אינו מעתיק את רֶצֶף הדנ''א בקצה הכרומוזום (החלק השקוף של הדנ''א שמופיע בתחתית האיור). כתוצאה מכך, הדנ''א מתקצר ככל שאנו מתבגרים (רְאו החלק השמאלי בתחתית האיור). כדי להבטיח תורשה יציבה של החומר הגנטי יש צורך במנגנון מיוחד להגנה על קצוות רצף הדנ''א במהלך השכפול. מקרא: Teenager Chromosome = כרומוזום של בן/בת נוער Adult Chromosome = כרומוזום של אדם מבוגר.
כשהתאים מתחלקים עליהם לשכפל את הדנ''א שבתוכם, כדי שגם התאים החדשים יכילו את כל ההוראות הנחוצות המאוחסנות בדנ''א. כפי שאתם אולי כבר יודעים, פולימר הדנ''א הוא חוט המורכב מארבעה סוגי כימיקלים המהווים את אבני הבניין שלו. הם מכונים בסיסים, ומסומנים בארבע אותיות – G, T, A ו-C שמייצגות את ארבעת הכימיקלים (A – אָדֵנִין; T – תִימִין; G – גוּאָנִין ו-C – צִיטוֹזִין). רֶצֶף הבסיסים הללו לאורך פולימר הדנ''א יוצר את הקוד המשמש כ'הוראות ההפעלה' של התא. בשני הגדילים המרכיבים את הסליל הכפול, הבסיסים הללו תמיד מופיעים בזוגות: A-T ו-C-G, כך שמול כל בסיס A בגדיל אחד של הסליל הכפול ניצב בסיס T בסליל האחר, מול בסיס G ניצב בסיס C, ולהפך (איור 1).
כאשר תהליך השכפול מתרחש בגרעין התא, המנגנונים המולקולריים המורכבים מפרידים תחילה את הסליל הכפול לשני גדילי דנ''א נפרדים. אז, כל סליל מקורי משמש כתבנית לסִינְתֶּזָה (מיזוג) עם הַגדיל המתאים לו. בתהליך זה, לכל בסיס בכל גדיל (שבשלב זה הוא כבר נפרד), 'משודך' הבסיס המתאים לו בזוג (A משלים את T, ו-T את C. A משלים את G, ו-G את C), עד שנוצר סליל חדש ומשלים עבור כל אחד מגדילי הדנ''א המקורי. בסיום התהליך מתקבלים שני סלילים כפולים חדשים, זהים לדנ''א המקורי.
עד כאן, הכול מובן – יש לנו סליל דנ''א כפול חדש, מוכן לשימוש בתא האיקריוטי החדש שנוצר לאחר חלוקת התא. אולם מסתבר כי המנגנון המורכב הזה לא יכול להעתיק את גדילי הדנ''א ממש עד קצותיהם (איור 1). לכן בתהליך חלוקת התא לא מתרחשת העתקה של רצף זוגות הבסיסים המצויים בסוף כל גדיל דנ''א. כלומר, בעקבות כל שכפול הדנ''א המקורי מתקצר עוד ועוד.
כאן ודאי תתעורר במוחותיכם הסקרנים השאלה – ובכן, מדוע זה קורה? למה הדנ''א לא משתכפל במלואו במהלך חלוקת התא? למען האמת, איננו יודעים ממש. זו אחת מאותן דוגמאות שבהן הביולוגים מרגישים כמו ארכיאולוגים – מנסים לפענח את התפתחות האירועים ההיסטוריים באמצעות פיסות מידע מהפריטים ששרדו עד ימינו אלה. אנו יודעים רק שלא מתרחשת העתקה מלאה של הדנ''א במהלך חלוקת התאים. אנו גם מסיקים כי התאים הראשונים באבוֹלוּציית החיים היו תאים פרוקריוטים (ולא איקריוטים), כלומר בעלי כרומוזומים מעגליים, כך שלדנ''א לא היו קצוות חופשיים, וכי התאים האיקריוטים בעלי הדנ''א הליניארי – ומכאן גם קצוות הדנ''א – התפתחו בשלב מאוחר יותר של האבוֹלוּציה.
קו המחשבה הזה הביא אותנו לְשַׁעֵר כי מנגנון שכפול הדנ''א הפועל באיקריוטים התפתח במקור בפרוקריוטים. שָׁם הוא פעל בצורה מספיק טובה, ולא נאלץ להתמודד עם קצוות הדנ''א, כיוון שלדנ''א מעגלי אין קצוות! האם המשמעות היא כי במקרה של כרומוזומים ליניאריים בתאים איקריוטיים, בכל פעם שהתא משכפל את הדנ''א שלו חלק מהחומר הגנטי החשוב שנושא את הקוד ומצוי בדנ''א אובד? למרבה המזל, זה לא מה שקורה, הודות למנגנון הגנה המוודא כי לא יאבד אף חלק מהדנ''א, שחשוב לתפקודו הַתַּקין בתאים האיקריוטיים.
הטֶּלוֹמֵרִים – מגיני הדנ''א
כפי שראינו בחלק הקודם של המאמר (איור 1), באיקריוטים, שכפול הדנ''א אינו מגיע עד לקצות גדילי הדנ''א. אם היו שואלים אתכם איך להגן על החומר החשוב המקודד במִּקטע הסופי של הדנ''א, האם יכולתם לחשוב על פתרון לחידה הזו? מסתבר כי בסופם של כרומוזומים ליניאריים ישנם רצפי דנ''א מיוחדים בשם טֶלוֹמֵרִים (ביוונית, משמעות המילה 'טֶלוֹ' היא סוף, ומשמעות המילה 'מֵר' – חֵלֶק). הדנ''א בטלומרים נקרא 'דנ''א לא מקוֹדֵד', ותפקידו להבטיח כי החלק המקוֹדֵד של הדנ''א (הכולל את ההוראות שההורים מעבירים לצאצאיהם), יועבר באופן תקין לדור הבא.
תוכלו לחשוב על הטלומרים כעל קצוות הפלסטיק המגוננים שבסוף שרוכי הנעליים. בפֹעַל, הטלומרים מפצים על כך שלא מתרחשת העתקה של הדנ''א שבקצות הכרומוזומים. לְמה הכּוונה? כדי להימנע ממקרים שבהם חלקים חשובים (מקוֹדְדים) בקצות הדנ''א לא יועתקו במהלך חלוקת התא, כשישנם טלומרים ממש בקצות הכרומוזומים, רק הם החלקים שלא מועתקים עד סופם, וכך חלקים בעלי חשיבוּת (מקודדים) של חומר הדנ''א אינם הולכים לאיבוד. אם נְדַמֶּה זאת לשרוכי נעליים – כשמשתמשים בשרוכים לאורך זמן, קצוות הפלסטיק שלהם הולכים וּמִתְבַּלִּים, אך השרוכים עצמם נשארים מוגנים. גילינו דבר אפילו יותר מלהיב – כאשר הטלומר מתקצר, ישנוֹ אֶנְזִים מיוחד שנמשך אליו, שביכולתו להוסיף עוד דנ''א טלומרי לכרומוזום. כך, הטלומר יכול להתחדש. זהו פתרון יפהפה שהטבע מצא לבעיית אי השלמַת שכפול הדנ''א בקצות הכרומוזומים הליניאריים.
ב-1930, הגנטיקאים האמריקאיים הרמן מוּלר [1] וברברה מקלינטוֹק [2] זיהו את הטלומרים כ'משהו' מיוחד בסוף הכרומוזומים, שהגן על קצותיהם. בהמשך, עם התפתחות הביולוגיה המולקולרית, היה ניתן לאפיין את טבעם המולקולרי של הטלומרים. ב-1978, הביולוג האמריקאי ג'וזף גוֹל ואני זיהינו את מבנה הטלומרים בקצות הכרומוזומים הליניאריים באורגניזם מעניין בשם Tetrahymena thermophila (להלן: טֶטְרָהִימֵנָה, בתעתיק לעברית), הנפוץ ביְרֹקֶת המצויה על פני השטח של מאגרי מים [3]. מצאנו כי הטלומרים של האורגניזם הזה מורכבים מדפוס מסוים של בסיסי דנ''א – הרצף TTGGGG (2 איור), שֶׁחזר על עצמו מספר שונה של פעמים (בין 50-20) בכרומוזומים שונים בתוך אוכלוסיית התאים. זמן לא רב לאחר מכן התגלו דפוסים חזרתיים דומים בטלומרים של אורגניזמים אחרים, כמו אוֹקְסִיטְרִיכָה רִיסָנִית (ciliate Oxytricha) – TTTTGGGG, וברִירָנִית – TTAGGG [4]. טלומרים אנושיים מכילים את הרצף TTAGGG, שחוזר על עצמו אלפי פעמים בסופֵי כל הכרומוזומים שלנו [4].
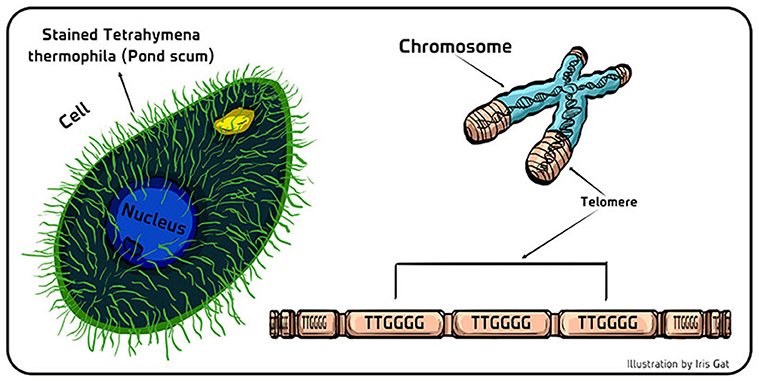
- איור 2 - טלומרים המצויים בירוקת מאגרי מים.
- צד שמאל: איור של האורגניזם האיקריוטי החד-תאי טֶטְרָהִימֵנָה, החי במים מתוקים. מאות האברונים דמויי השערות (רִיסוֹנִים) על פני השטח של התא (Cell) פועלים כמְשׁוֹטִים זעירים המאפשרים לאורגניזם לנוע במים, לצוד מזון או להזדווג. צד ימין: טלומרים הם כמו קצוות הפלסטיק המגינים בשרוכי הנעליים. הם שומרים על החומר הגנטי המאוחסן בחלק המקודד של הדנ''א (חלק הכרומוזום הצבוע בכחול). החלק הטלומרי (לא מקוֹדד) של הדנ''א (חלק הכרומוזום הצבוע בחוּם) מורכב מיחידות חוזרות של בסיסים (TTGGGG בטטרהימנה; TTAGGG בָּנוּ, בני האדם). Stained = צבוע Nucleus = גרעין.
בנקודה זו, יכולות לעלות הרבה שאלות מעניינות על אודות הטלומרים והדפוסים החוזרים שלהם. הייתי רוצה להתמקד כעת בשאלה זו: כיצד הטלומרים מתווספים לקצוות הכרומוזומים? האם מנגנון זה מספֵּק הגנה במצבים אחרים, נוסף על חלוקת התא? בהמשך המאמר נתבונן במנגנון המופלא שבונה את הטלומרים, ונראה מה הם יכולים ללמד אותנו על אודות בריאות בני האדם ולגבי רווחתנו.
מאריכים את חיי הטֶּטְרָהִימֵנָה – גילוי הטֶּלוֹמֵרָאז
כשחקרתי את הטטרהימנה ואת הזנים הקשורים לה, בשנות ה-80 המוקדמות של המאה הקודמת, היה ידוע כי במהלך מחזוֹר חיי הטטרהימנה, יש שלב שבו הכרומוזומים המקוריים נחתכים לכרומוזומים ליניאריים קטנים, המכונים מִינִי-כרומוזומים. גם הם, כמו הכרומוזומים השלמים שעליהם דיברנו קודם לכן, מסתיימים בחזרות של דפוס רצפי הדנ''א הטלומרי – TTGGGG. כשגילינו את המבנה של חזרות הדנ''א האלה בתאי ירוקת במאגרי מים, ניסינו לבדוק אם הוא תואם את היֶּדע שהיה בידינו באותה תקופה בנוגע להתווספות בסיסי דנ''א לכרומוזומים. המנגנונים היחידים בתחום שהיו מוכרים לנו באותו זמן היו (i) שכפול דנ''א, ו(ii) שִחְלוּף דנ''א. לכל אחד מהמנגנונים הללו היו מערכי חוקים מסוימים מאוד לתוספת דנ''א. הופעַת רצפי הטלומרים החזרתיים שגילינו (למשל, לאור העובדה שהטלומרים של הירוקת המצויה במאגרי מים לא היו אחידים באורכם – לפעמים הכילו מספר מועט של חזרות; לעיתים מספר רב; ולפעמים כל הטלומרים התארכו בבת אחת) סתרה את היֶּדע הקודם שהיה ברשותנו על אודות מערכי החוקים הללו. הופתענו לגלות את ההתנהגויות האלה כיוון שהממצאים החדשים שלנו לגבי מבנה הטלומרים לא תאמו את העקרונות והיֶּדע המבוססים היחידים שהיו לנו בזמנו על אודות דנ''א.
כשניצבים בפני צמתים יוצאי דופן שכאלה במדע, צריך לחשוב 'מחוץ לקופסה' ולשקול אפשרויות יצירתיוֹת אחרות כדי למצוא את התשובה שמחפשים. במקרה הזה, ניסיתי לשעֵר איזה מנגנון יכול להיות אחראי לתוספת רצפי הטלומרים החזרתיים למִינִי-כרומוזומים לאחר שהם נפרדים מהכרומוזומים הארוכים. אחת האפשרויות הייתה פעילות של אנזים. כדי לבדוק את ההשערה הזו, שׂמתי במבחנת המחקר תמצית של תאי ירוקת המצויה במאגרי מים, והוספתי כימיקלים שונים כדי לראות אם אחד מהם גָּרַם להוספה של טלומרים למיני-כרומוזומים. לאחר תהליך של ניסוי וטעייה, גיליתי כי אחת התוספות אכן האיצה סינתזה של רצפי טלומרים חזרתיים.
בשלב הזה, קָרוֹל גְרָיידֶר, כיום פרופסורית, הצטרפה למעבדה שלי במסגרת לימודי הדוקטורט שלה. האתגר שניצב בפניה היה לפשֵּׁט את התגובה במבחנת המחקר, כדי שנוכל לגלות את פעילות האנזים המסוימת האחראית לתוספת הטלומרים בקצוות. לאחר ניסוי וטעייה נוספים קרול צמצמה ופישטה את הבדיקה עד כמה שניתן. הוספנו רצפים חזרתיים של TTGGGG שיצרנו במעבדה, מייד לאחר שהכרומוזומים נחתכו למיני-כרומוזומים. בשלב זה ציפינו שהטלומרים יתווספו. הוספנו את אבני הבניין של הדנ''א למבחנה (שתי מולקולות בשם dGTP ו-TTP), עם מעט מגנזיום גופרתי. ראינו כי רצפי החזרות של ה- TTGGGG אכן נוספו לקצוות הדנ''א שיצרנו במעבדה [5]. משמעות הדבר הייתה שמצאנו מנגנון אפשרי להארכַת טלומרים! עמיתתה של קרול, תלמידת התואר השני Claire Wyman, המציאה שֵׁם לאנזים החדש, שנראה כאחראי לתוספת רצפי הטלומרים החזרתיים: טֶלוֹמֵרָאז [6].
כדי לְתַקֵּף את השׁערתנו בנוגע לתפקידו של הטלומראז בהארכַת הדנ''א בתאים חיים (ולא רק במבחנת מחקר), ביצענו כמה ניסויים נוספים. לא אכנס כאן לפרטים, אך גילינו כי לאנזים הטלומראז יש חלק של רנ''א, המכיל רצף קצר המשלים את רצף הדנ''א של הטלומרים. הרנ''א הזה פועל כתבנית לרצף הטלומרי המשלים המתווסף לכרומוזום. בכמה מהניסויים הללו שינינו (במילים אחרות, הִנדסנו) את מבנה הטלומראז כדי לבחון אם השינויים השפיעו על יכולתו לסנתֵּז את רצף הדנ''א הטלומרי, ולהאריך את הטלומרים. היו גרסאות מהונדסות שאפשרו לטלומראז להמשיך לפעול, אך הכילו שינוי בתבנית הרנ''א שאחראית על הוספַת רצפי הדנ''א הטלומרי. בגרסאות הללו מצאנו כי בתאי הירוקת המצויה במאגרי מים היו חזרות חלופיות של רצפי הטלומרים – שונות מהרצף החוזר המקורי, TTGGGG, ומשלימות לשינוי הבסיסים ששׂמנו בתבנית [7].
חשוב לציין שכאשר הִנדסנו את הטלומראז כך שלא יְתפקד כלל, הטלומרים של תאי ירוקת מאגרי מים המשיכו להתקצר עוד ועוד עם כל חלוקה של התא, ולבסוף, לאחר 25-20 חלוקות, התא הפסיק להתחלק ומת [7] (איור 3, צד שמאל). כלומר, כאשר פעולת הטלומראז ניזוקה, תאי הירוקת המצויה במאגרי מים, שבאופן רגיל לא מתים (לכאורה אלה תאים שמתחלקים לָנֶצַח), הפכו לבני תמותה (כלומר, הפסיקו להתחלק אחרי מספר מסוים של חלוקות). כל הממצאים הללו הובילו למסקנה שלפיה הטלומראז אכן אחראי להוספַת הדנ''א הטלומרי לקצוות הכרומוזומים הליניאריים. זו הייתה התגלית שזיכתה את קרול ואותי בפרס נובל לפיזיולוגיה או לרפואה לשנת 2009 (במשותף עם עמית נוסף, פרופ' ג'ק שוֹסְטָק, שעִמו חקרתי את תפקודֵי הטלומרים בתאים של שֶמֶר האפייה). חשוב לציין שבהמשך, לאחר גילוי הטלומראז, התגלה כי פעילותו חשובה במקרים נוספים פרט לחלוקת תאים. הסתבר שדנ''א טלומרי רגיש מבחינה כימית לנזק גם בתוך תאים, ולכן מצריך תיקון במצבים שונים – במיוחד לאורך תקופות ארוכות, כמו במהלך חיי בני האדם. מסיבה זו, הטלומראז חשוב גם בתאים שלא מתחלקים (איור 3, צד ימין).
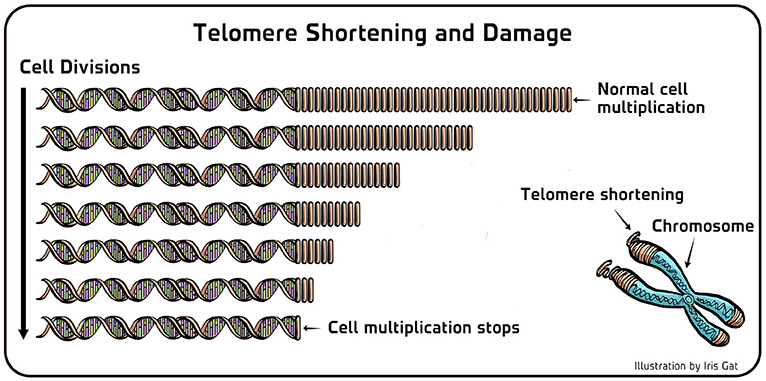
- איור 3 - התקצרות טלומרים ונזק שנגרם להם.
- צד שמאל: כאשר מתקיימת פעילות בלתי תקינה של הטלומראז בתאי ירוקת המצויה במאגרי מים, הדנ''א הטלומרי (המוצג כחלק הימני החוזר באיור זה), מתקצר עוד ועוד עם כל חלוקה של התא. כאשר הטלומרים נהיים קצרים מדי, התא מפסיק להתחלק. הדבר נכון גם עבור תאים אנושיים. צד ימין: הקצוות המורכבים מטלומרים רגישים מבחינה כימית לנזק בתוך התאים. לכן, פעילות הטלומראז חשובה גם לתחזוקת הטלומרים בתאים שאינם מתחלקים. מקרא: Cell divisions = חלוקת תאים Normal cell multiplication = שכפול תאים רגיל Telomere shortening = התקצרות טלומר Cell multiplication stops = שכפול התא מפסיק.
כעת, משהתוודעתם לעבודתי בתחום הטלומרים והטלומראז, אני רוצה להציג בפניכם נתיב מחקר נוסף שהתפתח בשלב מאוחר יותר של הקריירה המדעית שלי. נתיב מחקר זה הצביע על הַקֶּשר שבין הטלומרים לבריאות האדם, בכמה דרכים מפתיעות מאוד.
שיעורים מהטלומרים – דרכים לשיפור בריאות האדם
כשחקרתי את תחזוקת הטלומרים ואת הטלומראז בתאים אנושיים באוניברסיטת קליפורניה, סן פרנסיסקו (UCSF), פנתה אליי חוקרת צעירה ומבריקה בתחום הפסיכולוגיה בשם אֵלִיסָה אֵפֶּל. אליסה, כיום פרופסורית במחלקה לפסיכיאטריה באוניברסיטת קליפורניה, סן פרנסיסקו, חקרה אז במסגרת לימודי הפוסט-דוקטורט שלה לחץ נפשי מתמשך חמוּר. באותו זמן, בתחילת שנות ה-2000, היה ידוע כי אנשים הסובלים מלחץ נפשי מתמשך חמור לעיתים קרובות מראים שינויים גופניים המְּחקים תהליכים המאפיינים הזדקנות טבעית של בני אדם, אך בקצב מהיר יותר. במילים אחרות, ראינו קשר בין לחץ נפשי מתמשך להזדקנות מואצת בקרב בני אדם. מנקודת מבט אחרת, כשחקרנו את הטלומרים הבנו כי אם משנים גנטית את הטלומראז של תאי ירוקת במאגרי מים, או של תאי השֶּׁמֶר, כך שיפסיק לפעול, הטלומרים ימשיכו להתקצר עם כל חלוקה. זאת עד שלבסוף הם יהיו קצרים מדי וישלחו אותות לתא להפסיק להתחלק (איור 3). תגלית זו הובילה לרעיון חדש שהֵחֵל לצבור תשומת לב ותמיכה בתחום: ייתכן כי התקצרות הטלומרים קשורה להזדקנות של יונקים כמונו. בזמנו, לא היה ברור מה מתרחש בתאי הגוף האנושי במהלך ההזדקנות.
כשאליסה פנתה אליי ושאלה אם ייתכן שישנוֹ קשר בין לחץ נפשי מתמשך להתקצרות הטלומרים, חשבתי שזו שאלה מעניינת מאוד. היא סיפרה לי על אודות מחקר מרתק שהיא עורכת באימהות לילדים המתמודדים עם בעיות התפתחותיות או עם מחלות כרוניות. קבוצת האימהות הזו הייתה נתונה תחת לחץ נפשי מתמשך חמור, בין השאר משום שלעיתים קרובות לא ניתנת תמיכה במצבים כאלו בארה''ב (שבּה חיו האימהות וילדיהן, ושבּה נערך המחקר). נוסף על העניין המדעי שניצת בי כששמעתי על המחקר של אליסה, וכשתהיתי לגבי הַקֶּשֶׁר שעשוי להתקיים בין ממצאי מחקרה להתקצרות הטלומרים, הייתה לי סיבה נוספת, אישית יותר, לעסוק במחקר הזה. בתקופה ההיא בני עוד היה קטן, ומצאתי שאני דואגת לו לעיתים קרובות למדי. זה גרם לי להרגיש אֶמפתיה רבּה כלפי הנשים מהמחקר של אליסה, במיוחד כשהבנתי כמה לחץ נפשי הן עלולות לחוות בתור מטפלות במצבים המאתגרים הללו.
החלטנו להתחיל במחקר ניסיוני, שבו הקבוצה שלי מדדה את פעילות הטלומראז, וקבוצה אחרת מדדה את אורך הטלומרים בתאים של אימהות שהיו המטפלות העיקריות בילדיהן המתמודדים עם מחלות כרוניות. השווינו את הממצאים לאלו של ההורים בקבוצת הביקורת. הורים בקבוצת הביקורת תאמו מכל בחינה להורים בקבוצה הנחקרת, פרט לעובדה שלהורים בקבוצת הביקורת לא היו ילדים המתמודדים עם מחלות כרוניות. את עבודתנו הובילה פוסט-דוקטורנטית בשם Jue Lin.Jue היא חוקרת שעסקה בעבר בטלומרים של שְׁמָרים ובטלומראז, ומצאה עניין בנתיב המחקר החדש הזה. מייד, כבר במחקר הראשון, קיבלנו תוצאה מפתיעה – הייתה קורלציה כמותית משמעותית בין אורך הטלומר – במקרה זה, בין אורכו הקצר של הטלומר – לנוכחות הטיפול, ולתחושת ההורה המטפל שלפיה הטיפול גורם להם ללחץ נפשי (איור 4)! התוצאה המדהימה הזו הייתה האינדיקציה הראשונה לכך שעשויה להיות התאמה בין מצב פסיכולוגי, כמו לחץ נפשי מתמשך, לשינוי גופני מובהק מאוד ברמה המולקולרית הבסיסית ביותר!
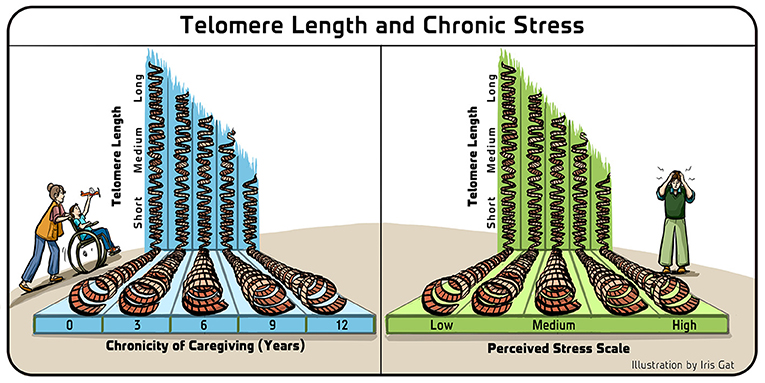
- איור 4 - אורך הטלומרים (Telomere length) ולחץ מתמשך (Chronic stress).
- במחקר שביצענו לראשונה בהשתתפות אימהות שהיו המטפלות הראשיות בילדיהן המתמודדים עם מחלות כרוניות, מצאנו שהייתה קורלציה סטטיסטית מובהקת בין הטלומרים הקצרים שנמצאו אצל האימהות למספר השנים שהיו במצב זה (צד שמאל של האיור), וכן לרמות הלחץ הנפשי שהן דיווחו שחוו (צד ימין של האיור). נלקח מ-[8] Epel et al.. מקרא: Telomere Length = אורך הטלומר Short = קצר Medium = בינוני Long = ארוך Chronicity of Caregiving (Years) = מֶשֶׁךְ הטיפול (שנים) Perceived Stress Scale = מידת הלחץ הנחווית Low = נמוך Medium = בינוני High = גבוה.
כמדענים, איננו נחפזים למסקנות, כיוון שאנו מודעים לנטייה האנושית לכפות על המציאוּת ועל הנתונים שלנו את מה שאנו רוצים לראות או למצוא. המשמעות היא שעָלֵינו להיות חשדנים במיוחד כשהתוצאות ההתחלתיות שאנו מקבלים תואמות את ההשׁערות ה'רצויות' לנו. מסיבה זו, החלטנו לנקוט בפעולות נוספות כדי לאמֵּת את התוצאות הראשוניות שלנו. אחת הדרכים הייתה לבחון קבוצות שונות של אנשים, החווים סוגים דומים של לחץ פסיכולוגי מתמשך הקשור בטיפול באחרים (למשל, טיפול בבן משפחה הלוקה בדֶמֶנְצְיָה). ביקשנו לבדוק אם ההשפעות על אורך הטלומרים שלהם יהיו זהות. במחקר נוסף שערכנו בדקנו קשרים אפשריים בין אורך הטלומרים למשתנים אחרים כמו גורמים סביבתיים, חינוכיים, וגורמים נוספים – נפשיים או פסיכולוגיים. מצאנו קשרים רבים כאלו. הקבוצה שלי וחוקרים אחרים הגיעו לבסוף למסקנה כי ישנם קשרים משמעותיים ביותר בין אורך הטלומרים לבריאות האדם [9].
ב-2017, אליסה ואני כתבנו יחד ספר לקהל הרחב, המציג את ליבַּת עבודתנו המתמשכת בנושא טלומרים ובריאות האדם, בשֵׁם'The Telomere Effect: A Revolutionary Approach to Living Younger, Healthier, Longer'(' אפקט הטלומרים: גישה מהפכנית לחיים צעירים, בריאים וארוכים יותר') [10] (רְאו בחלק המאמר שכותרתו 'חומרים נוספים'). על אף שהמוציאים לאור שלנו הם אלו שהתעקשו שנוסיף את המילה 'מהפכנית' לשמו של הספר, הספר אכן מקבֵּץ ומציג מִגוון עובדות ומסקנות מעניינות. אני רוצה לחלוֹק עימכם שתי נקודות חשובות. ראשית, אֹרַח החיים והַגישׁה שלנו אליהם – עושים את ההבדל! הכּוונה היא לכך שהבחירות שלנו בנוגע לשינה, למזון ולפעילות גופנית קבועה משפיעות על אורך הטלומרים שלנו. לכן, הפעולות הללו יכולות לתרום לבריאותנו בטווח הארוך, או לחלופין לפגוע בה, כמו גם להשליך על תוחלת החיים שלנו. הדבר נכון גם לגבי הֶרגלים של חשיבה שלילית, הקשורים להתקצרות הטלומרים. בניגוד לכך, חשיבה חיובית וחוסן נפשי תורמים לתחזוקה הטובה של הטלומרים שלנו. שנית, ברצוני להדגיש את נקודת המבט החברתית הרחבה יותר של אורך הטלומרים. הטלומרים מושפעים מהסביבה שלנו! המשמעות היא שכשאנו תומכים זה בזה, הן ברמת הפרט הן ברמת החֶברה, אנו תורמים לתחזוקה טובה של הטלומרים ושל בריאות האדם באופן כללי. אם כך, עָלֵינו לזכור שיש לנו תפקיד חשוב בשמירה על אורכם ועל בריאותם של הטלומרים שלנו ושל שאר בני האדם. ישנהּ השפעה לבחירות שאנו עושים על בסיס יומיומי, כמו גם להשלכות החברתיות שעָלֵינו לשאוף לשפר תמיד, כיוון שהן משתקפות אפילו בביולוגיה המולקולרית הבסיסית ביותר של תאי הגוף.
המלצות למוחות צעירים
מָהֵן הדרכים המיטביות לעסוק במדע, ואיך תהיו מדענים ומדעניות טובים? יש לי כמה עצות לתת לכם (איור 5). בתור התחלה, ברצוני להדגיש את חשיבותה של ההתמדה. אם אתם מתעניינים במדע עליכם לדעת שתצטרכו להתְמיד, כיוון שלפעמים התחום הזה עלול להיראות די מורכב וּמְאיים. אף על פי כן, אל תוותרו! אז, בנקודה מסוימת, תְּגַלּוּ שיגיע זמן נפלא שבו תְּפַצְּחוּ את האתגר. כשתגיעו לשָׁם תחוו סיפוק גדול, ותדעו שההתמדה שלכם השתלמה. כמו כן, כדי להיות מרוצים לאורך זמן, עליכם להיות משוכנעים שאתם עושים משהו חשוב ובעל עֵרֶךְ. כשאתם בוחרים את הנתיב הייעודי לכל אחת ואחד מכם במדע (או בכל מקצוע אחר), וַדְּאוּ שאתם עוסקים בדברים שאתם מאמינים שכדאי לעסוק בהם. כך, תחושת הָעֵרֶךְ שאתם מַקְנִים לעבודתכם תעודד אתכם להתמיד, אפילו בזמנים שבהם ייראה לכם שֶׁקַּל יותר לוותר. בבחירת דרכּכם הייחודית והתמדה בה, זִכרו שאפשר להשתמש בכל כלי בדרכים שונות – במיוחד ביֶּדע ובטכנולוגיה, ולכן, שימו לב שאתם רותמים את יכולותיכם לטובת האנוֹשוּת. כשאתם עושים זאת, זִכרו תמיד גם לבדוק את התוצאות שלכם בקפידה, ואל תאפשרו להעדפות ולמשאלות האישיות שלכם להשפיע על הדרך שבה אתם אוספים נתונים ומנתחים אותם.
- איור 5 - המלצות למוחות צעירים.
- מקרא (מלמעלה – ציור זכוכית המגדלת, עם כיוון השעון): Puzzles & surprises = עיסוק במדע כולל חידות והפתעות Stay calm = הישארו רגועים Positive thinking = אַמְּצוּ חשיבה חיובית Persistence = הַקפידו על התמדה Sport training = עִסקו בפעילות גופנית Eat healthy food = אִכלוּ מזון בריא Supporting community = היעזרו בתמיכת הקהילה Asking for advice = אל תהססו לבקש עצה.
ברצוני להדגיש היבט נוסף – חשוב מאוד לדעת לבקש עצות. למדתי זאת בדרך הַקָּשָׁה; בשלב מוקדם בקריירה שלי היססתי לעשות זאת. דאגתי מכך שאם אבקש עזרה אנשים יעריכו אותי פחות, לכן נמנעתי מלבקש עצות. במבט לאחור, אני מבינה שלפעמים התנהלות זו הקשתה על דרכּי. אני אומרת זאת כיוון שככל שהזמן עבר, ובמיוחד כשבני נולד ונאלצתי לְתַמְרֵן בין היותי אימא צעירה למִשְׂרָה כפרופסורית באוניברסיטה, הסכמתי לשקול לבקש עצות. הסתבר שזה מֵקֵל ומסייע מאוד – אנשים שכבר התמודדו עם אתגרים שעמדתי בפניהם, מקצועיים ואישיים כאחד, הציעו לי מִגוון פתרונות שלא הייתי חושבת עליהם. הבנתי שברוב המקרים אנשים אוהבים לעזור לזולת, ואף מכבדים את הנכוֹנוּת לבקש עצה. לכן, אני מעודדת אתכם לבקש עצות לאורך הדרך, בִּמקום להקשוֹת על עצמכם שלא לצורך. כמו כן, חשוב שתזכּרו כי ישנם הרבה אנשים שרוצים בהצלחתכם. מִצאו את האנשים האלה וטַפְּחו את הַקְּשָׁרים איתם, ולעומת זאת אַל תַּקְנוּ חשיבוּת רבה מדי לאנשים שאינם מסייעים לכם.
ברצוני לדבּר איתכם גם על אודות חידות והפתעות. עבורי, המדע מלא בחידות – חלקן גדולות, כאלו שעשויות ללוות אתכם לאורך כל הקריירה שלכם, וחלקן קטנות יותר, שאתם נתקלים בהן יום-יום. החידה הגדולה שאני מנסה לפתור היא להבין איך פועלים החיים עצמם. חידה גדולה זו מתחלקת לחידות קטנות יותר מִדֵּי יום, כאשר אני מנתחת נתונים ומנסה לפתור שאלה פרטנית הנוגעת לתופעה מסוימת. בעיניי, בתמונה הרחבה, מצד אחד המדע מספֵּק לי ביטחון ויציבוּת, בצורת נתיב אובייקטיבי ומדוקדק לחֵקֶר האמת; ומצד אחר המדע מפתיע ומלהיב אותי, באמצעות תגליות בלתי צפויות לאורך הדרך. אני מכנה את התגליות הללו 'הפתעות יום הולדת', ונהנית מהן מאוד. במובן הזה, עֲצָתִי לכם היא ליהנות עד תום מ'הפתעות יום ההולדת' שנִקְרוֹת בדרכּיכם. אני יודעת שעבור חלקכם הפתעות עלולות להראות מאיימות, אך מבטיחה לכם שההפתעות שבהן תִּתָּקלו בתחום המדע הן טובות, אם תתייחסו אליהן ככאלה. ככל שתעמיקו יותר בתחום התמחות מסוים, כך תרגישו חופשיים יותר לצאת מאזור הנוֹחוּת שלכם, ולחקור 'הפתעות יום הולדת' מדעיות.
לסיום, אבקש להפנוֹת כמה מילות עידוד מיוחדות למדעניות העתידיות שביניכם. כפי שתוכלו להתרשם מהמקרה שלי, נשים יכולות לפתֵּח קריירה מדעית המובילה להצלחה, למימוש עצמי, ולרוב גם לשִׂמחה. איני בטוחה שאתן יודעות זאת, אך בשנת 2009, כאשר קרול גריידר ואני זכינו בפרס נובל לפיזיולוגיה או לרפואה, שלוש נשים אחרות זכו גם הן בפרסי נובל, בתחומים כימיה, כלכלה וספרוּת. הִרגשתי שהצלחנו להעביר מֶסֶר משמעותי למדעניות ולמדענים מהדור הצעיר – שלפיו זוכי פרס נובל יכולים להיות נשים וגברים באותה המידה. על כן, אני מרגישה שנפל בחלקי הכבוד להיות סֵמֶל לדורות הבאים של הנשים, ושל כל האנשים, שמעוניינות ומעוניינים לעסוק במדע.
חומרים נוספים
1. The Telomere Effect: A Revolutionary Approach to Living Younger, Healthier, Longer—Amazon.
2. Women who changed Science—Elizabeth Blackburn.
3. Elizabeth Blackburn on the telomere effect—The Guardian.
מילון מונחים
כְרוֹמוֹזוֹם (Chromosome): ↑ מבנה של דנ''א הדחוס בצפיפות בתוך תאים.
דנ''א (DNA): ↑ המולקולה הנושאת את המידע על אודות נראותם של אורגניזמים חיים, ותפקודם.
אֵיקַרְיוֹטים (Eukaryotes): ↑ אורגניזמים שתאיהם מכילים גרעין.
פְּרוֹקַרְיוֹטִים (Prokaryotes): ↑ אורגניזמים שתאיהם אינם מכילים גרעין.
טֶלוֹמֵר (Telomere): ↑ רצף דנ''א 'מֵגֵן' (כמו סוג של פקק), המופיע בסופיהם של כרומוזומים ליניאריים.
אֶנְזִימִים (Enzymes): ↑ מבנֵי חלבונים שמעצימים את הפעילות הכימית המתרחשת בתאים חיים.
טֶלוֹמֵרָאז (Telomerase): ↑ אנזים המוסיף דנ''א טלומרי לכרומוזומים.
רנ''א (RNA): ↑ עותק נייד של דנ''א המשמש את התא לביצוע פעולות שונות, כמו שִׁכְפּוּל דנ''א.
הצהרת ניגוד אינטרסים
המחברים מצהירים כל המחקר נערך בהעדר כי קשר מסחרי או פיננסי שיכול להתפרש כניגוד אינטרסים פוטנציאלי.
תודות
ברצוני להודות לנועה שגב על עריכת הריאיון שהיווה את הבסיס למאמר זה, ועל כתיבה משותפת של המאמר. תודה לאיריס גת עבור האיורים, ול-Susan Debad על עריכת כתב היד.
מקורות
[1] ↑ Muller, H. J. 1938. The remaking of chromosomes. Collect. Net 13:181–98.
[2] ↑ McClintock, B. 1939. The behavior in successive nuclear divisions of a chromosome broken at meiosis. Proc. Natl. Acad. Sci. U.S.A. 25:405–16. doi: 10.1073/pnas.25.8.405
[3] ↑ Blackburn, E. H., and Gall, J. G. 1978. A tandemly repeated sequence at the termini of the extrachromosomal ribosomal RNA genes in Tetrahymena. J. Mol. Biol. 120:33–53.
[4] ↑ Blackburn, E. H. 2010. Telomeres and telomerase: the means to the end (Nobel lecture). Angew. Chem. Int. Ed. 49:7405–21. doi: 10.1002/anie.201002387
[5] ↑ Greider, C. W., and Blackburn, E. H. 1985. Identification of a specific telomere terminal transferase activity in Tetrahymena extracts. Cell. 43:405–13.
[6] ↑ Greider, C. W., and Blackburn, E. H. 1987. The telomere terminal transferase of Tetrahymena is a ribonucleoprotein enzyme with two kinds of primer specificity. Cell. 51:887–98.
[7] ↑ Yu, G. L., Bradley, J. D., Attardi, L. D., and Blackburn, E. H. 1990. In vivo alteration of telomere sequences and senescence caused by mutated Tetrahymena telomerase RNAs. Nature. 344:126–32.
[8] ↑ Epel, E. S., Blackburn, E. H., Lin, J., Dhabhar, F. S., Adler, N. E., Morrow, J. D., et al. 2004. Accelerated telomere shortening in response to life stress. Proc. Natl. Acad. Sci. U.S.A. 101:17312–5. doi: 10.1073/pnas.0407162101
[9] ↑ Blackburn, E. H., Epel, E. S., and Lin, J. 2015. Human telomere biology: a contributory and interactive factor in aging, disease risks, and protection. Science. 350:1193–8. doi: 10.1126/science.aab3389
[10] ↑ Blackburn, E., and Epel, E. 2017. The Telomere Effect: A Revolutionary Approach to Living Younger, Healthier, Longer. New York, NY: Grand Central Publishing.
