摘要
你的日常选择, 包括你的运动量、吃的食物, 甚至是思考的方式, 都可以改变你身体细胞中的基本单元。 在这篇文章中, 我将向你介绍储存生物基因的 DNA 分子的保护端——端粒, 以及我们发现的负责添加和维持端粒的酶——端粒酶。在深入了解端粒和端粒酶的分子细节之后, 我将为你揭示端粒和人类健康之间一些非常有趣的联系。我希望在本文结束时, 你会惊喜地了解到心理、环境和社会因素是如何影响我们的生物学的基本原理。
2009 年, 伊丽莎白 ⋅ 布莱克本教授、卡罗尔 ⋅ 格莱德尔教授和杰克 ⋅ 绍斯塔克教授, 因发现端粒和端粒酶是如何保护染色体获得诺贝尔生理学或医学奖。
DNA 末端的保护套
生命, 因其错综复杂, 像个巨大的谜题。像你我这样好奇的人总会问: “这是什么?” “这是怎么回事?”以及“为什么会这样?” 我选择通过研究生物, 也就是生命的科学, 来应对这种无尽的好奇心。但是生物学是如此复杂, 你必须时常问自己: 我能理解的东西是什么, 我的研究应该专注于什么。否则, 你很快就会招架不住你所研究的生物现象的种种细节。分子生物学是生物学中通过研究分子的面貌及其相互作用来研究生物过程的一种途径。它对我来说是一个令人欢喜的科学领域, 因为在很多方面, 它可以帮助你回答关于生命奥秘的具体而基本的问题。在这篇文章中, 我将介绍我们利用分子生物学获得的发现, 也就是关于 DNA 分子末端的一个重要保护机制, 而 DNA 分子上含有父母遗传给孩子的遗传指令或密码。但首先, 我们先了解一些基本的概念。
DNA, 染色体和复制
每个活细胞都包含一种叫做染色体的结构。每条染色体都含有一种叫做脱氧核糖核酸 (DNA) 的聚合物 (一种非常大的分子)。所有这些 DNA 就像一个指令库, 告诉细胞以及由这些细胞组成的生物如何发挥其功能。DNA 分子以双螺旋的形式存在, 由两条方向彼此相反的线性链组成, 并扭曲在一起形成双螺旋(图 1)。在染色体中, DNA 紧密地缠绕和聚集在细胞中(图 1)。比如人类细胞有23 对染色体, 包含了我们所有的 DNA。这些染色体位于细胞核中, 因为每条染色体都有两个端点, 所以被称为线性染色体。真核生物的染色体都是线性染色体,真核生物是指细胞中具有细胞核的生物, 包括所有的动物、植物、真菌以及大多数藻类。相比之下, 细胞中没有细胞核的生物, 称为原核生物, 如细菌, 它们有着圆形的染色体, 没有两端, 而是像一个圆圈。
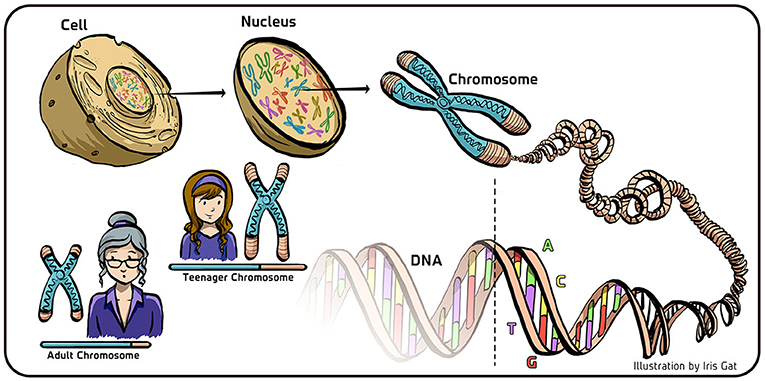
- 图 1 - 真核细胞中的 DNA 和染色体。
- 在真核生物中, DNA 储存在细胞核中, 盘绕和聚集成被称为染色体的结构。DNA 以双螺旋结构的形式存在, 由四个碱基 (A、T、G 和 C) 组成, 这里用四种颜色示意。当细胞分裂时, DNA 被复制, 从原来的双螺旋结构中创造出两个新的双螺旋结构。复制 DNA 的分子机制并不复制染色体末端的 DNA 序列 (DNA 的透明部分;底部)。这就会导致 DNA 随着年龄的增长而变短 (左下)。为了确保遗传物质的稳定遗传, 在复制过程中需要一种特殊的机制来保护 DNA 序列的末端。
当细胞分裂时, 它的 DNA 必须被复制, 这样新的细胞才能包含所有存储在 DNA 中的必要指令。你可能知道, DNA 是由四种称为碱基的基本化学成分组成的长链, 这四种碱基分别用字母 A、T、G 和 C 表示 (A 代表腺嘌呤,T 代表胸腺嘧啶, G 代表鸟嘌呤, C 代表胞嘧啶)。DNA 上这些碱基的序列就是细胞的“说明书”。在组成双螺旋的两条链中, 碱基总是成对出现,A-T 和G-C, 因此双螺旋的一条链中每条A 的对面都有一个T, G 的对面有一个C, 反之亦然 (图 1)。
当 DNA 复制在细胞核内发生时, 复杂的细胞机制首先将双螺旋结构分离成两条 DNA 链。然后, 每条原始链都作为其互补链合成的模板。在这个过程中, 每条链 (现在已经分离) 中的每个碱基都与其对应碱基配对 (T-A、A-T、G-C 和 C-G), 直到为原始 DNA 的每条链合成一个全新的互补链。在这个过程的最后, 我们会得到两个新的双螺旋结构, 它们与原始 DNA 完全相同。
到目前为止, 一切顺利——在细胞分裂后, 我们有了一个新的双螺旋 DNA, 准备用于新的真核细胞。但事实证明, 这种复杂机制不能将 DNA 链复制覆盖到它们的末端 ( 图 1), 也就是说, 在细胞分裂过程中, 每条 DNA 链末端的碱基对序列不会被复制。这意味着在每次复制之后, 原始 DNA 会变得越来越短。
这时, 你好奇的头脑会停下来提问: “为什么会发生这种情况? 为什么在细胞分裂过程中 DNA 没有完全复制?” 事实上, 我们并不真正了解。这就是我们生物学家感觉自己像考古学家的例子之一——我们试图利用留存至今的历史文物的零碎信息来破译事件的历史转折。在这里, 我们确定的是 DNA 在细胞分裂过程中没有完全复制 (就像“历史文物”)。 我们推测, 生命进化过程中的第一个细胞是具有环状染色体的原核细胞 (而不是真核细胞), 它们的 DNA 没有游离端, 而具有线性 DNA——因此有 DNA 末端——的真核细胞在进化的较晚阶段出现。
根据这样的推理, 我们认为在真核生物中运行的 DNA 复制机制最初是在原核生物中发展起来的, 在原核生物中, 因为环状 DNA 没有“结束”, 所以环没有端点的问题。这是否意味着真核细胞的线性染色体在每次复制其遗传物质 DNA 时, DNA 中包含的一段重要编码遗传物质会丢失呢? 幸运的是, 情况并非如此, 这都要归功于一种保护机制, 该机制确保了真核生物细胞中对其正常功能至关重要的DNA不会丢失。
端粒: DNA 的保护者
正如我们在前一节 (图 1) 看到的, 在真核生物中, DNA 复制在到达 DNA 链末端之前就会停止。如果有人问你如何保护编码在 DNA 末端的重要内容, 你能想出解决这个难题的办法吗? 事实证明, 在线性染色体的末端, 有一种特殊的 DNA 序列, 称为 端粒 (telomere, 在希腊语中, “telo” 表示末端, “mere” 表示部分)。端粒上的 DNA 被称为 “非编码 DNA”, 它确保 DNA 的编码部分 (包括从父母传递给后代的指令) 能够正确地传递给下一代。
你可以把这些端粒想象成鞋带末端的塑料保护端, 它们对染色体末端DNA复制缺失的情况做了弥补。意思是说, 为了避免在细胞分裂过程中 DNA 末端的重要 (编码) 部分未被复制的情况, 只有部分端粒 (位于染色体的最末端) 没有被复制, 但这不会导致 DNA 物质中有意义 (编码) 的部分有任何缺失。这类似于鞋带的塑料头在多次使用时部分磨损, 但鞋带本身仍然受到保护。更令人兴奋的是, 我们发现当端粒缩短时, 它会吸引一种特殊的酶, 这种酶可以将更多的端粒序列添加到染色体上。因此, 端粒可以得到补充。这是大自然发现的解决线性染色体末端 DNA 复制不完整问题的绝美方法。
1930 年, 穆勒 [1] 和麦克林托克 [2] 将端粒确定为一种保护染色体末端的 “特殊物质”。后来, 随着分子生物学的发展, 人们开始能够对端粒的分子性质进行刻画。1978 年, 我和约瑟夫 • 盖尔在一种叫做嗜热四膜虫 的有趣生物中发现了线性染色体末端的端粒结构, 这种生物通常存在于池塘的绿藻层中 [3]。我们发现, 这种生物的端粒是由特定的 DNA 碱基形式组成的, 即序列 TTGGGG (图 2), 该序列在细胞群中的不同染色体中重复了不同的次数 (约 20-50 次)。不久之后, 在其他生物的端粒中也发现了类似的重复模式, 如纤毛虫 (TTTTGGGG) 和黏菌 (TTAGGG) [4]。而人类的端粒由序列 TTAGGG 组成, 它在我们所有染色体的末端重复了数千次 [4]。
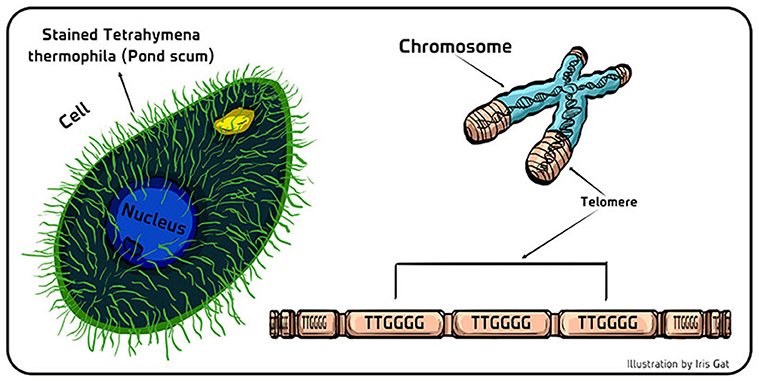
- 图 2 - 嗜热四膜虫的端粒。
- (左) 生活在淡水中的单细胞真核生物嗜热四膜虫的示意图。细胞表面数以百计的毛发状突起 (纤毛) 就像小桨一样使得它可以四处游动寻找食物或配偶。 (右) 端粒就像鞋带的保护端, 保护存储在 DNA 编码部分 (染色体的蓝色部分) 中的遗传材料。端粒 (非编码部分) DNA (染色体的棕色部分) 由重复的碱基单位组成 (嗜热四膜虫中为 TTGGGG;人类中为 TTAGGG)。
此时, 就有了许多关于端粒及其重复模式的有趣的问题。我想重点讲的是: 端粒是如何添加到染色体末端的? 除了细胞增殖外, 这种机制在其他情况下也能为染色体提供保护吗? 在接下来的部分中, 我们将了解构建端粒的奇妙机制, 并看看端粒能教给我们什么关于人类健康和幸福的知识。
端粒酶的发现
20 世纪 80 年代初, 我在研究四膜虫及其相关物种时, 已经知道在它们的生命周期的某一阶段, 原始染色体会被切割成更小的线性染色体, 称为小染色体。我们发现, 和整个染色体一样, 四膜虫小染色体也以 TTGGGG 的端粒重复结束。随后, 我们试着用当时的已知机制来解释 DNA 碱基添加到染色体上的方式。当时已知的 DNA 碱基添加机制只有 DNA 复制和 DNA 重组。每一种机制都有一套非常特定的 DNA 添加规则, 而我们发现的端粒重复却违背了这些规则 (例如, 四膜虫的端粒长度是不同的, 有时重复次数很少, 有时重复次数很多, 有时所有的端粒都同时变长)。这些令人惊讶的行为意味着我们关于端粒结构的新发现与当时关于 DNA 的唯一公认的原则和理论不吻合。
在走到科学的这种特殊的十字路口时, 你必须跳出思维定势, 考虑其他创造性的可能, 以便找到你正在寻找的答案。在这个情况下, 我试图思考什么机制使得端粒重复序列在小染色体从长染色体上剪下来后添加到小染色体上的。一种可能性是细胞中的某种酶的活性导致了这个添加行为。为了验证这一假设, 我将四膜虫细胞的一种提取物放入试管中, 并添加各种化学物质, 以观察是否有任何物质将端粒添加到小染色体上。经过反复试验, 我发现这种提取物确实促进了端粒重复序列的合成。
这时, 卡罗尔 • 格雷德以博士生的身份加入了我的实验室。她的挑战是简化试管中的反应, 这样我们就可以找到负责端粒末端添加的特定酶活性。经过了更多的试验和错误, 卡罗尔将实验简化到了最基本的必需的部分。在四膜虫的染色体被切成小染色体之后, 我们添加了 TTGGGG 的合成重复序列, 因为在这个阶段端粒有望被添加到染色体末端。同时, 我们在试管中加入了DNA 构建模块 (dGTP 和TTP 两个分子), 以及一些镁盐。我们发现 TTGGGG 重复序列确实被添加到了我们合成的 DNA 的末端 [5], 这意味着我们发现了端粒延长的一种可能机制!卡罗尔的研究生同事克莱尔 • 怀曼为这种似乎负责增加端粒重复段的新酶起了一个名字: 端粒酶 [6]。
为了验证我们关于端粒酶对于延长活细胞 DNA (不仅仅是在试管中) 的作用的假设, 我们进行了进一步的实验。我不会在这里详细介绍实验过程, 实验结果是我们发现端粒酶有一个 RNA 部分, 包含了一个与端粒 DNA 序列互补的短序列, 是补充端粒序列的模板。在其中一些实验中, 我们改变 (或“突变”) 了端粒酶的结构, 以观察突变是否影响其合成端粒 DNA 和延长端粒的能力。在保证端粒酶正常功能的前提下, 我们对其负责与端粒延长互补的 RNA 序列进行了突变, 发现四膜虫细胞产生了另一种不同于原始 TTGGG 的端粒重复, 这种端粒序列与我们在模板中添加的碱基变化互补 [7]。
重要的是, 当我们突变端粒酶使其不再起作用时, 四膜虫细胞的端粒在每次细胞分裂中都变短, 最终在 20-25 次分裂后细胞停止分裂并死亡 [7] (图 3, 左)。这意味着当端粒酶的活性被破坏, 通常不死的四膜虫细胞 (似乎永远繁殖) 就会死亡 (在一定数量的繁殖后停止繁殖)。所有这些发现都得出了这样的结论: 端粒酶确实负责将端粒 DNA 添加到线性染色体的末端。正是因为这一发现, 卡罗尔和我被授予了 2009 年的诺贝尔生理学或医学奖 (还有另一位合作者杰克• 绍斯塔克, 我和他一起探索了面包酵母细胞中的端粒功能)。值得注意的是, 在端粒酶被发现之后, 人们发现它的活性不仅仅在细胞增殖的情况下很重要。事实证明, 端粒的 DNA 在细胞内很容易受到化学损伤, 因此在许多不同的情况下它需要得到修复, 尤其是在比较长的时间范围内, 比如人类生命的时间框架下。所以, 端粒酶即使在不增殖的细胞中也很重要 (图 3, 右)。
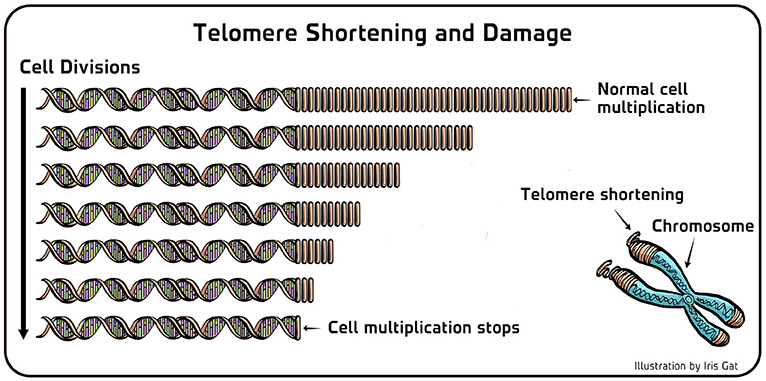
- 图 3 - 端粒缩短和损伤。
- (左) 在端粒酶不能正常工作的四膜虫细胞中, 端粒 DNA (图中右侧重复的 DNA 部分) 随着细胞的每一次增殖而变短。当端粒过短时, 细胞就会停止增殖。这同样适用于人类细胞。(右) 端粒末端在细胞内容易受到化学损伤。因此, 端粒酶的活性对于维持未分裂细胞中的端粒也很重要。
现在你已经熟悉了我在端粒和端粒酶方面的工作, 下面我想介绍我后来在科学道路上开展的另一项研究。这一系列研究将端粒与人类健康以一些意外的方式联系了起来。
端粒的启示: 如何改善人类健康
当我在加州大学旧金山分校研究人类细胞中端粒的维护和端粒酶时, 一位聪明的心理学研究员艾丽莎 • 伊帕尔找到了我。艾丽莎现在是加州大学旧金山分校精神病学系的教授, 当时她正在做关于严重慢性压力的博士后研究。在 21 世纪初, 人们知道处于严重慢性压力下的人经常表现出与自然衰老相似的生理变化, 只是速度更快。换句话说, 慢性压力与人类加速衰老有关。从另一个角度来看, 通过研究端粒, 我们知道, 如果你在四膜虫或酵母细胞的端粒酶中进行基因突变, 使其停止工作, 端粒在每次繁殖中都会变得越来越短, 直到最终变得太短, 这意味着给细胞发出停止增殖的信号 (图 3)。这为该领域提供了一个广受关注的新想法: 也许端粒缩短与哺乳动物的衰老有关。而在当时, 大家还不清楚人类细胞在衰老过程中究竟发生了什么。
当艾丽莎来问我慢性压力是否可能与端粒缩短有关时, 我认为这是一个非常有意思的问题。她告诉我, 她正在做一项极为有趣的研究, 研究对象是孩子患有发育障碍或慢性疾病的母亲。这群母亲承受着严重的慢性压力, 部分原因是在美国这种情况往往缺乏支持。艾丽莎的研究和她的发现与端粒缩短之间可能的联系激发了我的科学兴趣, 除此之外, 我还有一个更私人的原因参与这项研究。那时, 我正非常担心我儿子成长的方方面面。这让我对艾丽莎研究中的女性感同身受, 意识到她们在具有挑战性的护理情况下会多么有压力。
因此, 我们决定开展一项试点研究。这项研究, 以慢性疾病儿童的主要照顾者为研究对象, 我的小组测定了她们端粒酶的活性, 另一个小组测定了她们细胞中的端粒长度。我们将结果与对照组的母亲进行了比较, 对照组的母亲除了没有患有慢性疾病的孩子之外, 其他各方面和试验组的母亲都是相似的。我们的工作由一位名叫林珏的博士后研究员主导, 她之前从事酵母端粒和端粒酶的研究, 对这一新的研究方向很感兴趣。很快, 在第一项研究中, 我们得到了一个令人惊喜的结果——端粒长度与护理的长期性和感知的心理压力之间存在显著的相关性! (图 4)。 这是一个惊人的结果, 它第一次表明, 像慢性压力这样的心理状况可与这种非常明显的、最基本的分子水平上的物理变化相关!
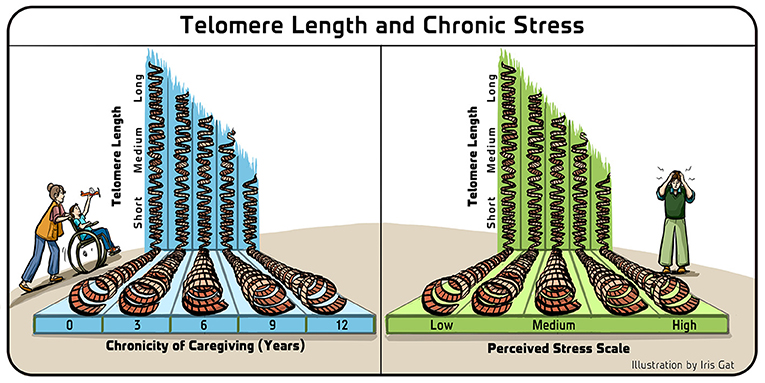
- 图 4 - 端粒长度与慢性压力。
- 首次对照顾慢性疾病儿童的母亲进行的研究发现, 母亲端粒的缩短与她们处于这种情况的年数 (左) 和感知的压力水平 (右) 之间存在统计上显著的相关性。改编自 Epel 等 [8]。
作为科学家, 我们不会急于得出结论, 因为我们知道人类倾向于把我们想看到的强加于现实和数据。这种倾向意味着, 当得到的初始结果符合我们“期望的”假设时, 我们应该特别警惕。因此, 我们决定采取进一步的实验来验证我们的初步结果。其中一种方法是以不同人群为研究对象, 但他们都有相似的长期护理心理压力 (比如照顾一个患有痴呆症的家庭成员), 分析他们端粒长度的结果是否与前期实验一致。其他研究还包括分析端粒长度与其他参数之间的可能关系, 如环境因素、教育因素和其他精神或心理因素。从这些研究中我们发现了许多相似的联系, 因此, 我的团队和其他参与者最终得出结论: 端粒长度和人类健康之间存在非常显著的联系 [9]。
2017 年, 艾丽莎和我为大众读者合著了一本书, 介绍了我们在端粒和人类健康方面的持续工作的核心和灵魂, 名为: 《端粒效应: 活得更年轻、更健康、更长寿的革命性方法》 [10] (中国大陆翻译版书名为: 《端粒: 年轻、健康、长寿的新科学》)。尽管我应该提到, 是我们的出版商坚持让我们在书名中加上“革命”二字, 但事实上, 我们的书确实收集并呈现了许多有趣的事实和结论。这里我想分享两点重要的观点。首先, 生活方式和态度很重要!我们的睡眠、饮食和定期锻炼的方式都会影响我们端粒的长度, 正因为如此, 这些活动可以促进或损害我们的长期健康和长寿。消极思维的习惯也是如此, 它们与端粒缩短有关;相反, 积极和坚韧的思维能增强端粒的良好维护。其次, 我想强调端粒长度更广泛的社会影响, 也就是端粒受到环境的影响。这意味着当我们确保在个人和社会层面上相互支持时, 就能促进良好的端粒维护和整体人类健康。因此, 请记住我们在确保自己的端粒以及人类同胞的端粒健康长寿方面所起的重要作用。我们的日常选择, 以及必须不断努力改善的社会影响, 确实很重要, 因为它们甚至会反映在我们细胞最基本的分子生物学中。
给小读者的建议
关于科学研究和成为科学家, 我有很多建议 (图 5)。我想从强调坚持的力量开始。如果你发现自己对科学感兴趣, 你应该知道坚持的必要性, 因为有时科学看起来相当艰巨和复杂。但是, 不要放弃, 因为你会在某个时刻发现突破挑战的美妙。随后的, 满足感会让你知道坚持是值得的。此外, 为了获得长期的满足感, 你必须确信你所做的一切都是有价值的。所以, 当你选择科学 (或任何其他职业) 的道路时, 一定要从事你认为值得做的事情。这样, 你的工作就有了内在价值, 即使当你想放弃的时候, 这种价值感也会鼓励你坚持下去。当你选择了自己的道路并坚持下去时, 请记住, 任何东西, 尤其是知识和技术, 都可以以不同的方式使用。一定要时刻记住, 无论你从事什么, 都要为人类造福。当你这样做的时候, 也要记住始终严格检查你的结果, 不要让你的个人偏好和愿望干扰你收集和分析数据的方式。
- 图 5 - 对年轻人的建议。
我想强调的另一个方面是征求意见的重要性。在这方面我经历过教训: 在我职业生涯的早期, 我对寻求建议很犹豫。我担心如果我看起来需要帮助, 人们可能会看轻我, 所以我会克制自己不去寻求帮助。事后看来, 这有时让我的人生之路变得更加艰难。我这么说是因为随着时间的推移, 特别是当我儿子出生后, 我必须找到同时做好大学教授和年轻妈妈的方式, 这时我渐渐开始寻求建议。事实证明, 这是非常有帮助的。无论是生活还是工作方面, 我从那些已经解决了我所面临的挑战的人那里都得到了各种我自己从未想过的解决方案。我意识到, 在大多数情况下, 人们是喜欢互相帮助的, 而且实际上大家会尊重你愿意寻求建议的态度。所以我鼓励你在前进的道路上寻求建议, 而不是让你的生活变得不必要的艰难。同时, 请记住, 有很多人都希望你成功, 所以找到这些人并与他们保持密切联系, 同时也要正确看待那些对你没有帮助的人。
我也想和你们谈谈困惑和惊喜。对我来说, 科学充满了谜题, 有些是需要你投入整个职业生涯尝试解决的大谜题, 有些是你每天都要面对的小谜题。我最大的困惑是试图理解生命本身是如何运作的。当我每天分析数据并试图解决一个关于特定现象的特定问题时, 这个大难题就会分解成小的难题。总的来说, 科学为我提供了安全与稳定, 使我通过一种客观的、严谨的方式来获得真理, 同时, 研究过程中意想不到的发现, 会给我带来惊喜和刺激。我把这些惊喜叫做生日礼物的惊喜, 我非常喜欢它们。在这方面, 我给你的建议是, 充分享受你人生道路上的生日礼物惊喜。我知道你们中的一些人可能会被意外吓到, 但我可以向你们保证, 如果你们用这种方式去对待科学, 你们在科学中遇到的那种意外也都是好的惊喜。你对自己的专业领域掌握得越好, 你就越能自由地走出你已知的领域, 探索科学的生日惊喜。
最后, 我想特别对你们中间未来的女科学家说几句鼓励的话。从我的例子你就可以看到, 女性可以在科学领域拥有成功、充实、快乐的职业生涯。我不知道你们是否知道, 2009 年, 当我和卡罗尔 • 格莱德被授予诺贝尔生理学或医学奖时, 另外三位女性也分别获得了诺贝尔奖: 化学奖、经济学奖和文学奖。我觉得这向年轻的科学家们发出了一个重要的信号, 告诉他们诺贝尔奖得主可以是男性, 也可以是女性。因此, 我很荣幸能够成为未来一代女性, 乃至所有科学家的一个标志。
扩展阅读
1. The Telomere Effect: A Revolutionary Approach to Living Younger, Healthier, Longer.
2. Women Who Changed Science—Elizabeth Blackburn.
3. Elizabeth Blackburn on the telomere effect—The Guardian.
术语表
染色体 (Chromosome): ↑ 细胞内紧紧挤在一起的 DNA 结构。
DNA: ↑ 携带关于生物外观和功能信息的分子。
真核生物 (Eukaryotes): ↑ 细胞中含有细胞核的生物。
原核生物 (Prokaryotes): ↑ 细胞中不含有细胞核的生物。
端粒 (Telomere): ↑ 位于线性染色体末端的保护性 DN A序列。
酶 (Enzymes): ↑ 增强生物细胞中化学活动的蛋白质结构。
端粒酶 (Telomerase): ↑ 一种将端粒 DNA 加到染色体的酶。
RNA: ↑ 可移动的 DNA 的复制品, 细胞会使用它做很多事情, 比如复制 DNA。
利益冲突声明
作者声明, 该研究是在没有任何可能被解释为潜在利益冲突的商业或财务关系的情况下进行的。
致谢
感谢诺亚戈夫进行的访谈作为本文的基础, 也感谢他与我共同撰写论文, 感谢爱丽丝 • 盖特提供的插图, 感谢苏珊 • 迪百德对手稿进行的文案编辑。感谢“赛先生”公众号及其译者李可、陈晓雪对本文中文翻译的贡献。
参考文献
[1] ↑ Muller, H. J. 1938. The remaking of chromosomes. Collect. Net 13:181–98.
[2] ↑ McClintock, B. 1939. The behavior in successive nuclear divisions of a chromosome broken at meiosis. Proc. Natl. Acad. Sci. U.S.A. 25:405–16. doi: 10.1073/pnas.25.8.405
[3] ↑ Blackburn, E. H., and Gall, J. G. 1978. A tandemly repeated sequence at the termini of the extrachromosomal ribosomal RNA genes in Tetrahymena. J. Mol. Biol. 120:33–53.
[4] ↑ Blackburn, E. H. 2010. Telomeres and telomerase: the means to the end (Nobel lecture). Angew. Chem. Int. Ed. 49:7405–21. doi: 10.1002/anie.201002387
[5] ↑ Greider, C. W., and Blackburn, E. H. 1985. Identification of a specific telomere terminal transferase activity in Tetrahymena extracts. Cell. 43:405–13.
[6] ↑ Greider, C. W., and Blackburn, E. H. 1987. The telomere terminal transferase of Tetrahymena is a ribonucleoprotein enzyme with two kinds of primer specificity. Cell. 51:887–98.
[7] ↑ Yu, G. L., Bradley, J. D., Attardi, L. D., and Blackburn, E. H. 1990. In vivo alteration of telomere sequences and senescence caused by mutated Tetrahymena telomerase RNAs. Nature. 344:126–32.
[8] ↑ Epel, E. S., Blackburn, E. H., Lin, J., Dhabhar, F. S., Adler, N. E., Morrow, J. D., et al. 2004. Accelerated telomere shortening in response to life stress. Proc. Natl. Acad. Sci. U.S.A. 101:17312–5. doi: 10.1073/pnas.0407162101
[9] ↑ Blackburn, E. H., Epel, E. S., and Lin, J. 2015. Human telomere biology: a contributory and interactive factor in aging, disease risks, and protection. Science. 350:1193–8. doi: 10.1126/science.aab3389
[10] ↑ Blackburn, E., and Epel, E. 2017. The Telomere Effect: A Revolutionary Approach to Living Younger, Healthier, Longer. New York, NY: Grand Central Publishing.
