摘要
本文基于两位作者的访谈撰写。 人体如同一片神秘丛林,每秒钟都有数万亿种奇妙现象悄然发生。 本文将聚焦于这片丛林中一个极为有趣的区域 ——免疫系统。 这个系统凭借“武术大师”杀手 T 细胞守护人体, 专门清除被病毒感染的细胞, 阻止病毒复制及扩散至全身。 让我们一同开启这场免疫系统探索之旅, 揭开杀手 T 细胞精准识别并攻击目标的奥秘。
Peter Doherty 教授与 Rolf Zinkernagel 教授凭借关于细胞介导免疫防御特异性的研究发现, 共同获得 1996 年诺贝尔生理学或医学奖。
人体的守护细胞
免疫系统是人体的一道关键防线, 由白细胞及其产生的活性物质构成, 可有效抵御感染, 维持机体健康 (关于免疫系统的详细介绍, 请参阅“ 补充资料”)。 病毒是一种能够潜入人体、 导致疾病的入侵者, 被入侵的生物就是它们的宿主。 微小的病毒颗粒会感染宿主体内的细胞, 并“诱骗”细胞大量复制病毒。 受感染细胞通常会死亡并释放新生病毒, 让它们在体内不断扩散, 感染更多细胞 (关于病毒的详细介绍, 请参阅这篇诺贝尔奖合辑文章) 。
免疫系统主要采用两大策略对抗病毒感染。 其中一个策略是产生抗体 [1] 。 由名为 B 细胞的淋巴细胞分泌的抗体能够与病毒结合并在感染扩大前使其失活 (图 1A)。 我们可以将抗体比作一支橄榄球队, 本方队员们扑向对方的带球队员 (病毒), 阻止其持球推进。
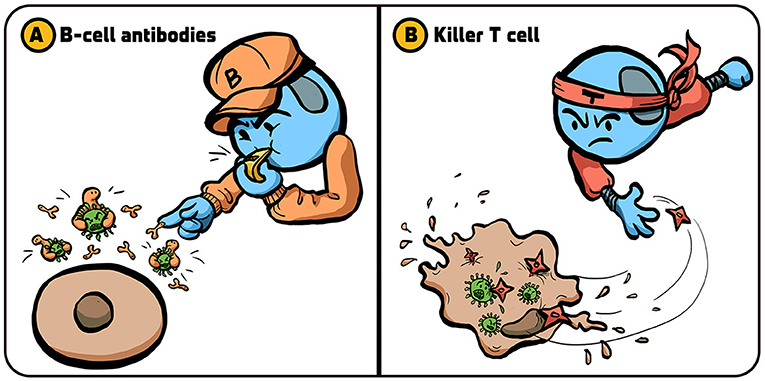
- 图 1 - 免疫系统的抗病毒策略, 通过多种方式应对病毒感染: (A) B 细胞释放抗体 (钳形小分子) 附着于病毒 (绿色), 阻止其侵入身体细胞; (B) 杀手 T 细胞清除被病毒感染的细胞, 阻止新病毒的产生。
- 插图: Iris Gat.
另一个策略是直接清除被病毒感染的细胞 (图 1B), 从而阻断病毒复制。 执行该任务的淋巴细胞被称为细胞毒性 T 淋巴细胞, 简称“ 杀手 T 细胞” [2] 。 当杀手 T 细胞遭遇被病毒感染的细胞时, 它们会在细胞膜上构建通道并启动名为细胞凋亡的程序, 促使该细胞自我毁灭 (关于细胞凋亡机制的详细介绍, 请阅读 这篇文章) 。
是“自体”还是“非自体”?
免疫系统采取杀灭细胞等极端措施应对潜在威胁。 那么, 它如何精准识别抗体攻击目标和细胞清除对象? 换句话说, 它如何在清除感染的同时避免损伤人体? 研究表明, 这需要非常精妙的技巧, 核心在于辨别“自体” (自身细胞与分子) 与“非自体” (入侵者) 。 免疫系统必须准确判断: 如果认不出入侵者, 宿主将丧失防护; 如果将自身细胞误认为入侵者, 则会攻击人体, 导致严重伤害。 由免疫系统自我攻击引发的病症称为自身免疫性疾病, 这类疾病多数尚无有效疗法 (研究人员目前正在验证新冠病毒是否可能诱发罕见自身免疫反应, 这或许是长期新冠症状的潜在成因之一) 。
双受体还是单受体?
20 世纪 70 年代初我研究杀手 T 细胞时, 科学界尚未破解其区分“自体”与“非自体”的机制。 当我们发现杀手 T 细胞会以某种方式靶向“自体”分子 (器官移植排斥中的移植蛋白) 后, 大多数科学家认为这种细胞表面存在两种 受体 (可识别特定分子的蛋白质) : 一种识别“自体”分子, 另一种识别外来 (病毒) “非自体”分子 (图 2A), 即两种分子需通过不同受体识别。
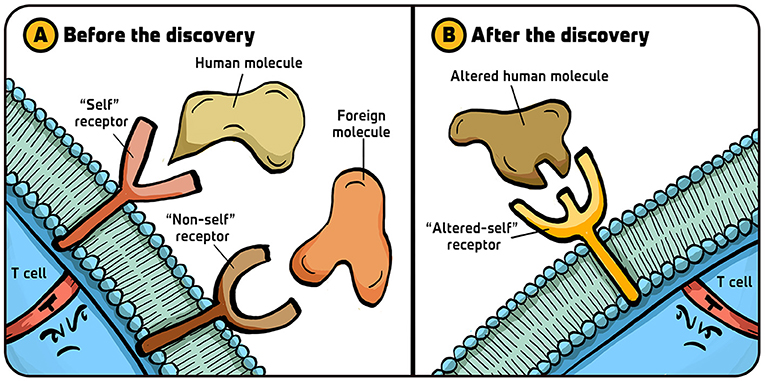
- 图 2 - 杀手 T 细胞受体假说: (A) 在我们发现杀手 T 细胞对“自体”的识别机制并获得诺贝尔奖前, 开展“辅助性” CD4+T 细胞研究的科学家普遍认为, 这些淋巴细胞表面存在两种受体 —— 一种识别机体自身分子 (“ 自体”) , 另一种识别外来分子 (“非自体”)。
- (B) 我们的发现最终明确, 所有 T 细胞仅具有单一免疫特异性受体, 用于识别自体分子的变化 (“改变自体”) 。 插图: Iris Gat。
我与同事 Rolf Zinkernagel 提出了不同见解: 杀手 T 细胞事实上仅通过一种受体识别“自体”分子的变化 (图 2B) 。 这一理念为免疫学提供了全新的阐释方式, 并随着技术手段的进步最终被证实正确。 在讲解单一受体如何识别危险入侵者之前, 我想先谈谈那些引领我们取得这项发现的关键突破。
我的科研历程: 从全球粮食问题到免疫机制解密
17 岁时, 我决定攻读兽医学。 对于一位生长在澳大利亚昆士兰的都市少年而言, 这是个奇怪的决定, 但我相信这将是一场伟大的冒险, 我希望通过改善畜牧业为解决全球粮食问题做出贡献。 尽管在当今的气候变化背景下, 至少发达国家更倡导植物性农业, 但当年我们的认知完全不同。 读博期间, 我对感染致病机制产生了浓厚兴趣, 因此转而研究牛羊感染性疾病。
我在早期取得的一项发现来自对绵羊脑部病毒感染的研究。 当时, 科学界刚开始探索淋巴细胞的作用, 尚未明确其具体运作机制。 在爱丁堡, 我与 Hugh Reid 共同证实被病毒感染的绵羊脑内存在产生抗体的 B 细胞, 这些细胞通过抗体对抗病毒 [3] 。 这是史上首次有直接证据表明感染组织内存在抗体产生细胞, 该发现极大激励了我对身体组织中免疫细胞活动的探索。
在爱丁堡研究绵羊期间, 我意识到需要加深对 T 细胞的认识, 便前往堪培拉澳大利亚国立大学访学数年, 那里的 T 细胞研究非常活跃。 我选择了淋巴细胞脉络丛脑膜炎病毒 (LCMV) 感染小鼠模型, 然后基于先前研究改良了从脑脊液区获取炎症白细胞的技术, 这些细胞主要是 LCMV 感染后侵入大脑及脑膜的 T 细胞。 后来, 巴塞尔大学的医学毕业生 Rolf Zinkernagel 加入实验室, 我们共同完成了那一套历时二十年、 最终为我们赢得诺贝尔生理学或医学奖的实验。
单受体识别“改变自体”的细胞
我与 Rolf 实施了下述实验: 用 LCMV 感染实验室小鼠, 一周 (免疫反应高峰期) 后收集其体内产生的抗病毒杀手 T 细胞 (图 3) 。 将这些 T 细胞与 LCMV 感染的小鼠细胞共同培养, 关键变量在于从感染小鼠体内提取的杀手 T 细胞与靶细胞是否具有相同的移植分子 (在小鼠体内称为 H2, 在人体内称为 HLA) 。 实验发现: 仅当 H2 匹配时, LCMV 免疫 T 细胞才能高效清除感染靶细胞; H2 不匹配时, 杀手 T 细胞则完全无视靶标。 由此, 我们假定杀手 T 细胞通过单一受体识别“改变自体”的感染细胞, 并据此构建出全新的 T 细胞免疫理论。
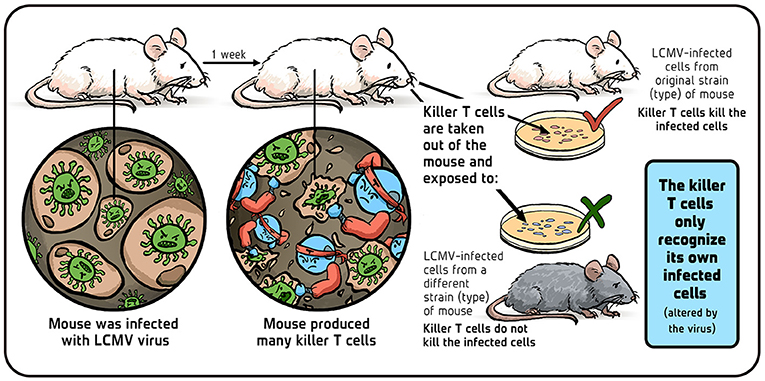
- 图 3 - 杀手 T 细胞会攻击不同品系小鼠的细胞吗? 插图: Iris Gat。
换句话说, 我们假定病毒会改变正常自体分子 (未感染细胞中的固有分子, 在基因完全相同的小鼠间相似, 在基因不同的小鼠间不同) 。 这些自体分子始终存在于宿主细胞表面, 杀手 T 细胞通过识别病毒诱导的分子形状变化, 将其视为感染信号并启动清除程序 [4] 。
虽然当时缺乏验证这一假设的实验技术, 但二十年间的技术发展最终证实了它的正确性 [5–8] 。 新的技术让科学家在细胞表面发现了一种自体分子, 名叫主要组织相容性复合体 (MHC) 。 当病毒入侵时, 病毒蛋白被切碎, 然后与 MHC 分子结合, 共同呈现于细胞表面 (图 4) 。 携带病毒片段会改变 MHC 分子形状, 正是这种形状变化被杀手 T 细胞识别并触发反应 [9] 。 换句话说, T 细胞通过识别 MHC 分子的修饰结构来判定“ 改变自体”的感染细胞。
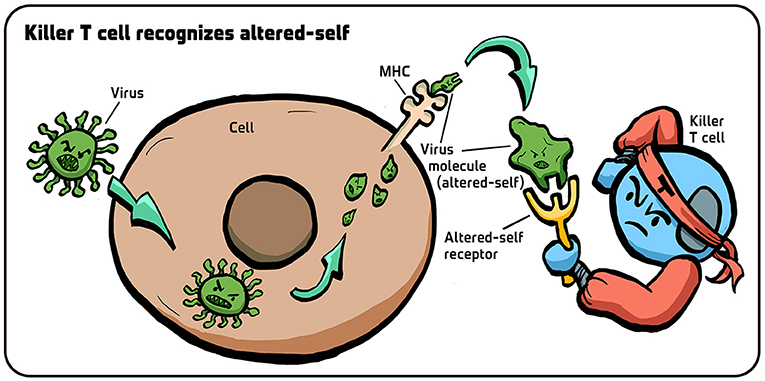
- 图 4 - 杀手 T 细胞如何识别“改变自体”的细胞? 当病毒感染细胞时, 病毒蛋白质会被分解。
- 这些病毒小片段 (绿色小结构) 随后由 MHC 分子携带至细胞表面。 在病毒片段的影响下, MHC 分子的结构会发生变化, 杀手 T 细胞表面的受体通过识别这种形状变化(“改变自体”) 来判定该细胞已被感染。 插图: Iris Gat。
这一理论的证实彻底颠覆了科学界对免疫系统核心成员 —— T 细胞运作机制的认知。
我们的发现能够改善人体健康吗?
对杀手 T 细胞的深入了解在多个医学领域具有重要价值。 首先, 这种了解有助于疫苗研发优化: 既然我们已知免疫系统通过 MHC 分子携带的病毒片段识别感染情况, 那么便可通过添加更多病毒蛋白片段设计出更强效的疫苗。 疫苗包含的片段越丰富, 就越容易引发强烈的杀手 T 细胞反应。 例如, 目前的新冠疫苗仅含有刺突蛋白片段, 而病毒本身却拥有 20 多种可能引发 T 细胞反应的蛋白。
我还高度关注保护性“静息”记忆 T 细胞的特性研究。 这类细胞在再度感染时可重新被激活为杀手 T 细胞。 已有科学家找出了“唤醒”肿瘤内“ 休眠”杀手 T 细胞的方法 (这正是某些抗癌疗法的原理, 详情请浏览此页 [10] ) 。 这项研究还有望推动自身免疫疾病新疗法的开发, 通过纠正误攻自身细胞的 T 细胞与 B 细胞来重建免疫平衡。
给年轻人的建议
我认为科学训练十分有价值, 无论以后走不走科研这条路, 它都能教会你深入思考问题 (图 5) 、 处理数据、 构建论证框架, 以及清晰表达观点的方法。 这些宝贵能力将在人生的各种场景中发挥作用。

- 图 5 - 给年轻人的三项建议: (A) 深入思考问题; (B) 科学是非常广阔的探索乐园; (C) 如果某个事物令你着迷, 那就全身心投入其中! 插图: Iris Gat。
如果你立志成为科学家, 特别是生物学家, 那么我有两则好消息: 第一, 这个领域仍有无数待解之谜;第二, 生物学 (尤其是生物医学研究) 能为拥有不同特长的人提供广阔舞台。 擅长计算机的同学可开发数据分析与集成系统, 热衷思辨的同学能提出新设想、 构建新理论, 擅长管理或产品开发的同学也能在这一领域大展身手。 科研就像一个大型“游乐场”, 可容纳各类人才的创新实践, 并且非常适合那些善于发现事物内在联系的人。
最后, 我想告诉大家: 如果某个事物令你着迷, 请全身心投入其中! 深入探索并把握每个实践机会。 你永远不知道兴趣会将你引向何方, 但在这段旅程中学会的独特思维方式将成为一笔终身财富。 因此, 不必为前途未卜而气馁, 要相信自己的能力必有广阔的用武之地。
补充资料
- 先天免疫系统如何守护健康
- 疾病与健康中的免疫系统 ——第一部分: 微生物与疫苗
- 免疫应答类型: 先天性与适应性免疫, 体液免疫与细胞免疫 | NCLEX-RN | 可汗学院
- Doherty, P. (2006). 《写给初学者的诺贝尔奖获奖指南: 给年轻科学家的建议》. 哥伦比亚大学出版社
术语表
免疫系统 (Immune System): ↑ 保护身体免受感染和特定疾病侵害的防御体系。
白细胞 (White Blood Cells): ↑ 免疫系统的主力军, 帮助身体对抗感染。
抗体 (Antibodies): ↑ 附着于病毒并使其失活的蛋白质。
淋巴细胞 (Lymphocytes): ↑ 负责产生抗体和清除感染细胞的白细胞, 包括 B 细胞与 T 细胞。
细胞毒性 T 淋巴细胞 (Cytotoxic T Lymphocytes): ↑ 即杀手 T 细胞, 一种专门清除被病毒感染的细胞的白细胞。
细胞凋亡 (Apoptosis): ↑ 通过细胞“程序性自杀”清除受损或感染细胞的机制。
自身免疫性疾病 (Autoimmune Diseases): ↑ 免疫系统错误攻击自身机体引发的疾病。
受体 (Receptor): ↑ 细胞表面能结合形状对应分子并引发细胞反应的蛋白质。
免疫学 (Immunology): ↑ 对免疫系统功能的研究。
主要组织相容性复合体 (MHC) (Major Histocompatibility Complex (MHC)): ↑ 存在于细胞表面的自体分子。
利益冲突声明
作者声明本研究不涉及任何潜在商业或财务关系。
致谢
在此感谢 Steffen Jung 教授对文稿提出的宝贵意见, Iris Gat 提供的所有插图, 以及 Susan Debad 完成的编校工作。
AI 人工智能工具使用声明
本文中所有图表附带的替代文本 (alt text) 均由 Frontiers 出版社在人工智能支持下生成。 我们已采取合理措施确保其准确性,包括在可行情况下经由作者审核。 如发现任何问题,请随时联系我们。
参考文献
[1] ↑ Johnson, A., Lewis, J., Raff, M., Roberts, K., and Walter, P. 2002. Molecular Biology of the Cell. New York, NY: Garland Science p. 4.
[2] ↑ Andersen, M. H., Schrama, D., thor Straten, P., and Becker, J. C. 2006. Cytotoxic T cells. J. Investig. Dermatol. 126:32–41. doi: 10.1038/sj.jid.5700001
[3] ↑ Doherty, P. C. 1970. Studies in the experimental pathology of louping-ill encephalitis (Doctoral dissertation). Edinburgh: University of Edinburgh.
[4] ↑ Zinkernagel, R. M., and Doherty, P. C. 1979. MHC-restricted cytotoxic T cells: studies on the biological role of polymorphic major transplantation antigens determining T-cell restriction-specificity, function, and responsiveness. Adv. Immunol. 27:51–177. doi: 10.1016/S0065-2776(08)60262-X
[5] ↑ Townsend, A. R. M., Rothbard, J., Gotch, F. M., Bahadur, G., Wraith, D., and McMichael, A. J. 1986. The epitopes of influenza nucleoprotein recognized by cytotoxic T lymphocytes can be defined with short synthetic peptides. Cell 44:959–68. doi: 10.1016/0092-8674(86)90019-X
[6] ↑ Brown, J. H., Jardetzky, T., Saper, M. A., Samraoui, B., Bjorkman, P. J., and Wiley, D. C. 1988. A hypothetical model of the foreign antigen binding site of class II histocompatibility molecules. Nature 332:845–50. doi: 10.1038/332845a0
[7] ↑ Garcia, K. C., Degano, M., Stanfield, R. L., Brunmark, A., Jackson, M. R., Peterson, P. A., et al. 1996. An αβ T cell receptor structure at 2.5 Å and its orientation in the TCR-MHC complex. Science 274:209–19. doi: 10.1126/science.274.5285.209
[8] ↑ Garboczi, D. N., Ghosh, P., Utz, U., Fan, Q. R., Biddison, W. E., and Wiley, D. C. 1996. Structure of the complex between human T-cell receptor, viral peptide and HLA-A2. Nature 384:134–41. doi: 10.1038/384134a0
[9] ↑ Wieczorek, M., Abualrous, E. T., Sticht, J., Álvaro-Benito, M., Stolzenberg, S., Noé, F., et al. 2017. Major histocompatibility complex (MHC) class I and MHC class II proteins: conformational plasticity in antigen presentation. Front. Immunol. 8:292. doi: 10.3389/fimmu.2017.00292
[10] ↑ Leach, D. R., Krummel, M. F., and Allison, J. P. 1996. Enhancement of antitumor immunity by CTLA-4 blockade. Science 271:1734–6. doi: 10.1126/science.271.5256.1734
