תַקצִיר
גוף האדם בנוי מ־37 טריליון תאים, ומיליארדים מהם מתים מדי יום ביומו. בגוף יש תאים מיוחדים הנקראים מקרופאג’ים, אשר בולעים את התאים הנוטים למות כדי למנוע מהם להצטבר בגופכם. המקרופאג’ים גם מסוגלים לבלוע כל תא שנגוע בחיידק או בנגיף. הדבר עוזר לגופכם להיות בריא ככל האפשר. לפעמים המקרופאג’ים מקבלים איתותים שגויים, והם תוקפים תאים בריאים. כשדבר זה קורה גופכם מְפַתח תגובה אלרגית או דלקת שעלולים להוביל למצב הנקרא אוֹטוֹאימוּניוּת (חיסון עצמי).
המקרופאג’ים הם מנהלי משק הבית
גוף האדם מורכב מאוד. הוא מורכב מ־37 טריליון (37,000,000,000,000) תאים. אם תעמידו בשורה כל תא ותא של גוף האדם, שורת התאים תימתח קצת יותר מהמרחק שבין כדור הארץ לירח! מדי יום ביומו, כ־50 מיליארד (50,000,000,000) תאים בגוף האדם מתים, כחלק תקין מהביולוגיה. צריך לסלק את התאים האלה כדי לשמור על בריאות הגוף. לגוף יש תאים מיוחדים, הנקראים תאים בולעניים (פאגוציטים), ש”בולעים“ את התאים המתים האלה, בתהליך הנקרא פאגוציטוזה (Phagocytose). לפאגוציטים יש תפקיד ”ניהול משק בית“ כדי לוודא ששאריות התאים יסולקו. סוג אחד נפוץ של פאגוציטים הוא המקרופאג’, שפירושו ביוונית ”אוֹכֵל גדול“. כאשר תאים נוטים למות הם שולחים את האיתות ”תאכלו אותי“, חומר כימי הידוע כפוֹסְפָטִידִילְסֵרִין, שמזעיק את המקרופאג’ים וגורם להם לבצע פאגוציטוזה לתאים הנוטים למות. המקרופאג’ים מפרקים את התאים הנוטים למות תוך שימוש בחלבוני עיכול שונים ורבים, בדומה לאלה שנמצאים בקיבה שלנו. לפעמים מקרופאג’ים אלה עלולים לתקוף את הגוף שלנו על-ידי בליעת תאים שאינם נוטים למות. אבל, לא תמיד מדובר בדבר רע.
המקרופאג’ים עוזרים במניעת מחלות
מערכת החיסון שלנו פועלת כדי להגן עלינו מפני מחלות על-ידי זיהוי מולקולות זרות, כגון אלה שעל גבי חיידקים או נגיפים, בלי להגיב נגד מולקולות של עצמנו. חיידקים ונגיפים הגורמים לדלקת או למחלה ידועים כפּתוגנים. כאשר התאים שלכם נגועים בפתוגן, הפתוגן יתחיל להתרבוֹת על-ידי הכנת עותקים רבים מהחומר התורשתי שלו (כגון דנ”א), והוא גם ייצר מולקולות רבות הנלחמות במנגנוני ההגנה של מערכת החיסון שלכם (איור 1) [1]. הדנ“א של הפתוגן והמולקולות שהוא מייצר הם זרים לתאים האנושיים שלנו, ולכן פועלים כאות ”סכנה“, ובזאת מצביעים על כך שמשהו אינו תקין בתא הנגוע. אות הסכנה גורם לפוספטידילסרין להיחשף על שטח הפנים של התא הנגוע, במטרה למשוך אליו מקרופאג’ים. אחרי הגעת המקרופאג’ים לתא הנגוע ובליעתו, הם מציגים לתאים אחרים של מערכת החיסון חלקים מהפתוגן, וכך מערכת החיסון יכולה ליצור זיכרון של אותו פתוגן ספציפי.
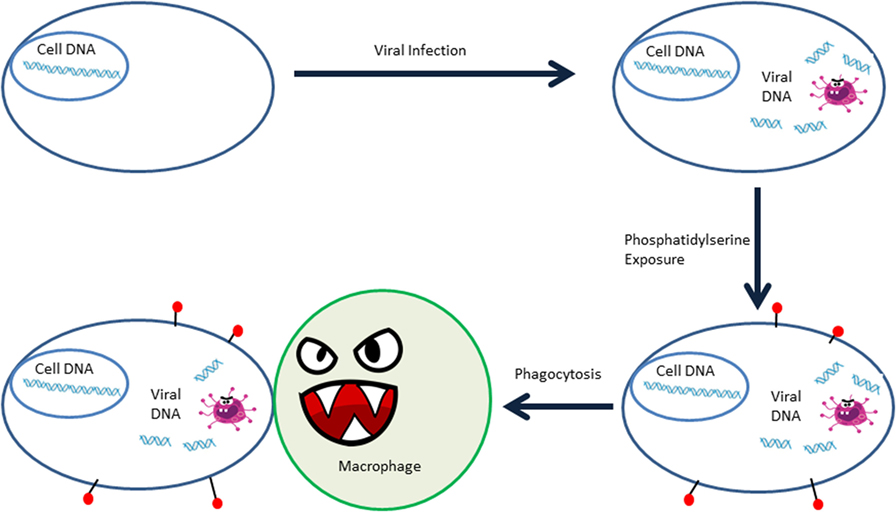
- איור 1 - תא בריא נגוע בנגיף (סגול), אשר גורם לפוספטידילסרין (אדום) להיות מוצג על שטח הפנים של התא, שאחר כך מגייס מקרופאג’ים (ירוק) כדי שיבצעו פאגוציטוזה לתא הנגוע.
- Cell DNA = דנ”א של התא Viral Infection = הדבקה נגיפית Viral DNA = דנ“א של הנגיף.
אם התאים הנגועים אינם עוברים פאגוציטוזה על-ידי המקרופאג’ים תאים נוספים עלולים להיות נגועים בפתוגן, ואפילו האיבר כולו. כאשר המקרופאג’ מפרק את התא הנגוע, החיידקים או הנגיפים אינם יכולים לשרוד או להתרבות – הם מתים יחד עם התא הנגוע. הדבר עוצר את הזיהום ושומר על בריאות הגוף. איור 2 מציג מקרופאג’ שעושה פאגוציטוזה לארבעה תאים שנוטים למות. תמונה זו צולמה על-ידי מיקרוסקופ חזק מאוד שנקרא מיקרוסקופ אלקטרונים.
![איור 2 - תמונה של מיקרוסקופ אלקטרונים המראה מקרופאג’ מבצע פאגוציטוזה של ארבעה תאים מתים (כתמים שחורים בתוך המקרופאג’) [2].](https://www.frontiersin.org/files/Articles/191721/frym-04-00023-HTML/image_m/figure-2.jpg)
- איור 2 - תמונה של מיקרוסקופ אלקטרונים המראה מקרופאג’ מבצע פאגוציטוזה של ארבעה תאים מתים (כתמים שחורים בתוך המקרופאג’) [2].
- Dying Cells = תאים שנוטים למות.
מקטעי דנ“א יכולים להפעיל מקרופאג’ים
בתאים שלנו הדנ”א מצוי בתוך הגרעין, שהוא מֶרְכָּז הבקרה של התא. כאשר דנ“א נמצא מחוץ לגרעין, הדבר מאותת על כך שייתכן שהתא נגוע בחיידק או בנגיף. כשדבר כזה קורה התא שולח אותות הַמְּספרים לתאי מערכת החיסון שקיימת בעיה. נגיפים רבים תוקפים את התא ומעתיקים את הדנ”א שלהם במטרה להחדיר אותו לתוך הדנ“א של התא כדי להחביא אותו ממערכת החיסון. אבל הנגיף ”מבולגן“ מאוד כאשר הוא משכפל את הדנ”א שלו, והוא משאיר מקטעי דנ“א קטנים רבים אשר צפים סביב. אם התא חש במקטעי דנ”א אלה הוא קורא למקרופאג’ים כדי שיבצעו לו פאגוציטוזה בטרם יצליח הדנ“א של הנגיף לחדור לתוך הדנ”א של התא. למרות זאת, במהלך האבולוציה הפכו הנגיפים לחמקניים מאוד. הנגיף משתמש בחלבונים ייחודיים, כגון חלבון הנקרא TREX1, כדי לפרק מקטעי דנ“א קטנים שנמצאים מחוץ לגרעין ועלולים למשוך מקרופאג’ים [3]. בעוד הנגיף ”מבלגן“ את הדנ”א שלו, TREX1 מפרק את מקטעי הדנ“א, וכך המקרופאג’ים אינם תוקפים את התא הנגוע. הדבר גורם לתא להיראות בריא אף שהוא נגוע, ומאפשר לנגיף להמשיך להתרבות. אבל, אם TREX1 יפסיק לפעול, מקטעי הדנ”א יתחילו להצטבר והתא יהיה ממש חולה. אז יתחילו המקרופאג’ים לתקוף את התא החולה גם אם אינו נגוע, דבר שעלול לגרום לדלקת.
גם מערכת החיסון עלולה לגרום לחולי
לפעמים אחרי שחלף אות ה“סכנה” התאים אינם מסירים את האות “תאכלו אותי”. כשדבר כזה קורה, מערכת החיסון חושבת שהתאים עדיין נגועים, והיא תמשיך לתקוף אותם. במקרים אחרים תאים בריאים עלולים להציג למערכת החיסון על שטח הפנים שלהם אות “סכנה” שמפעיל את מערכת החיסון, אף שלא קיימת סכנה בתא המאחסן. כשדבר כזה קורה, המקרופאג’ים אינם יודעים שלמעשה אין איום כלל, והם תוקפים תאים בריאים בכל מקרה. תגובה זו עלולה לגרום לתגובה אלרגית או מצב הנקרא אוֹטוֹאימוּניוּת.
אוטואימוניות היא התהליך שבו מערכת החיסון תוקפת את הגוף. מחלה אוטואימונית עלולה לגרום לדלקת ולכאב. אוטואימוניות עשויה להופיע בכל הגוף או להישאר בתחום של איבר אחד. קיימות יותר מ־80 מחלות אוטואימוניות שונות כגון זאבת, דלקת מפרקים שגרונית ומחלת קרוהן. מחלה אוטואימונית משפיעה על מיליוני אנשים, ונשים רגישות לכך במיוחד – 75% מכלל החולים האוטואימוניים הם נשים. אם כך, איך אפשר לטפל במחלות אוטואימוניות?
טיפולים באוטואימוניות
אוטואימוניות היא בעיה מורכבת, כי מחלות אוטואימוניות שונות כרוכות בכך שמקרופאג’ים תוקפים תאים מסוגים שונים באזורים שונים של הגוף. למשל, בדלקת שריר הלב מערכת החיסון תוקפת את הלב, ובזאבת כלייתית הכליות הן המותקפות. בגלל המורכבות הָרַבָּה של האוטואימוניות, רוב הטיפולים הקיימים במחלות אוטואימוניות מטפלים רק בסימפטומים של המחלה. הטיפולים מאפשרים לחולה להרגיש טוב יותר, אבל למעשה הם אינם גורמים למקרופאג’ים להפסיק לתקוף את הגוף. אחד הטיפולים הנפוצים ביותר עבור אנשים שחולים במחלות אוטואימוניות חמוּרוֹת הוא תרופות שמדכאות את מערכת החיסון. תרופות אלה מדכאות את מערכת החיסון או מאטות את קצב פעולתה. אף שהתרופות אשר מדכאות את מערכת החיסון מועילות בכך שהן גורמות לחולים להרגיש טוב יותר, הן גם מגדילות את הסיכויים של האדם שנוטל אותן לחלות באופן קשה מחיידקים ומנגיפים אחרים, כגון הצטננות רגילה, כי מערכת החיסון כבר אינה פועלת היטב כאשר נוטלים את התרופות האלה. סוג נוסף של תרופות אשר ניתנות לחולים במחלות אוטואימוניות הוא תרופות שמפחיתות את תהליך הדלקת בחולה. תרופות כאלה נקראות תרופות אנטי-דלקתיות. כמה מהתרופות האנטי-דלקתיות משמשות גם לטיפול בכאבי ראש. תרופות אנטי-דלקתיות יכולות לגרום לחולה להרגיש נוח יותר הודות להפגת הכאב.
סיכום
הגוף מורכב מטריליוני תאים, וכאשר התאים האלה חולים ונוטים למות צריך לסלקם. מקרופאג’ים הם סוג אחד של תאים שמכלים את התאים הנגועים אשר נוטים למות כדי לשמור על גוף בריא. תאי הגוף יכולים לחוש שהם נגועים על-ידי חיידקים ונגיפים, בשל נוכחות של מולקולות זרות שמייצר הפתוגן. התא הנגוע משתמש במולקולות זרות אלה כדי לקרוא למקרופאג’ים שיבואו ויבצעו פאגוציטוזה לתא הנגוע. כאשר התא הנגוע נבלע, גם הנגיף או החיידק מתים ואינם יכולים להתרבות ולהדביק תאים אחרים. לפעמים מערכת החיסון מקבלת הודעה שגויה, והיא תוקפת תאים שאינם נגועים ואינם נוטים למות. דבר זה גורם לתגובה אלרגית או למחלה אוטואימונית. טיפולים עכשוויים למחלות אוטואימוניות עוזרים רק להקל על החולה את הסימפטומים, על-ידי הקטנת הכאב או הדלקת או על-ידי דיכוי מערכת החיסון. בעזרת מחקר נוסף, תחומי המדע והרפואה יצליחו להבין טוב יותר את המחלות האוטואימוניות ולטפל בהן.
מילון מונחים
מקרופאג’ (Macrophage): ↑ סוג של תא אשר בולע תאים שנוטים למות או תאים שנגועים בחיידק או בנגיף, בתהליך הנקרא פאגוציטוזה.
פוספטידילסרין (Phosphatidylserine): ↑ אות כימי המסמן למקרופאג’ים “לאכול” תאים מתים.
פתוגנים (Pathogens): ↑ חיידקים או נגיפים הגורמים לזיהום בתאים אנושיים.
TREX1: ↑ חלבון שמפרק דנ“א.
אוטואימוניות (Autoimmunity): ↑ כל מחלה אשר נגרמת על-ידי מקרופאג’ים שתוקפים תאים בריאים.
תרופות מדכאות מערכת חיסון (Immunosuppressants): ↑ תרופות המשמשות להאטת פעילות מערכת החיסון כדי שלא תתקוף תאים בריאים.
הצהרת ניגוד אינטרסים
המחברים מצהירים כי המחקר נערך בהעדר כל קשר מסחרי או פיננסי שיכול להתפרש כניגוד אינטרסים פוטנציאלי.
מקורות
[1] ↑ National Institute of Allergy and Infectious Diseases. 2013. Immune System. Available at: https://www.niaid.nih.gov/research/immune-system-overview
[2] ↑ McIlroy, D., Tanaka, M., Sakahira, H., Fukuyama, H., Suzuki, M., Yamamura, K., et al. 2000. An auxiliary mode of apoptotic DNA fragmentation provided by phagocytes. Genes Dev. 14:549–58. doi: 10.1101/gad.14.5.549
[3] ↑ Bailey, S. L., Harvey, S., Perrino, F. W., and Hollis, T. 2012. Defects in DNA degradation revealed in crystal structures of TREX1 exonuclease mutations linked to autoimmune disease. DNA Repair (Amst.) 11(1):65–73. doi: 10.1016/j.dnarep.2011.10.007
