摘要
你知道铁是地球上最重要的元素之一吗?据推测, 生命是在靠近铁源的地方进化而来的。这意味着最早的生命形式——也是最古老的生物——能够像我们摄入食物一样摄入铁, 来获取能量。这些微小的生物被称为嗜铁微生物, 会出现在泥沙这类沉积物中。但人们对嗜铁微生物在这些沉积物中的生活位置知之甚少——它们是靠近沉积物表层还是底部?在这项研究中, 图宾根大学的一个团队调查了嗜铁微生物的分布和种类。科学家们发现嗜铁微生物可以脱离于它们最喜欢的摄入物 (铁、氧气和光照) 而存活! 这种独立存活的特性, 源于它与一种“活电缆”之间意想不到的非凡友谊。您想知道什么是“活电缆”吗?
你知道有些细菌可以 “吃掉” 铁吗?!
微生物是微观生命形式, 包括细菌、古生菌、真菌、藻类、原生动物和病毒。在本研究中, 我专注于探索细菌。细菌生活在我们的胃部和皮肤上, 也可以在地壳最深处, 乃至云层高处生活, 它们甚至可以成功地存活在南极的冰层下或温泉中。细菌虽小, 但数量众多, 一勺海洋沉积物可含有超过十亿个细菌!因此, 它对我们的环境影响巨大。
为了在如此多样化的环境中生存, 细菌物种不断进化, 不同的物种“摄入”不同的东西, 从而获得生存所需的能量。在本文中, 我们将重点关注铁元素! 嗜铁细菌广泛存在于我们的环境中。除了氧、硅和铝之外, 铁是地球上最常见的元素之一。嗜铁细菌对于地球上生命的起源是必不可少的, 对其他含铁行星 (例如火星) 也可能很重要。
嗜铁细菌可以利用铁为它的生长产生能量, 并在此过程中产生褐色铁矿物形式的废物 [1], 通常称为铁锈。迄今为止, 已发现三类嗜铁细菌可以产生铁矿物质。其中一类依赖光, 这意味着它们需要在光照下才能生存, 另一类依赖氧元素, 还有一类依赖氮元素 [1]。
一些嗜铁细菌生活在泥沙这类沿海沉积物中。典型的沿海沉积物通常遵循地球化学梯度组成不同的沉积层 [2] (图 1)。在阳光可以到达的上层沉积层中, 可以检测到氧气和大量有机物质。在较深的沉积层中, 光线和氧气较少, 但仍然可以测量到一些硝酸盐、有机物质、铁、铁矿物和硫酸盐。这些特定层内包含的物质, 往往都是每层沉积物里不同种类的细菌所偏好的摄入物。
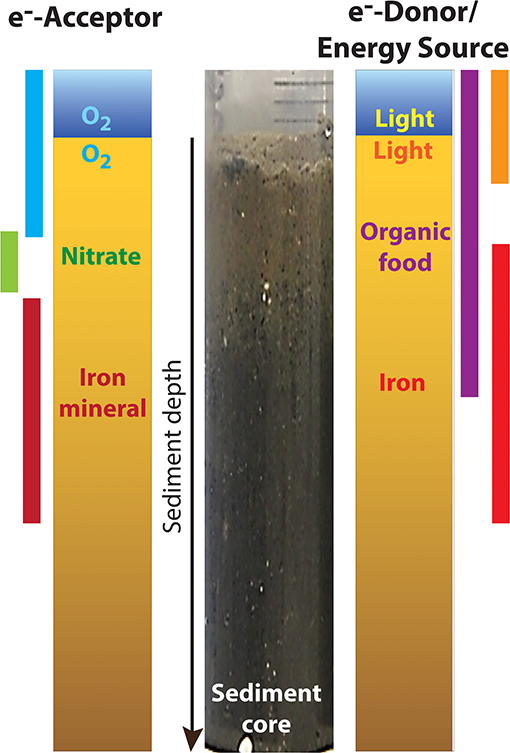
- 图 1 - 图中显示了海洋沉积物中的地球化学梯度, 典型沿海沉积物的层状结构, 中间灰色条形则是包含来自丹麦海岸 (丹麦诺斯明德峡湾) 的沿海沉积物的主体部分。
- 表层因为有机物的原因而呈棕色, 较深层因铁矿物质的缘故而呈黑色。沉积物层中电子受体和电子供体的存在显示在主体部分的左侧和右侧, 各种物质在梯度中的大致位置由彩色条表示。在沉积物的表层, 发生依赖于光、氧和有机物的反应, 而在更深的沉积层, 这些过程依赖于硝酸盐、铁和铁矿物质 (注: e–: 电子, O2: 氧气)。
细菌如何从摄入物中获取能量?
为了更好地理解我的研究发现, 我们首先需要详细地解释一下细菌从摄入物中获取能量的过程。在细胞层面上, 包括细菌在内的所有生物产生生长所需能量的过程称为细胞呼吸。在最小的分子层面上, 这个过程涉及电子交换 (电子是带负电荷的原子粒子)。
原则上, 细菌的一种食物来源是所谓的电子供体 (它提供电子), 另一种食物来源称为电子受体 (它接受电子)。沉积物中典型的电子供体是可溶性铁或有机物质, 例如死去的生物, 而典型的电子受体则是氧、硝酸盐或铁矿物 (图 1)。通过消耗氧气来降解有机物质的过程, 可以提供最多的能量, 因此, 氧气通常会被最先用完, 其次是硝酸盐, 然后是铁矿物质 [2]。
到目前为止, 我们知道嗜铁细菌——和所有其他生物体——需要通过电子转移反应来获取能量。嗜铁细菌接收来自铁 (电子供体) 的电子, 并将电子提供给氧 (电子受体) [1]。总之, 这种从铁到氧的电子转移使细菌获得细胞生长所需的能量。这表明细菌真的很聪明: 它们利用铁 (高电势) 和氧 (低电势) 中电子的能量差来产生能量。你可以想象一下, 这个原理和天然瀑布或者水力发电厂类似。来自铁的具有高能势的电子, 像瀑布水流一样落到具有低能势的氧上。在这个过程中, 嗜铁细菌像水力发电站一样运行它们的“涡轮机”, 并产生能量。嗜铁细菌的电子转移发生在细胞膜, 并且在细胞膜处产生铁矿物质。
值得一提的是, 嗜铁细菌的细胞膜配备了一种特殊的生化机制 (称之为“电线”), 可以沿着细胞膜传输电子 [3]。当然, 嗜铁细菌的电子转移反应要复杂得多, 因此与嗜好其他沉积物的细菌和其他生物不同。
沿海沉积物中嗜铁细菌的意外分布
直到最近, 嗜铁细菌在沿海沉积物层中的自然分布还是未知的。因此, 图宾根大学的研究团队配备了胶靴、手套、水桶、瓶子和注射器, 耗时 3 年, 在丹麦波罗的海沿岸采集各种沉积物样本, 研究嗜铁细菌在典型沿海沉积物中的分布情况, 并且分析了样本中的细菌类型, 以及沉积物上层 (0–5 cm) 中存在的铁、氧和硝酸盐的含量。在沉积物的表层能够检测到氧气, 而在较深的沉积物层中, 氧气逐渐减少 [4] (图 2A)。我认为, 这种氧气逐渐减少的梯度, 也影响了生活在不同深度的沉积层中细菌的类型。然后, 我们寻找沉积物中, 所有典型的依赖光照和氧气生活的细菌。我们希望看到的结论是: 沉积物中大多数依赖光和氧的细菌生活在表层, 只有较少部分生活在深层的沉积物中 [4] (图 2A)。
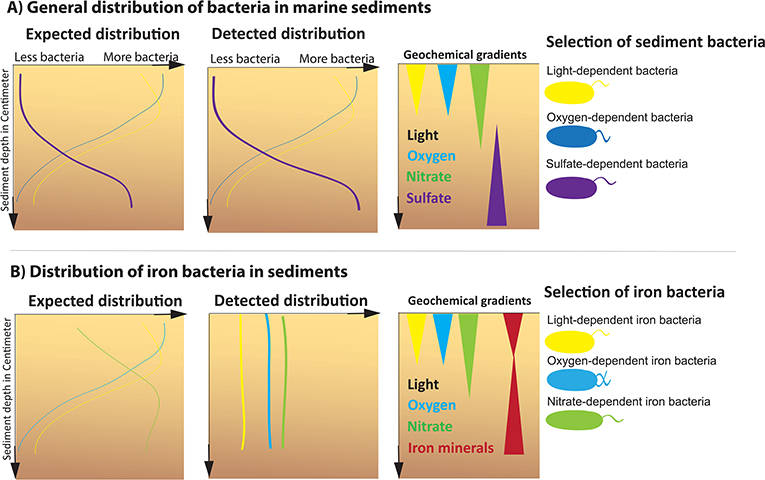
- 图 2 - 图中显示沿海沉积物中预计的和实际的细菌分布。
- (A) 我们预计能观察到所有不同的典型沉积物细菌 (如右图所示) 是根据它们产生能量所需物质的梯度而分布的 (例如, 光, 氧和硫酸盐)。在“地球化学梯度”的图示中, 几种物质的含量显示为三角形, 较宽的部分表示物质的浓度较高, 三角形变窄表示浓度降低。我们检测到大约 75% 的细菌是根据梯度来分布的。当存在大量氧气时, 可以发现大量好氧细菌, 当存在较少氧气时, 几乎检测不到好氧细菌。(B) 然而, 当我们只观察三种类型的铁细菌时, 我们发现它们并不遵循沉积物中的预期分布, 而是遍布所有沉积层。
然而, 当具体观察所有三种类型的嗜铁细菌时, 我们团队很惊讶地发现, 所有三种类型的嗜铁细菌——即使是那些依赖沉积物表层中存在的物质 (如氧气、硝酸盐和阳光) 的嗜铁细菌——在所有沉积层中均匀分布 [4] (图 2B)。这意味着, 嗜铁细菌的行为与大多数其他生活在沉积物中的细菌不同。在考虑它们最喜欢的生活地点时, 它们不会根据氧气、硝酸盐或阳光的递减梯度来选择。这是一个非常有趣的结果, 让我们来试着弄清楚: 为什么嗜铁细菌的行为与其他类型的细菌不同, 并且它们可以生活在所有沉积层中?
我们如何解释沉积物中嗜铁细菌的意外分布?
让我们先用如下几个假设来解释嗜铁细菌在整个沉积物层中的分布 (图 3A-E)。
(A) 嗜铁细菌是否会因蠕虫活动或波浪运动而混入沉积层? 我和我的同事不倾向于这个假设, 因为混合会影响所有沉积物细菌, 所以这不能解释为什么在所有层中只发现嗜铁细菌。
(B) 嗜铁细菌是否可能在某些层中处于某种“休眠”状态, 直到更好的生存条件出现? 然而, 嗜铁细菌其实很活跃, 并没有“休眠”, 所以这个假设也无法解释它们在沉积物中的分布模式。
(C) 也许嗜铁细菌是可移动的, 能够穿过沉积层? 但是很多生活在沉积物里的生物都是可以移动的, 这并不是嗜铁细菌的特殊特征。
(D) 嗜铁细菌能否使用更深沉积层中充满氧气或硝酸盐的“气泡”作为食物来源? 但是充满氧气或其他食物来源的小气泡无法单独解释嗜铁细菌的分布。所以这个假设也被排除了。
(E) 嗜铁细菌是否可以灵活选取不同的食物来源? 同样地, 灵活的饮食无法单独解释沉积物中所有不同嗜铁细菌的分布。
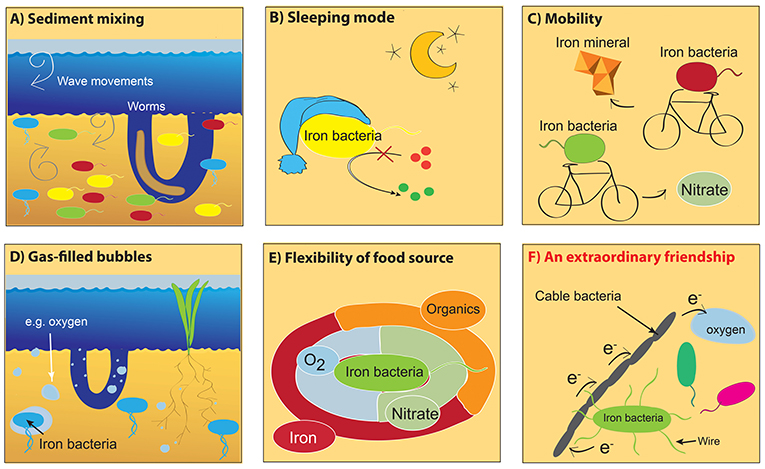
- 图 3 - 为什么嗜铁细菌分布在所有沉积层中?
- 我们探讨了嗜铁细菌不遵循沉积物梯度分布的几个可能原因。 (A) 嗜铁细菌通过波浪或蠕虫进行物理混合; (B) 嗜铁细菌正在“休眠”, 不需要营养; (C) 嗜铁细菌可以在各层之间移动; (D) 嗜铁细菌能找到充满氧气或硝酸盐的小气泡; (E) 嗜铁细菌可以摄入各类“食物”; (F) 嗜铁细菌与电缆细菌相互作用, 互相交换电子。从 (A) 到 (E) 的任何假设都无法解释嗜铁细菌的分布。因此, 我们推想嗜铁细菌可以使用电缆细菌作为电子受体。嗜铁细菌能够独立于地球化学梯度 (例如氧气含量的梯度) 而生存, 要归功于它们的朋友——电缆细菌的帮助 (注: e–, 即电子; O2, 即氧气)。
当我们意识到无法用上述假设中的任何一个来解释嗜铁细菌的行为时, 我们团队不得不继续研究, 整个过程也越来越令人兴奋!
令人着迷的电缆细菌是否在这里发挥了作用?
2010 年, 丹麦电微生物学中心的一组科学家发现了一种不寻常的电细菌 [5], 它们具有包含数千个细胞的长线状多细胞结构。这些非凡的细菌被称为电缆细菌。与其他细菌相比, 电缆细菌可以在其多细胞电缆结构中长距离 (约 5 厘米) 传输电子, 其功能类似于沉积物中的电缆! 因此, 嗜铁细菌在沉积物不同层面分布的原因可能在于电缆细菌。实际上, 电缆细菌和嗜铁细菌共同生活在同一沉积层中 [4] (图 3F)。为什么说这两者之间存在非凡的友谊呢? 在上文中, 我们介绍了嗜铁细菌需要电子转移反应来获得能量, 并且嗜铁细菌在其细胞膜上配备了特殊的生化机制 (也称为电线), 可帮助它们提供或获取电子 [3]。使用这种生化机制, 当嗜铁细菌没有氧气作为电子受体时, 它们可以将电子转移到电缆细菌! 电缆细菌可以充当嗜铁细菌的电子受体, 从嗜铁细菌中获取电子并将它们通过电缆移动到沉积物表面。在沉积物表面, 有大量的氧气可以充当正常的电子受体。由于与电缆细菌的这一非凡友谊, 需要氧气的嗜铁细菌可以在所有沉积层中生存, 不受到它们生活的沉积层中氧气含量的限制, 并将电缆细菌用作一种通气管! 类似地, 依赖硝酸盐和光的嗜铁细菌, 也可以独立于所有沉积层中的食物来源而存活 (图 3B)。
非凡的微生物友谊
嗜铁细菌和电缆细菌之间的这种非凡友谊, 有待找到更多的证据来证实。然而, 通过这项研究, 我们团队已经探明, 嗜铁细菌很可能使用一种独特的策略在所有沉积层中生存, 无须担忧此处是否有足够的摄入物来源!
嗜铁细菌可以利用细胞膜上传输电子的特殊能力 (大多数其他细菌并不具备这项能力), 与电缆细菌相互作用。因此, 嗜铁细菌和电缆细菌的非凡友谊可以解释嗜铁细菌为何在海洋沉积物中特殊的分布。嗜铁细菌和电缆细菌在所有沉积层中令人惊讶的分布和意想不到的关系, 也对整个微生物群落产生积极影响, 因为嗜铁细菌可以独立于表层的光和氧气, 生活在更深的沉积层中, 并且可以通过产生铁矿物质帮助其他生物。例如, 有毒物质可以粘附在它们产生的铁矿物上, 使其他生物免受其害。这种非凡的细菌友谊可以对生态系统产生许多积极的副作用。当然, 我们还需要进一步的研究, 来了解这两个朋友之间的确切关系。科学家们了解到, 即使是发生在小小细菌之间的合作, 也可以为其他生物的生存做贡献。当两个细菌群体通过合作而互相受益时, 这种积极的互动就会通过生命之树发生。
术语表
海洋沉积物 (Marine Sediment): ↑ 被风、冰和河流从沿海地区带到海洋的岩石和土壤颗粒, 以及海洋生物的遗骸。
地球化学梯度 (Geochemical Gradient): ↑ 两个不同区域 (本文中是沉积层表面和更深的沉积层) 之间的差异, 具体为氧气或光等物质的量, 或者温度、压力或含盐浓度的大小。
细胞呼吸 (Cellular Respiration): ↑ 所有生物体用来产生生存所需能量的过程。它涉及电子从电子供体 (高能化合物) 转移到电子受体 (低能化合物), 从而释放能量。
电子供体 (Electron Donor): ↑ 在细胞呼吸的半反应过程中向其他化合物释放电子的化学物质。例如: 有机物或铁。
电子受体 (Electron Acceptor): ↑ 在细胞呼吸的半反应过程中接受从其他化合物转移而来的电子的化学物质。例如: 氧、硝酸盐、硫酸盐、铁矿物质。
利益冲突声明
作者声明, 该研究是在没有任何可能被解释为潜在利益冲突的商业或财务关系的情况下进行的。
原文
↑Otte, J. M., Harter, J., Laufer, K., Blackwell, N., Kappler, A., and Kleindienst, S. 2018. The distribution of active iron cycling bacteria in marine and freshwater sediments is decoupled from geochemical gradients. Environ. Microbiol. 20:2483–99. doi: 10.1111/1462-2920.14260
参考文献
[1] ↑ Weber, K. A., Achenbach, L. A., and Coates, J. D. 2006. Microorganisms pumping iron: anaerobic microbial iron oxidation and reduction. Nat. Rev. Microbiol. 4:752–64. doi: 10.1038/nrmicro1490
[2] ↑ Canfield, D. E., and Thamdrup, B. 2009. Towards a consistent classification scheme for geochemical environments, or, why we wish the term ‘suboxic’ would go away. Geobiology 7:385–92. doi: 10.1111/j.1472-4669.2009.00214.x
[3] ↑ Reguera, G., McCarthy, K. D., Mehta, T., and Nicoll, J. S. 2005. Extracellular electron transfer via microbial nanowires. Nature 435:1098–109. doi: 10.1038/nature03661
[4] ↑ Otte, J. M., Harter, J., Laufer, K., Blackwell, N., Kappler, A., and Kleindienst, S. 2018. The distribution of active iron cycling bacteria in marine and freshwater sediments is decoupled from geochemical gradients. Environ. Microbiol. 20:2483–99. doi: 10.1111/1462-2920.14260
[5] ↑ Pfeffer C., Larsen, S., Song, J., Dong, M., Besenbacher, F., Meyer, R. L., et al. 2012. Filamentous bacteria transport electrons over centimetre distances. Nature 491:218–21. doi: 10.1038/nature11586
