תַקצִיר
ייתכן שמעולם לא שמעתם עליו, אולם קיים סרטן מוח נדיר אך אגרסיבי שנקרא “גליובלסטומה”. שמו מורכב ממש כמו מציאת תרופה שתטפל בו! בדרך כלל כשתאים מבינים שהם נעשים חולים, הם מסוגלים לשלוח הודעות מצוקה ויכולים להשמיד את עצמם לפני שהם מתפתחים להיות מחלה. לרוע המזל, תאי סרטן הגליובלסטומה אינטליגנטים במידה יוצאת דופן; הם שולחים הרבה מולקולות קטנות (“BLOCKERS” כדי ליירט את ההודעות האלה. בעזרת הסְכֶמָה הזו תאי הסרטן נעשים בני אלמוות; הם יכולים להתרבוֹת ולהתפשט בכל המוח. לכן, חוקרים בוחנים את הבעיה הזו כדי לנסות למצוא תרופה חדשה שתוכל לתפוס את ה-BLOCKERS האלה. אנו חקרנו את הפוטנציאל הטיפולי של תרופה שתופסת את המולקולות הקטנות האלה ונועלת אותן, מה שמאפשר לתאי הסרטן להרוס את עצמם. באופן מרגש, מצאנו שהתרופה הזו מסוגלת להילחם בסרטן גליובלסטומה בעכברים!
האם אתם יודעים כמה תאים מרכיבים את גופכם? אתם לא תאמינו... בסביבות מאה אלף מיליארדים! הגוף הוא מכונה מדהימה; הוא שולט בכל החלקים הקטנים האלה כדי לעבוד בצורה טובה ביומיום. לכל התאים שלנו יש תפקיד מסוים כמו למשל יצירת איברים דוגמת המוח. לעיתים חלק מהתאים מותמרים, מה שאומר שהם עוברים מוטציות (קצת כמו צבי הנינג’ה) ומתחילים לעשות שטויות. זה קורה כל יום לכולנו. כשהתאים המוטנטים האלה נעשים רבים מדי באיבר מסוים, זה נראה כמו סרטן. אולם אז השאלה היא: מדוע לא כל האנשים מפתחים סרטן, אם חלק מהתאים מותמרים כל הזמן?
לתאים שלנו יש מערכת אזעקה שמופעלת כשהם נעשים חולים ומזיקים לגוף. התאים החולים האלה שולחים אותות מצוקה, כמו S.O.S, ואומרים לגוף להפעיל את מערכת ההגנה שלו. התופעה הזו נקראת “אפופטוזיס”, וזהו תהליך של השמדה עצמית, או התאבדות מתוכננת של תאים. במרבית הזמן מערכת האזעקה הזו פועלת בצורה מושלמת, אולם לפעמים ישנם מקרים יוצאי דופן כמו למשל סרטן המוח שנקרא גליובלסטומה. גליובלסטומה הוא סוג סרטן נדיר שמופיע “רק” אצל 250,000 איש בכל שנה. לרוע המזל, הוא גם סרטן אגרסיבי ונכון להיום איננו יודעים לרפא מטופלים שחולים בגליוסלבטומה [1]. אולם, זיכרו שבכל יום המחקר מתקדם במה שנוגע לטיפולים בסרטן. כיום אנו יודעים לטפל בסוגי סרטן רבים כמו למשל סרטן השד, כך שמטופלים יוכלו לחיות חיים ארוכים.
מתקפת הנגד של הגליובלסטומה
תאי גליובלסטומה מפתחים מנגנונים מתוחכמים במטרה לברוח מאפופטוזיס, כולל ייצור של מולקולות שנקראות מעכבי אפופטוזיס (IAPSs), שאנו נקרא להן “BLOCKERS”. ה-BLOCKERS נוכחוֹת בכל התאים ומסייעות להם לשרוד, אולם הן רבות יותר בתאי סרטן! בגליובלסטומה, ה-BLOCKERS מיירטות את אות ה-S.O.S מתאי הסרטן כך שהתאים האלה לא יכולים לבצע השמדה עצמית. ה-BLOCKERS גם מוֹנעים ממערכת החיסון לראות את התיישבות הסרטן במוח. כדי לאזן את הפעילויות המסוכנות האלה של ה-BLOCKERS, כימאים יצרו תרופה שצריכה להיות מסוגלת לקשור את ה-BLOCKERS ולנטרל אותן [2]. באופן הזה, אותות ה-S.O.S שנשלחים על-ידי תאי הסרטן הראשונים יגיעו למטרות המיועדות, ותאי הסרטן יושמדו (איור 1).
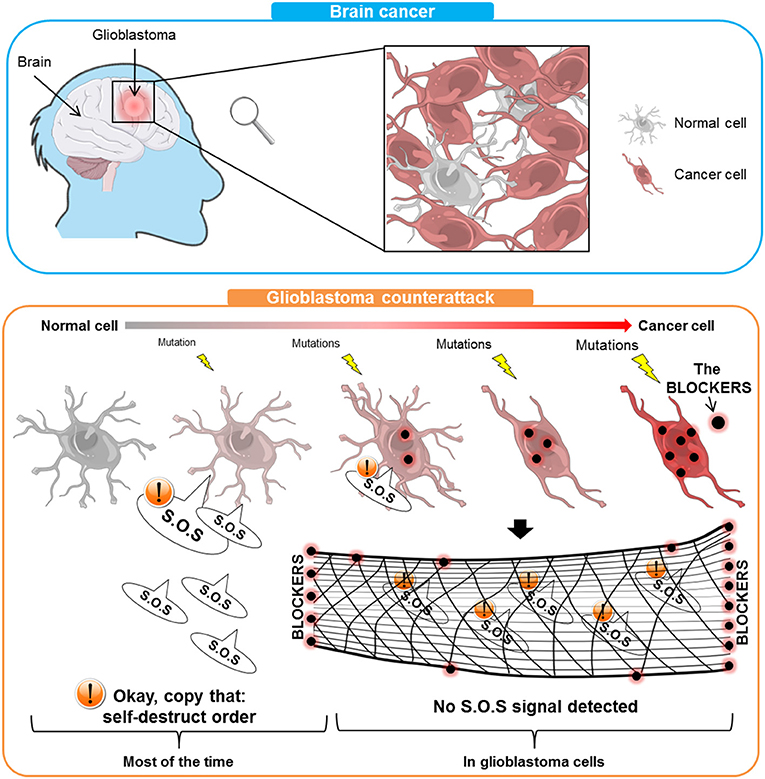
- איור 1 - גליובלסטומה הוא סרטן מוח שבדרך כלל משפיע על אנשים מבוגרים.
- בפאנל העליון אתם יכולים לראות שהגליובלסטומה מכיל תאי סרטן מעורבבים עם תאים רגילים. בפאנל התחתון, תאים רגילים עוברים מוטציות (ברקים צהובים) שמתמירים אותם לתאי סרטן שיש להם הרבה BLOCKERS (נקודות אדומות/ שחורות). במרבית הזמן, תאים חולים מצווים לבצע השמדה עצמית. במקרה של גליובלסטומה, ה-BLOCKERS מיירטים את הודעות ה-S.O.S (כמות הרשת שבאיור), מה שמאפשר לתאי הסרטן להישאר בחיים ולהתפשט.
כיצד בדקנו את התרופה החדשה?
ביולוגים (אנשים שחוקרים יצורים חיים) ממשיכים את עבודתם של הכימאים במטרה לבדוק את כוחה של התרופה החדשה בטיפול בסרטן. עבור התרופה שלנו, המחקר נערך בשני שלבים: חלק in vitro, שמשמעותו שערכנו ניסויים עם התרופה באמצעות תאים במבחנות בדיקה במעבדה, וחלק in vivo שבו חקרנו את השפעות התרופה על חיות. עבור מחקרי ה-in vitro השתמשנו בתאי סרטן אנושיים. העיקרון הוא פשוט: אנו לוקחים חתיכה מהגידול (מסה מסוימת של תאי סרטן) מחולה הסרטן, מסירים את התאים מהגידול ומספקים להם מים ומזון. ברגע שתאי הסרטן גדלים טוב במבחנות אנו יכולים להתחיל לחקור אותם ולבצע מבדקים עם התרופה.
ראשית, חקרנו את השפעת התרופה על ייצור ה-BLOCKERS על-ידי תאי הסרטן [3]. אכן, התרופה גרמה להפחתה בייצור ה-BLOCKERS מאחר שהיא קשרה אותם וסייעה לתאים להיפטר מהם. לאחר מכן, תאי הסרטן היו מסוגלים לבצע השמדה עצמית. כדי להעריך את יעילות התרופה הזו היינו צריכים להשוות אותה למשהו. לכן, היו לנו תאי סרטן שטופלו באמצעות התרופה, וקבוצה אחרת של תאי סרטן שטיפלנו בהם רק באמצעות מים (שנקראים תאי בקרה). ראינו שהטיפול באמצעות התרופה גרם לאפופטוזיס בתאי הסרטן וכמובן שתאי הביקורת נשארו בחיים (איור 2).
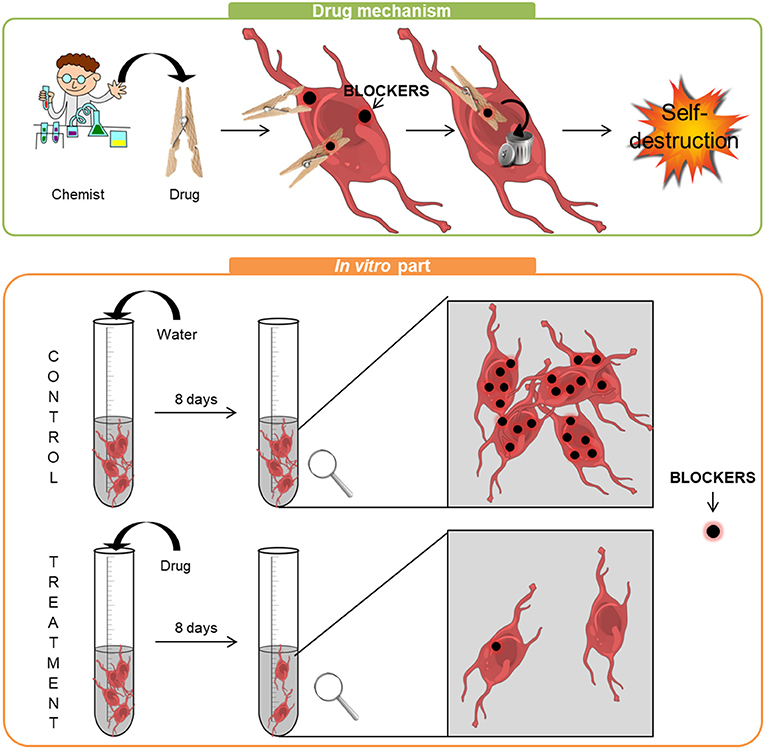
- איור 2 - פאנל עליון: האופן שבו התרופה פועלת הוא פשוט: היא תופסת את ה-BLOCKERS בתאים, כמו אטב, מה שמסייע לתאים להיפטר מה-BLOCKERS.
- כאשר ה-BLOCKERS נעלמו, תאי הסרטן ביצעו השמדה עצמית. פאנל תחתון: בניסויי in vitro תאי הסרטן טופלו באמצעות מים (ביקורת) או באמצעות תרופה (טיפול). אחרי 8 ימים הסתכלנו על התאים בפירוט. בסוף הניסוי מספר תאי הבקרה היה זהה כמו בתחילתו. אולם תאי סרטן רבים מתו בנוכחות התרופה, ואלה שנותרו הכילו פחות BLOCKERS.
בשלב השני ערכנו את הניסוי in vivo [3]. תרופות תמיד נבדקות על חיות לפני שהן נבדקות על בני אדם, וזה נקרא מחקר קדם-קליני. המחקר הקדם-קליני הוא שלב הכרחי בבדיקת תרופה חדשה. הדבר הראשון שצריך לבדוק, מאחר שרצינו שהתרופה תרפא מחלה מוחית, היה לוודא שהתרופה נכנסה אל המוח.
אתם ודאי יודעים שבגוף שלנו זורם דם שמספק לאיברים שלנו (כבד, ריאות, כליות וכד’) את כל מה שהם צריכים. לכן, אם תרופה מוזרקת לתוך הגוף אנו עשויים לחשוב שהיא תיכנס לתוך האיברים שלנו באופן טבעי. אולם לא כך המצב, הגוף שלנו הרבה יותר מורכב מזה. המוח מבוּדד ממחזור הדם באמצעות מה שנקרא מחסום דם-מוח, אשר מונע מווירוסים, לדוגמה, להגיע אל המוח. מחסום הדם-מוח יעיל מאוד בהגנה על המוח ממחלות חיצוניות כמו וירוסים, אולם הבעיה היא שהוא גם מונע מתרופות מסוימות להיכנס אל המוח. לכן, בדקנו אם התרופה החדשה שלנו קטנה מספיק כדי לחצות את מחסום הדם-מוח ולהגיע למוח, והיא אכן הייתה!
לאחר מכן, הניסוי הבא היה להזריק תאי גליובלסטומה לתוך מוחם של עכברים, בזמן שדואגים לרווחתם ומוודאים שהם לא סובלים. הכנסת התאים לתוך המוח הייתה תהליך כירורגי מדויק מאוד אשר דרש שהחיות יהיו ישנות. תאי הסרטן שהזרקנו היו מיוחדים, הם היו בצבע אדום פלורסצנטי! זה אִפשר לנו לראות אותם בזמן שהחיה התנהגה כרגיל. כמו בני אדם, גם העכברים התעוררו לאט אחרי הניתוח וחזרו בהדרגה לחיי היומיום שלהם.
שלוש קבוצות של שבעה עכברים התגבשו: קבוצת ביקורת (קבוצה 1); קבוצה שטופלה באמצעות מנה נמוכה של התרופה (קבוצה 2) וקבוצה נוספת שטופלה באמצעות מנה גבוהה יותר של התרופה (קבוצה 3).
כדי לדעת מה שלומם של העכברים בדקנו כל יום את משקלם ואת התנהגותם. הבדיקה התקופתית הזו אפשרה לנו למדוד את מספר הימים, השבועות או אפילו החודשים שבמהלכם העכברים חיו בלי לסבול מסרטן במוח.
האם התרופה החדשה הייתה יעילה במניעת גליובלסטומה?
התוצאות שלנו היו מבטיחות מאוד: קבוצת הביקורת חיה בממוצע במשך 25 ימים; הקבוצה השנייה חיה בממוצע 40 ימים והקבוצה השלישית חיה יותר מ-90 ימים. זה אמר לנו שהתרופה מאיטה את התפתחות הגידול ושהמינון הגבוה ביותר היה יעיל יותר, מה שאפשר לעכברים לחיות זמן רב יותר.
המידע החשוב שלנו הופק מתאי הסרטן שנצבעו בפלורסצנט אדום. הייתה לנו טכנולוגיה מיוחדת שאפשרה לנו לראות את התאים האדומים הפלורסצנטים דרך הגולגולת של העכברים, בלי לפגוע בהם. פעם בשבוע הסתכלנו על התפתחות סרטן המוח אצל כל העכברים. הבחנו בכך שכל שבעת העכברים שטופלו עם מים פיתחו סרטן, בעוד שרק חמישה עכברים מקבוצה 2 ושלושה עכברים מקבוצה 3 פיתחו סרטן מוח (איור 3). בקבוצת הביקורת הגידולים הופיעו בשבוע השני אחרי שתאי הסרטן הוזרקו, בעוד שהגידולים הופיעו רק בשבוע הרביעי בעכברים שטופלו באמצעות התרופה. מצאנו גם שהעכברים שטופלו באמצעות התרופה היו עם גידולים הרבה יותר קטנים מאשר הגידולים שהיו אצל עכברים שטופלו באמצעות מים בלבד (איור 3, חיצים לבנים). הניסוי הזה הראה שהתרופה הזו האיטה באופן משמעותי את התפתחות הסרטן אצל העכברים האלה. עם כל התוצאות האלה אנו יכולים לומר שהטיפול בחיות היה יעיל. לא היו תופעות לוואי שאותרו, אפילו במקרים של מינון התרופה הגבוה ביותר.
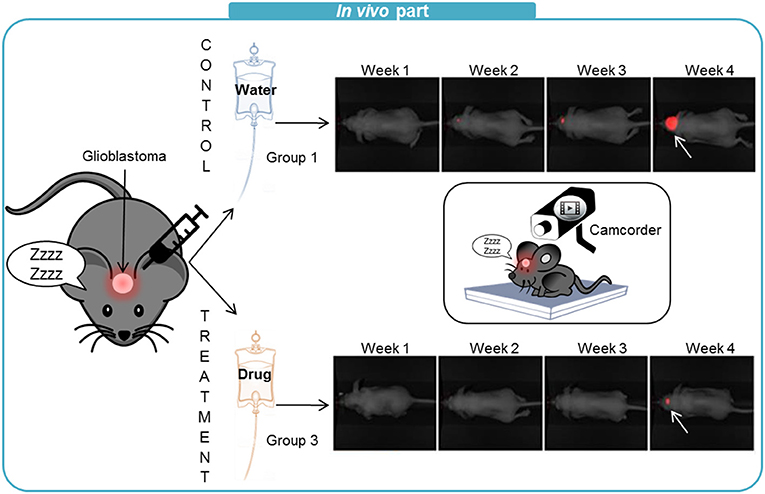
- איור 3 - בניסויי ה-in vivo השתמשנו בעכברים שהוזרקו אליהם תאי גליובלסטומה.
- כאן אנו מראים את התוצאות של עכברי קבוצה 1 (ביקורת) שטופלו באמצעות מים, ועכברי קבוצה 3 שטופלו באמצעות מינון גבוה של התרופה. פעם בשבוע צילמנו את העכברים באמצעות מצלמה מיוחדת שמאתרת את תאי הסרטן האדומים הפלורסצנטיים. החיצים הלבנים מצביעים על הגידולים ואתם יכולים לראות שהגידול הופיע מאוחר יותר ושהוא היה קטן הרבה יותר אצל עכברים שטופלו באמצעות התרופה.
מסקנות
המחקר הזה אפשר לנו להסיק שהתרופה שהשתמשנו בה היא מועמדת טובה לטיפול בסרטן מוח בבני אדם. אכן, היא נטרלה את ה-BLOCKRES וגרמה להשמדה עצמית של תאי סרטן. תוצאות טובות נראו אצל עכברים עם סרטן מוח, שם הטיפול התרופתי האט את התפתחות הסרטן, ועבור חלק מהעכברים התרופה אפילו מנעה מהם לפתח סרטן. הצעד הבא הוא לבחון את התרופה בשילוב עם טיפול קונבנציונלי במטרה לשלב את כל ההשפעות של התרופות ובתקווה, בעתיד, לרפא מטופלים עם גליובלסטומה.
מילון מונחים
אפופטוזיס (Apoptosis): ↑ אפופטוזיס (או מוות תאי מתוכנן) הוא תהליך שבו תאים מתחילים לבצע השמדה עצמית בתגובה לאות.
גליובלסטומה (Glioblastoma): ↑ גידול שמתפתח במוח. הוא נגרם על-ידי התרבוּת מהירה של תאים חולים במוח.
מעכבי אפופטוזיס (IAPs - Inhibitors of apoptosis): ↑ קבוצה של חלבונים שחוסמים מוות תאי מתוכנן שיכול באופן שכיח לגרום לסרטן.
מחסום דם-מוח (Blood-brain barrier): ↑ מחסום פיזיולוגי סלקטיבי במיוחד במוח, אשר מפריד בין זרימת הדם ובין מערכת העצבים המרכזית. הוא מגן על המוח מפני פתוגנים, רעלים והורמונים שזורמים בדם.
הצהרת ניגוד אינטרסים
המחברים מצהירים כי המחקר נערך בהעדר כל קשר מסחרי או פיננסי שיכול להתפרש כניגוד אינטרסים פוטנציאלי.
תודות
האיורים נוצרו תוך שימוש ברישיון Servier Medical Art under Creative Commons Attribution 3.0 Unported License.
עבודתי נתמכה על-ידי האגודה הצרפתית ARTC (האגודה למחקר על מדעי מוח).
אני מודה בחום לד"ר Céline Caravagna עבור עזרתה הרבה בכתיבת המאמר הזה.
מאמר המקור
↑ Tchoghandjian, A., Soubéran, A., Tabouret, E., Colin, C., Denicolaï, E., Jiguet-Jiglaire, C., et al. 2016. Inhibitor of apoptosis protein expression in glioblastomas and their in vitro and in vivo targeting by SMAC mimetic GDC-0152. Cell Death Dis. 7:e2325. doi: 10.1038/cddis.2016.214
מקורות
[1] ↑ Louis, D. N., Perry, A., Reifenberger, G., von Deimling, A., Figarella-Branger, D., Cavenee, W. K., et al. 2016. The 2016 World Health Organization Classification of Tumors of the Central Nervous System: a summary. Acta Neuropathol. 131:803–20. doi: 10.1007/s00401-016-1545-1
[2] ↑ Flygare, J. A. and Fairbrother, W. J. 2010. Small-molecule pan-IAP antagonists: a patent review. Expert Opin. Ther. Pat. 20:251–67. doi: 10.1517/13543770903567077
[3] ↑ Tchoghandjian, A., Soubéran, A., Tabouret, E., Colin, C., Denicolaï, E., Jiguet-Jiglaire, C., et al. 2016. Inhibitor of apoptosis protein expression in glioblastomas and their in vitro and in vivo targeting by SMAC mimetic GDC-0152. Cell Death Dis. 7:e2325. doi: 10.1038/cddis.2016.214