תַקצִיר
תסמונת ויליאמס היא תסמונת נוירו-התפתחותית המאופיינת על ידי חברתיות-יתר ותסמינים נוירו-קוגניטיביים ייחודיים. אחד המאפיינים בתסמונת זו הוא התנהגות חברתית מוגברת. אנשים בעלי תסמונת זו עשויים להיות חברתיים יתר על המידה גם כלפי זרים. ביצענו מחקר חדשני במעבדתנו אשר מציג כי חוסר בגֶן Gtf2i עשוי למלא תפקיד בתסמונת ויליאמס. כאשר ישנו חסר בגן זה גילינו כי אחד ממרכיבי המוח החשובים ביותר להעברת אותות במוח נפגע, ומוביל להפרעה בשליחת האותות במוח אשר ככל הנראה גורמת לחברתיות-יתר שנצפית בתסמונת ויליאמס. אנו חושפים מנגנונים מפתיעים המעורבים בהתנהגות חברתית מוגברת אשר מהווה אחד המאפיינים של תסמונת ויליאמס.
במאמר זה אנו מדגימים כיצד תרופות שונות מפצות על המרכיב אשר נפגע, ומובילות להפחתת ההתנהגות החברתית המוגברת עד לרמת הנורמה.
מהי תסמונת ויליאמס?
דמיינו שאתם הולכים ברחוב ולפתע נתקלים באדם מסוכן. סביר להניח שתיבהלו, תעברו לצד השני של הרחוב ואף תזעיקו משטרה. ובכן, אדם בעל תסמונת ויליאמס היה ככל הנראה כה נרגש למראה פניו של אדם זר עד שייתכן ולא היה מבחין שהזר הזה מסוכן. בעלי תסמונת ויליאמס מתוארים כבעלי אישיות חברתית באופן בלתי רגיל, רגישים ואמפתיים במיוחד, ולכן גם נוצר הכינוי המתאר אותם “ילדי האהבה”.
תסמונת ויליאמס היא תסמונת גנטית הנגרמת כתוצאה ממחיקת עותק אחד מתוך שני העותקים של כ-26 גֶּנִים המצויים על כרומוזום 7 בבני אדם [1]. התסמינים הפיזיים המופיעים בה כוללים כשלים במערכת הלב וכלי הדם; בעיות הורמונליות ותווי פנים ייחודיים [1]. התסמינים ההתנהגותיים של התסמונת כוללים חברתיוּת יתר; אמפתיה מוגברת (היכולת להבין את רגשות האחר); הפרעות קוגניטיביות (שכליות); כישורי שפה גבוהים; יכולת לקויה לזיהוי סכנות הקשורות למצבים חברתיים ורמות גבוהות של חרדה לא-חברתית (חרדה שאינה קשורה למצבים חברתיים).
כבר שנים שמדענים מנסים לפצח מהו המנגנון שעומד מאחורי תסמונת ויליאמס [2, 3] במחקרים קודמים גילו שאחד מהגנים הנמחקים בתסמונת – Gtf2i – נקשר בעבר כאחראי לחברתיות היתר בתסמונת ויליאמס[3]. אולם המנגנון העומד מאחורי השפעת גן זה על חברתיות לא הובן בצורה מספקת עד לאחרונה.
תפקיד הגן Gtf2i בתסמונת ויליאמס
גנים שונים מבוטאים בסוגי תאים שונים, ומדענים מסוגלים להשתיק גן מסוים על ידי מחיקתו מתא מסוים, או מכל הגוף. במחקר זה מחקנו את הגן Gtf2i באופן מכוון בתאי עצב במוח הקדמי של עכברים. מצאנו שעכברי המודל בעלי המחיקה של Gtf2i הראו התנהגויות חריגות המזוהות עם תסמונת ויליאמס, כולל פגמים במבנה המוח; ליקויים במוטוריקה עדינה ורמות מוגברות של חברתיות וחרדה לא-חברתית (איור 1).
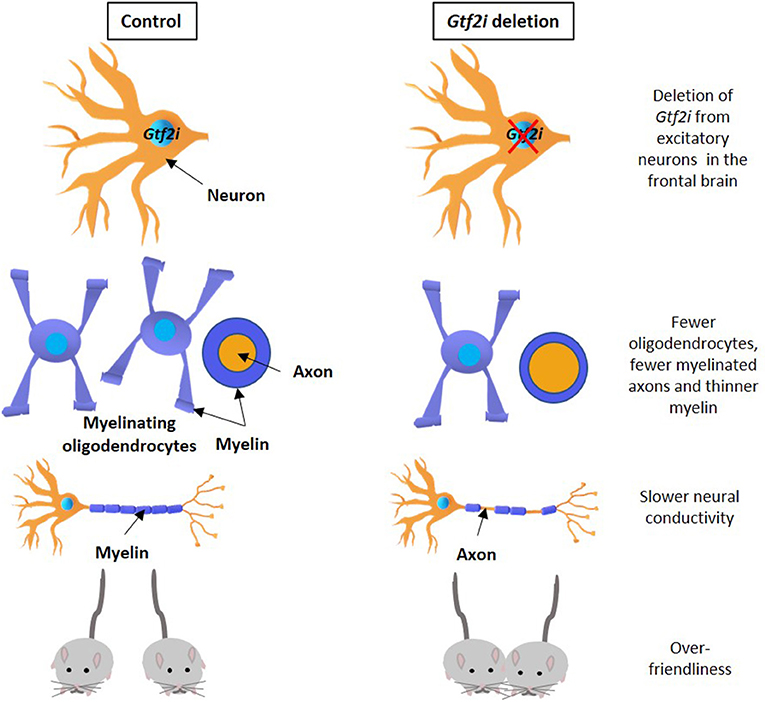
- איור 1 - מחיקת הגן Gtf2i ותוצאותיה.
- מחיקת הגן Gtf2i בתאי עצב במוח הקדמי של עכבר והפגיעות הנובעות מכך, חלקן דומות לפגיעות האופייניות לתסמונת ויליאמס (מימין), בהשוואה לעכברי ביקורת (משמאל). הפגיעות הן: פחות אוליגודנדרוציטים, פחות אקסונים עטופים מיאלין ושכבת מיאלין דקה יותר (שורה שנייה), הולכה עצבית נמוכה יותר (שורה שלישית) וחברתיות יתר (שורה תחתונה). עוּבּד מתוך [4].
באמצעות ניסויים שונים מצאנו קשר ישיר בין מחיקת הגן Gtf2i בעכברים לבין בעיות בחומר הנקרא מִיאָלִין. המיאלין הוא שכבה שומנית העוטפת ומבודדת את שלוחות תאי העצב, הנקראות אַקְסוֹנִים. ללא מיאלין, האות החשמלי עובר באקסון באופן בלתי תקין ונוצר פגם במערכת העצבים המרכזית, מה שמוביל לבעיה תפקודית שיכולה להתבטא למשל בהתנהגות לקויה. הגילוי הזה, אשר מראה השפעה של מחיקת הגן Gtf2i על המיאלין, פותח צוהר חדש למציאת טיפולים חדשים לתסמונת ויליאמס.
תוצאות
מחיקת Gtf2i בתאי עצב במוח הקדמי גורמת לשינויים מבניים והתנהגותיים
הלוקים בתסמונת ויליאמס מראים ירידה בנפח המוח ובמבנה של קליפת המוח (השכבה החיצונית של המוח). על כן, רצינו לבדוק אם מחיקה של הגן Gtf2i בלבד מתאי עצב במוח הקדמי מספיקה כדי לגרום לחריגות מבניות כאלה. משקל המוח ועובי קליפת המוח של עכברי מודל בני חודש היו נמוכים באופן משמעותי בהשוואה לעכברי ביקורת (עכברים “בריאים”, ללא פגיעה גנטית כלשהי).
נוסף לכך עכברי המודל שלנו הראו רמות גבוהות יותר באופן משמעותי של התנהגות חברתית, אותה הערכנו בשלושה מבחנים. עכברי המודל, ללא Gtf2i, יצרו אינטראקציות קרובות עם בני מינם בתדירות גבוהה ולמשך זמן ארוך יותר בהשוואה לעכברי הביקורת. יש אף לציין כי עכברי מודל העדיפו ליצור יותר אינטראקציות עם עכבר זר מאשר עם עצם דומם בהשוואה לעכברי הביקורת, עם Gtf2i. פירשנו את התנהגות עכברי המודל כהעדפה לביצוע התנהגות חברתית מוגברת.
כמו כן, מאחר שאחד המאפיינים המזוהים עם תסמונת ויליאמס הוא רמות גבוהות של חרדה לא-חברתית, בחנו את העכברים לגבי התנהגויות הקשורות לחרדה. בעכברי המודל מצאנו רמות גבוהות משמעותית של חרדה אשר לא קשורה בחברתיות בהשוואה לעכברי ביקורת. נתונים אלה דומים לכמה תסמיני ליבה שנמצאו בעבר בקרב הלוקים בתסמונת ויליאמס.
מחיקה של Gtf2i מתאי עצב משפיעה על מיאלין וגנים נוספים הקשורים למיאלין
באופן מפתיע, על אף שמחקנו את הגן Gtf2i מנוירונים בלבד, מצאנו שגנים נוספים הושפעו. אנו חושדים שגנים אלה השתנו כתוצאה ממחיקת החלבון Tfii-i אשר נוצר על ידי הגן Gtf2i (איור 2) ומעורב בבקרה על פעילותם של גנים שונים. באופן מפתיע, 70% מהגנים אשר רמתם ירדה באופן משמעותי בקליפת המוח של עכברי מודל בני חודש היו מעורבים בהתפתחות המיאלין ותפקודו. כמו כן, גנים אלה מקודדים לחלבונים המעורבים בהתפתחות ותפקוד של אוליגודנדרוציטים, שהם תאים המייצרים מיאלין. מצאנו גם כי מספרם של האוליגודנדרוציטים פחת משמעותית בקליפת המוח של עכברי המודל בהשוואה לעכברי הביקורת.
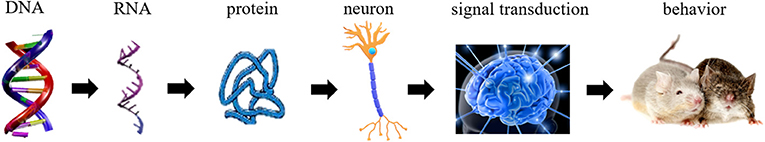
- איור 2 - שרשרת התהליכים במוח אשר משפיעה לבסוף על התנהגות.
- הגנים ב-DNA משועתקים ל-RNA אשר עובר תרגום לחלבונים. החלבונים משפיעים על פעילות תאי המוח בהם תאי עצב, ובכך משפיעים על העברת האותות במוח. הצורה שבה מידע מועבר במוח משפיעה על התנהגות.
מחיקה של Gtf2i גורמת לפגמים במבנה המיאלין, בהולכה העצבית ובכישורים המוטוריים
בניתוח מבנה המיאלין ראינו אחוז נמוך יותר משמעותית של אקסונים עטופים במיאלין, ושכבת מיאלין דקה יותר משמעותית בקרב עכברי המודל בהשוואה לעכברי הביקורת. כתוצאה מהפגמים בשכבת המיאלין, גם ההולכה העצבית במוח עכברי המודל נפגעה משמעותית בהשוואה לעכברי הביקורת.
נוסף על כך אנשים בעלי תסמונת ויליאמס מבטאים חסכים במוטוריקה עדינה. עכברי המודל הראו חוסר שליטה על תנועות רצוניות עדינות, עם טוֹנוּס שרירים חלש יותר בגפיים הקדמיות והאחוריות בהשוואה לחיות הביקורת. כלומר, הפגמים במיאלין אכן פגעו ביכולתם המוטורית של עכברי המודל.
תיקון הפגמים במיאלין ובמוליכות העצבית משפר ליקויים התנהגותיים ועצביים
כתוצאה מהפגיעה במיאלין ראינו שעכברי המודל מראים הולכה עצבית לקויה. ישנהּ תרופה בשם 4-AP, הידועה בכך שהיא משפרת הולכה עצבית. נתנו לעכברי מודל ולעכברי ביקורת את התרופה הזו במטרה לבחון אם עכברי המודל יראו שיפור בהולכה העצבית וכתוצאה מכך בהתנהגות המוטורית והחברתית שלהם. מצאנו כי מתן חד-פעמי של 4-AP הוביל לתיקון הכישורים המוטוריים העדינים בעכברי המודל. כמו כן, עכברי המודל הראו העדפה חברתית תקינה במבחן ההעדפה החברתית. על כן מצאנו שטיפול ב-4-AP נִרְמֵל את המוליכות העצבית, וכתוצאה מכך השתפרו התנהגויות חברתיות ומיומנויות מוטוריות בעכברי המודל (איור 3).
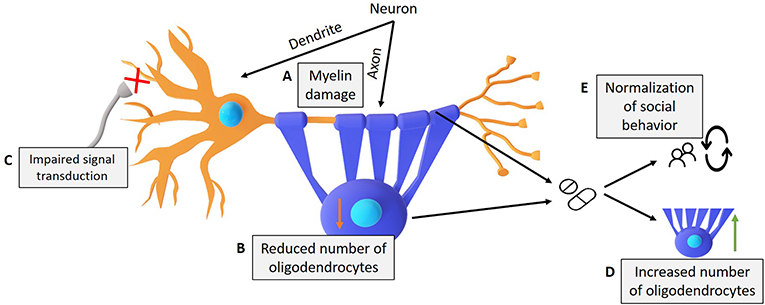
- איור 3 - תיאור הפגיעות אשר מתרחשות בתסמונת ויליאמס ותרופות אשר נוסו כדי לתקנן במודל העכברי.
- (A) מחיקת הגן Gtf2i מתאי עצב מביאה לפגיעות בשכבת המיאלין (B) ובמספר האוליגודנדרוציטים (C), וזה מוביל לפגיעה במעבר האות החשמלי. (D) הראינו כי קלמסטין מביאה לעלייה במספר האוליגודנדרוציטים ותיקון ההתנהגות החברתית (E), והתרופה 4-AP הביאה לשיפור בהולכת הסיגנל ותיקון ההתנהגות החברתית בעכברי המודל בהשוואה לעכברי הביקורת.
נוסף על כך רצינו לבדוק אם תיקון הפגמים במיאלין עצמו מספיק כדי לשפר את הליקויים החברתיים. כדי לבדוק זאת, נתנו באופן כרוני תרופה בשם קלמסטין לעכברי מודל בני חודש. טיפול בקלמסטין הביא לנורמה את מספר האוליגודנדרוציטים בקליפת המוח, והגדיל את עובי שכבת המיאלין בעכברי המודל (איור 3). מצאנו אף כי תיקון הפגמים בתהליך יצירת המיאלין הספיק כדי לתקן את ההעדפה החברתית המוגברת.
הפגמים אשר נמצאו בעכברי המודל אושרו גם בדגימות מוח של בני אדם עם תסמונת ויליאמס.
כדי לבדוק אם ממצאי מחקר זה אודות פגמים במיאלין בעכברים תקפים גם באנשים אשר לוקים בתסמונת ויליאמס, חקרנו דגימות מקליפת מוח קדמי של אנשים עם תסמונת ויליאמס אשר תרמו את מוחם למדע, והשווינו אותן לקבוצת ביקורת. בדומה לפגמים שמצאנו בעכברי המודל, מצאנו גם מספר אוליגודנדרוציטים נמוך משמעותית, ירידה חדה בעובי שכבת המיאלין ומגמה של אחוז מופחת של אקסונים בעלי שכבת מיאלין בקליפת המוח הקדמי של הלוקים בתסמונת ויליאמס, בהשוואה לקבוצת הביקורת.
כמו כן, מצאנו כי 19% מכלל הגנים שרמתם השתנתה באופן משמעותי (עלתה או ירדה) בקרב הלוקים בתסמונת ויליאמס, בהשוואה לקבוצת הביקורת, הם גנים הקשורים למיאלין. רבים מהגנים הללו הם אותם גנים שהושפעו בעכברי המודל במחקר הנ“ל.
מסקנות
על ידי מחיקת Gtf2i באופן סלקטיבי מתאי עצב בעכברים, מצאנו באופן בלתי צפוי הפחתה דרמטית בביטוי הגנים הקשורים למיאלין, במספר האוליגודנדרוציטים ובהולכה העצבית. נוסף על כך קיבלנו תוצאות דומות גם ברקמות אנושיות מאנשים אשר לקו בתסמונת ויליאמס. יחד, נתונים אלה מצביעים על כך שפגיעה במיאלין מהווה תפקיד חשוב בתסמונת ויליאמס, ושמחיקת Gft2i מנוירונים היא ככל הנראה הגורם לפגיעה זו. מחקר זה מזהה תפקיד חשוב של ביטוי Gtf2i בתאי עצב, תפקיד הכרחי להתפתחות אוליגודנדרוציטים ושמירה על תנאי מיאלין תקינים, וכי חוסר בגן זה עלול לתרום לחלק מהתסמינים הקשורים לתסמונת ויליאמס.
מחקר זה שופך אור על אופן השפעת המיאלין וההולכה העצבית על התנהגות חברתית בתסמונת ויליאמס, ולכן יכול להקל על פיתוח אסטרטגיות טיפול חדשות להפרעות התנהגותיות. כיוון שיעילות ומהירות המוליכות העצבית נשענות על מיאלין, ליקויים בתכונות המיאלין עשויים להשפיע על תקשורת וסנכרון תקין בין אזורי מוח שונים החיוניים לביצוע התנהגויות תקינות. לכן, התמקדות בתיקון ליקויי מיאלין עשויה להיות אסטרטגיה טיפולית מועילה בתסמונת ויליאמס.
מילון מונחים
Gtf2i: ↑ גן הנמחק באנשים בעלי תסמונת ויליאמס, ומחיקתו נקשרה להפרעות החברתיות בתסמונת.
תא עצב (נוירון): ↑ תא שתפקידו לקלוט אות חשמלי (סִיגְנָל) ולהעביר את המידע שבו לתא העצב הבא.
אקסון (Axon): ↑ שלוחת תא העצב שמוליכה את הסיגנל לתא הבא.
מיאלין (Myelin): ↑ שכבה שומנית העוטפת את האקסון במטרה לשמור על מעבר סיגנלים מהיר ויעיל (ממש כמו חומר מבודד שעוטף כבל חשמל).
עכברי מודל (Model Mice): ↑ עכברים שהונדסו גנטית במטרה להוות מודל למחלה אנושית מסוימת.
עכברי ביקורת (Control Mice): ↑ עכברים שאינם נושאים מוטציה גנטית מסוימת, ואליהם משווים את עכברי המודל.
אוליגודנדרוציט (Oligodendrocyte): ↑ תא האחראי על ייצור מיאלין במוח.
הולכה עצבית (Neural Conductivity): ↑ הצורה שבה אותות נשלחים לאורך האקסונים של תאי העצב.
הצהרת ניגוד אינטרסים
המחברים מצהירים כי המחקר נערך בהעדר כל קשר מסחרי או פיננסי שיכול להתפרש כניגוד אינטרסים פוטנציאלי.
תודות
בכתיבת מאמר זה לקחו חלק נועה שוכמן ורועי שמש, צעירים יוצאי-דופן אשר פעלו רבות כדי לעבד את המאמר המקורי ולערוך אותו כך שיתאים לכל אחד ואחת.
נועה ורועי לקחו חלק פעיל בפרויקטים שונים במעבדתו של ד”ר בועז ברק כחלק מתוכנית אלפא של אוניברסיטת תל אביב לנוער. נועה, בת 17, לומדת בתיכון “אהל שם” ברמת גן במגמות כימיה וביוטכנולוגיה, הצטרפה לתוכנית אלפא מתוך סקרנות ורצון ללמוד על המוח, על אופן הפעולה שלו ובפרט על מחלות ותסמונות שמשפיעות על המוח. רועי, בן 16 מפתח תקווה, לומד בכיתת מחוננים בתיכון “אחד העם” באם המושבות. הצטרף לתוכנית אלפא מתוך אהבה גדולה לביולוגיה וחֵקֶר גוף האדם.
נועה ורועי, אנו מודים לכם מקרב לב ומאחלים המון הצלחה בהמשך.
תודה רבה!
מאמר המקור
↑ Boaz, B., Zhang, Z., Liu, Y., Nir, A., Trangle, S. S., Ennis, M., et al. 2019. Neuronal deletion of Gtf2i, associated withWilliams syndrome, causes behavioral and myelin alterations rescuable by a remyelinating drug. Nat. Neurosci. 22:700–8. doi: 10.1038/s41593-019-0380-9
מקורות
[1] ↑ Pober, B. R. 2010. Williams-Beuren syndrome. N. Engl. J. Med. 362:239–52. doi: 10.1056/NEJMra0903074
[2] ↑ Morris, C. A., Kimberley, K. W., and Stock, A. D. 2003. GTF2I hemizygosity implicated in mental retardation in Williams syndrome: genotype-phenotype analysis of five families with deletions in the Williams syndrome region. Am. J. Med. Genet. A 123A:45–59. doi: 10.1002/ajmg.a.20496
[3] ↑ Barak, B., and Feng, G. 2016. Neurobiology of social behavior abnormalities in autism and Williams syndrome. Nat. Neurosci. 19:647–55. doi: 10.1038/nn.4276
[4] ↑ Osso, L. A., and Chan, J. R. 2019. A surprising role for myelin in Williams syndrome. Nat. Neurosci. 22:681–3. doi: 10.1038/s41593-019-0368-5
