תַקצִיר
מערכת החיסון מגינה עלינו ונלחמת במיקרואורגניזמים רבים כגון נגיפים הגורמים להצטננות הנפוצה או חיידקים החודרים לפצעים. מערכות ההגנה שלנו יכולות גם ללמוד להגן עלינו במצבים מסובכים יותר, והן יכולות לעשות זאת בעזרת מה שלמדו מהחיסונים. למשל, החיסון לנגיף הפוליו מלמד את מערכת החיסון לזהוֹת את נגיף הפוליו ולחסלו, במקרה שזה יחדור לגוף. בשנים האחרונות גילו מדענים שאפשר גם ללמד את מערכת החיסון לתקוף מחלה מסוג אחר: סרטן. מחלת הסרטן היא טעות גדולה בגוף שלנו. זה קורה כאשר תאים מאבדים את הבקרה שלהם ומתחילים להתרבוֹת ללא הגבלה. החדשות הטובות הן שאנו יכולים ללמד את מערכת החיסון של חולי סרטן – לזה קוראים אִימוּנוֹתֶרַפְּיָה. במאמר זה אנו מסבירים איך מערכות ההגנה שלנו יכולות ללמוד לתקוף את הסרטן ולחסלו.
סרטן: כאשר הגוף מאבד את הבקרה
מחלת הסרטן היא מחלה רצינית התוקפת אנשים רבים. ייתכן שאנו מכירים אנשים סביבנו אשר מנהלים מלחמה ארוכה וקשה עם מחלת הסרטן, ולבסוף הם עלולים למות. אולם לא כל מחלות הסרטן זהוֹת. קיימות צורות שונות של סרטן, ולא כולן גורמות בהכרח למוות. מידת החומרה של המחלה תלויה מאוד בסוג הסרטן, בטיפול שניתן ובעיקר – בשלב שבו אובחנה מחלת הסרטן.
מהי מחלת הסרטן? מקורה של מילה זו במילה היוונית “קארקינוס”, שפירושה “סרטן”. אומרים שבתקופה העתיקה הרופא היווני היפוקרטס היה הראשון שהשווה את המחלה הזו לסרטן, שֶׂכֵּן הוא ראה שהחלקים הפגועים בגוף של החולים היו קשים כסלע, גרמו לכאב כמו צביטה של סרטן ויכלו לחדור לאזורי גוף נוספים. בביולוגיה, מחלת הסרטן היא טעות גדולה. תאים מתחילים להתרבות בגוף ללא בקרה. מתחילת ההיריון כל חלק בגוף גדֵל ומתפתח תחת בקרה קפדנית. בקרה זו מעצבת את האצבעות שלנו; את העצמות; את המוח ואת כל האיברים שלנו. סוג התאים הסרטניים המתפתחים בגוף החולה תלוי בסוג התאים שעושים טעות ומאבדים את הבקרה שלהם. למשל, יש סרטן של המוח (נוירובלסטומה); סרטן של העצמות (אוסטאוסרקומה); או סרטן של תאי הפיגמנט שבעור הנקראים מלנוציטים (מלנומה). לעיתים קרובות הסיבה לסרטן אינה ידועה או שהיא נובעת מריבוי של טעויות מצטברות. לפעמים אנו יודעים מדוע מופיע הסרטן – יש דברים מסוימים הפוגעים בגוף ומְפֵרִים את מנגנון הבקרה. למשל, עשן סיגריות עלול לגרום לסרטן הריאות, וחשיפה רבה מדי לשמש עלולה לגרום לסרטן העור.
אימונותרפיה: הטיפול החדש נגד סרטן
ישנן אפשרויות רבות לטיפול במחלת הסרטן. אפשרויות אלה כוללות ניתוח, כאשר התאים הסרטניים נמצאים במקום שהמנתחים יכולים לחתוך בבטחה; ריפוי בעזרת קרינה (רדיותרפיה); או ריפוי בעזרת חומרים כימיים (כימותרפיה). באיזה טיפול נבחר עבור חולה נתון? הבחירה תלויה בכמה דברים כגון סוג הסרטן והשלב שבו המחלה נמצאת (כלומר עד כמה איבוד הבקרה וריבוי התאים הסרטניים נמצאים בשלב מתקדם).
בשנים האחרונות גילו מדענים יותר ויותר הוכחות לכך שגם מערכות ההגנה שלנו – מערכת החיסון – יכולות לתקוף את הסרטן. ריפוי המבוסס על מערכת החיסון שלנו נקרא אימונותרפיה. אימונותרפיה מתבססת בעיקר על סוג ייחודי מאוד של תאי דם לבנים הנקראים תאי T ציטוֹטוֹקסיים, ואופן פעולתם מתואר בסעיפים הבאים.
תאי T ציטוטוקסיים יכולים לחסל את הסרטן ולסייע לחולים
תאי T הם הכוחות המיוחדים של מערכת החיסון שלנו. כמו המשטרה, תאי T מסיירים בגוף כדי למצוא פולשים מזיקים (איור 1A). כל תא T מצויד ברדאר מיוחד הנקרא קולטן של תא T (TCR), שמאפשר לתא לזהוֹת פולש מסוים אחד. קולטנים של תאי T קובעים אם תאי הגוף בריאים על-ידי בדיקת זהותם (ID), המתאפשרת על-ידי מולקולה הנקראת MHC (בתרגום חופשי מאנגלית: המערך הראשי של התאמת רקמות). כל תא בגוף טוען פיסות מעצמו על ה־MHC שלו, וכך מציג תמונה כללית של זהותו כאשר הוא באינטראקציה עם קולטן של תא T.
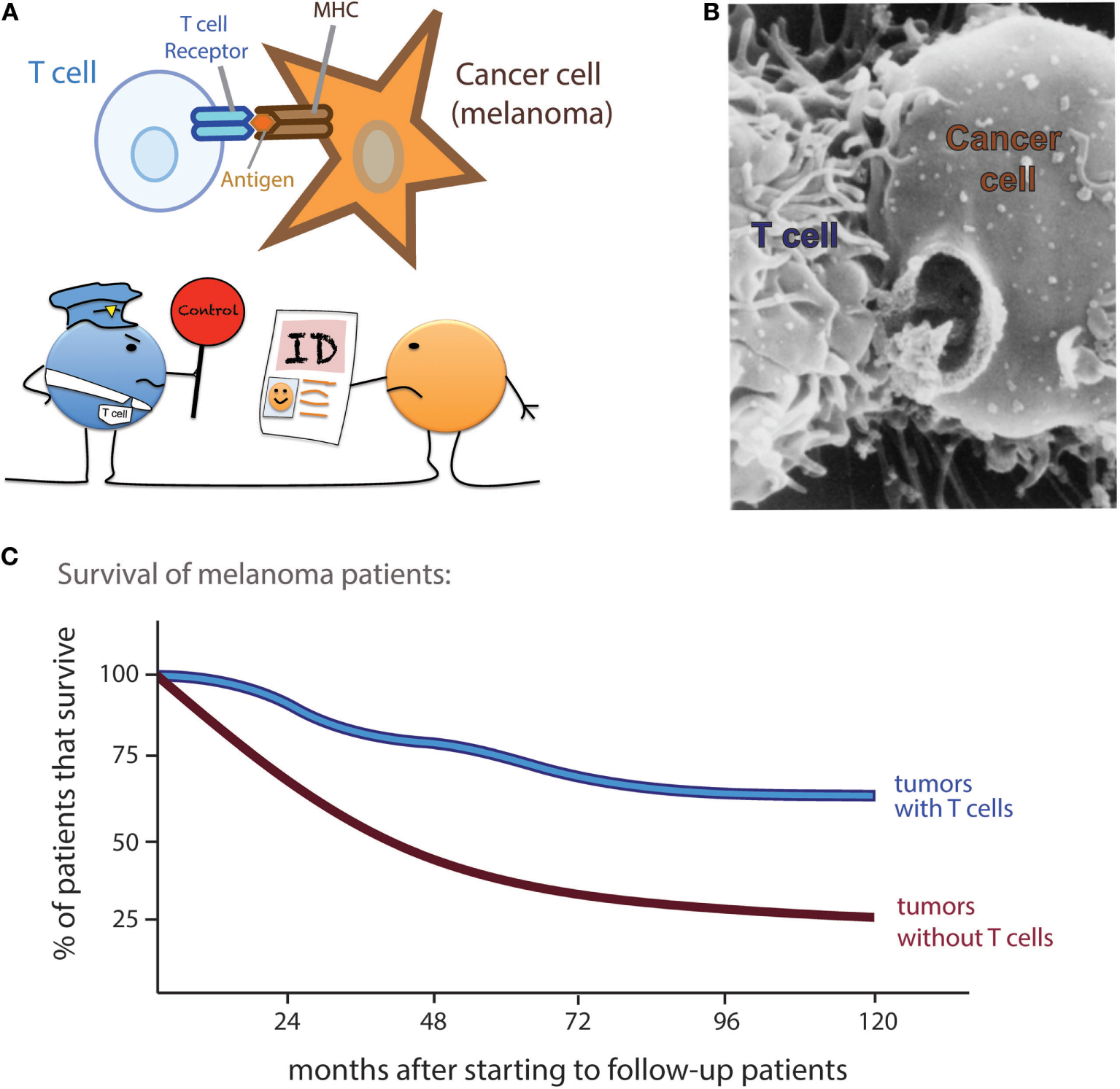
- איור 1 - תאי T יכולים לגלות תאים סרטניים ולהרוג אותם, ובכך לעזור לחולים לשרוד למשך זמן ארוך יותר.
- A. לתאי T יש קולטנים ייחודיים של תאי T. תא מציג את זהותו (ID) על-ידי הצגת פיסות מעצמו (אנטיגנים) על ה-MHC. תא סרטני (מלנומה, נראה ככוכב באיור) מציג זהות שחל בה שינוי, דבר הגורם להפעלת תאי T. B. תמונה אמיתית של תא T שיוצר חור בתא סרטני. צולם בעזרת מיקרוסקופ אלקטרונים (נלקח ברשות מ־http://lib.jiangnan.edu.cn/ASM/350-Introduce.htm). C. כאשר רופאים ביצעו מעקב אחר החולים שלהם, התגלה כי חולים שבגידולים שלהם נמצאו תאי T (קו כחול) שרדו למשך זמן ארוך יותר לעומת חולים שבגידולים שלהם לא נמצאו תאי T (קו שחור) (נתונים אלה נלקחו ממחקר על חולי מלנומה [1]).
פיסות תא אלה נקראות אנטיגנים כי הן יכולות לחולל תגובת חיסון (אנטי – נגד, גֶן – לחולל) כאשר תאי T מגיבים להן. נוסף על רדאר TCR, לתאי T יש גם כלי נשק לחיסול פולשים: תאי T יכולים להיות ציטוטוקסיים (פירוש המילה היוונית “ציטוס” הוא תא), כלומר הם יכולים להרוג תאים. כאשר הם מסיירים בגוף, תאי T מוודאים שהגוף בריא על-ידי בדיקת הזהוּת של תאי הגוף (איור 1A). אם תא נגוע וחולה הוא יציג את ה־MHC שלו עם פיסות של המיקרואורגניזם הפוגע, והדבר יגרום לשינוי הזהות שלו, ויגרום לו להיראות זר. כאשר תא T מגלה שינוי כזה בזהות, הוא מופעל והורג את התא החולה, כולל הפולש שבתוכו. כך נמנעת התפשטות הפולש לשאר הגוף.
כיצד תא T הורג תא חולה? דמיינו זאת כמו ניקוב חור בבלון מים (איור 1B). כלי הנשק של תאי T הם חומרים הנקראים פֶּרְפוֺרינים, היוצרים חורים ומפרישים אנזימים הגורמים להֶרֶס כללי בתוך התא המותקף.
כך תאי T מזהים פולשים ומחסלים אותם. אבל, תאים סרטניים אינם חיידקים פולשים – אלה הם תאים חולים שמתפתחים מתאי גוף תקינים עקב טעויות בגידול ובהתפתחות שלהם. בדרך כלל, תאי T אינם רואים שתאים סרטניים מזיקים לגוף כי תאים סרטניים אינם פולשים לגוף מבחוץ. למרבה המזל, יש יוצאי דופן לכלל פלישה זה – תאים סרטניים מתנהגים בצורה מחשידה מאוד, ומציגים זהות של תא חולה ששונה מתאים בריאים. אז, תאי T יכולים לזהות את התאים הסרטניים החולים הללו ולהרוג אותם.
כיצד אנו יודעים כי תאי T יכולים להילחם בסרטן? מדענים שמו לב לכך שחולי סרטן שאצלם תאי T מופעלים שורדים למשך זמן ארוך יותר. בהשוואת הגידולים של חולי סרטן רבים נמצא כי חולים שבגידול שלהם נמצאים תאי T רבים שורדים למשך זמן ארוך יותר לעומת חולים שבגידול שלהם אין תאי T (איור 1C) [1]. אם כך, קיום הסיורים של תאי T הוא יתרון גדול עבור חולי סרטן שֶׁכֵּן תאי T רואים את התאים הסרטניים ונכנסים אל תוך הגידולים כדי להרוג את התאים החולים.
אימונותרפיה יכולה ללמד תאי T לזהוֹת את הסרטן, ותאי T יזכרו זאת למשך שנים רבות!
מדוע אצל חולי סרטן מסוימים יש סיורים מוצלחים של תאי T שיכולים להרוג תאים סרטניים חולים, בעוד שבחולים אחרים אין? זו שאלה שעדיין נחקרת רבות. החדשות הטובות הן שמדענים מצאו שיטות ללמד את מערכת החיסון לזהות את הסרטן וללמד את תאי T לחסל את הגידולים גם בחולים שאצלם אין תאי T מוצלחים מלכתחילה. סוג זה של ריפוי, המבוסס על לימוד מערכת החיסון להילחם במחלה, נקרא אימונותרפיה.
היתרון הגדול באימונותרפיה הוא לא רק שהיא מלמדת את מערכת החיסון להילחם בסרטן פעם אחת אלא גם תאי T זוכרים זאת, ולמשך שנים רבות! ללמד תאי T להילחם בסרטן דומה לשימוש בחיסונים כדי ללמד תאי T להילחם בזיהומים חיידקיים. חיסונים הם חומרים המחוללים תגובת חיסון ייחודית נגד מחלה נתונה. בדרך כלל הם עשויים מחלק של החיידק הגורם למחלה בלבד, או מגִרְסָה של החיידק לאחר שינויו. למשל, החיסון נגד שיתוק ילדים (מחלה הנגרמת מנגיף הפוליו) מיוצר על-ידי הֲכָנַת צורה בלתי פעילה (מומתת) של נגיף הפוליו עצמו. כאשר נגיף פוליו בלתי פעיל זה מוזרק, הוא אינו יכול להדביק במחלה כי הוא מת. למרות זאת מערכת החיסון רואה את נגיף הפוליו ולומדת לזהות אותו. ברגע שאנו מחוסנים, אם אי פעם נידבק בנגיף הפוליו מערכת החיסון תזכור ותגיב מהר, ותחסל את נגיף הפוליו בטרם יתרבה בגוף ויגרום למחלה. יכולת זו של מערכת החיסון ללמוד ולזכור מה צריך להיות מחוסל נקראת זיכרון חיסוני.
בדיוק כפי שחיסון יכול ללמד את מערכת החיסון לחסל נגיף מסוים, אנו יכולים להשתמש באימונותרפיה כדי ללמד את מערכת החיסון להילחם טוב יותר במחלת הסרטן. אפשר להזריק לחולים טיפולים אימונותרפיים שילמדו תאי T מסוימים להתרבות ולתקוף את התאים הסרטניים (איור 2A). ברגע שהסרטן סולק, תאי T המסוימים יירגעו ויישארו בגוף החולה בצורת תאי זיכרון מסוג T (איור 2B). תאי זיכרון מסוג T אלה ימשיכו לסייר בגוף. אם אי פעם הם ייתקלו באותם תאים סרטניים שוב, אפילו במרחק או במקום אחר בגוף (מַעֲבָר של תאים סרטניים ידוע בשם מטאסטאזיס), תאי הזיכרון מסוג T יזכרו את הסרטן הזה ויופעלו מחדש במהירות כדי לתקוף אותו (איור 2C).
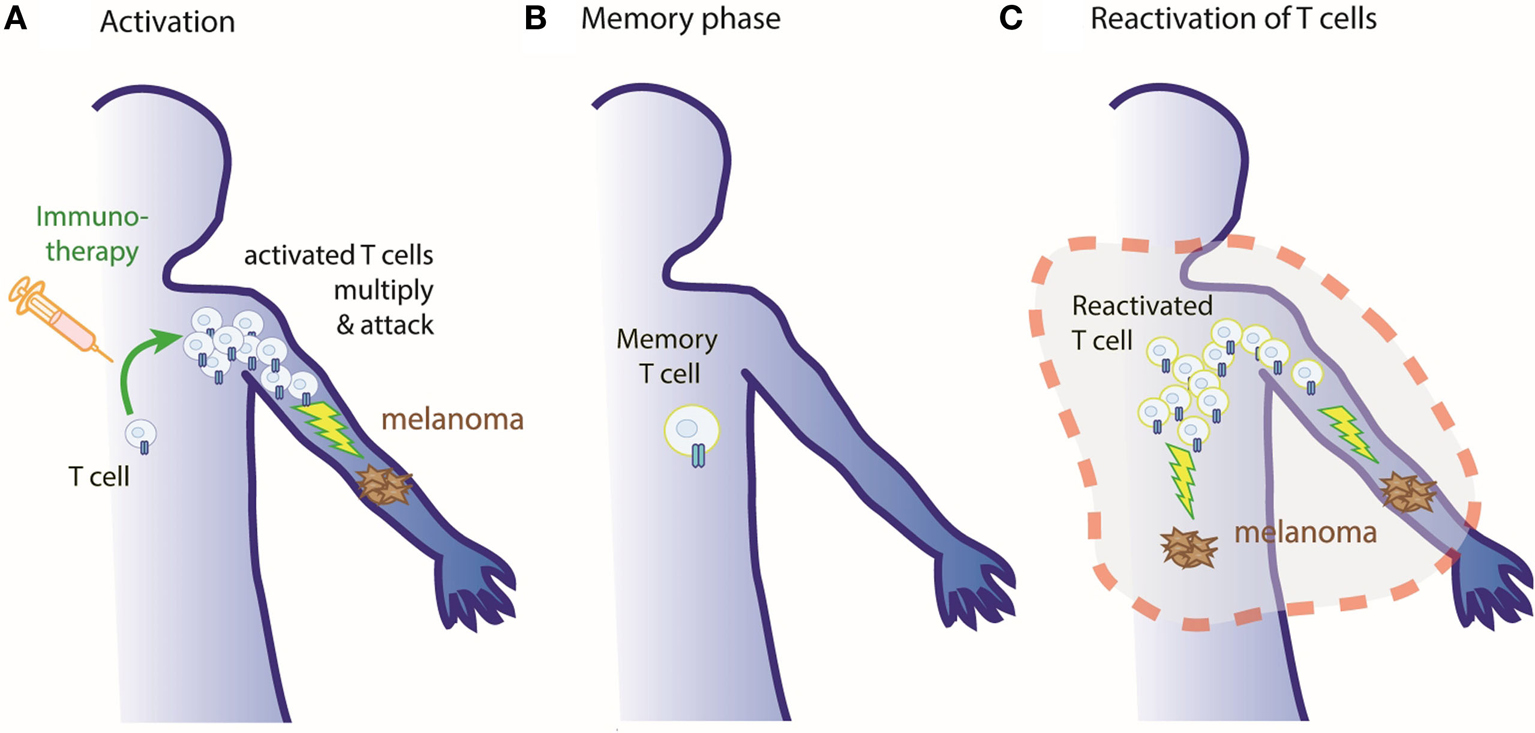
- איור 2 - מערכת החיסון שלנו זוכרת!
- A. אפשר לטפל בחולי סרטן בעזרת אימונותרפיה שמטרתה להפעיל את תאי T נוגדי סרטן, המזהים את הגידולים והורגים אותם. B. ברגע שהגידול נהרס תאי T חוזרים לנוח, ויכולים להישאר בגוף במצב הנקרא תאי זיכרון. C. אם הגידול חוזר (גם באזורי גוף מרוחקים או אחרים), תאי זיכרון מסוג T זוכרים איך לגלות את התאים הסרטניים החולים האלה ולהרוג אותם, והם מופעלים מחדש – מתרבים תחילה, ואחר כך תוקפים מחדש את הגידול.
העובדה שמערכת החיסון זוכרת למשך שנים רבות היא היתרון הגדול, שהודות לו הַשְׁפָּעַת האימונותרפיה נמשכת זמן רב. זאת בניגוד לטיפולים אחרים כגון רדיותרפיה או כימותרפיה, שיש לחזור עליהם שוב ושוב בחולה אם מחלת הסרטן חוזרת. מערכת החיסון יכולה לשמור על הזיכרון האימונולוגי הזה לכל משך חיי החולה.
ישנם סוגי אימונותרפיה שונים, כתלות בסוג הסרטן ובחולה
אם כך, מהי אימונותרפיה? מה מוזרק למעשה אל גוף החולה?
יש כמה סיבות אפשריות לכך שמערכת החיסון אינה יכולה לראות את התאים הסרטניים או להרוג אותם. לכן, יש כמה שיטות אפשריות כדי לעזור למערכת החיסון לזהות את התאים הסרטניים ולתקוף אותם. זיכרו שתאים סרטניים יכולים להיות שונים מאוד זה מזה, כתלות באדם ובסוג הסרטן. המטרה הכללית של אימונותרפיה היא ללמד את מערכת החיסון לתקוף את הסרטן. הדבר יכול להיעשות בשיטות הזרקה רבות ושונות. ישנם אלפי סוגים שונים של אימונותרפיות שמדענים בכל רחבי העולם חוקרים עבור סוגים שונים של סרטן.
טבלה 1 מציגה ארבע דוגמאות שונות לאימונותרפיה, ומתארת כיצד היא פועלת. הדוגמה האחרונה מוצלחת במיוחד בשנים האחרונות, והיא תוסבר בפירוט בסעיף הבא (ראו גם איור 3).
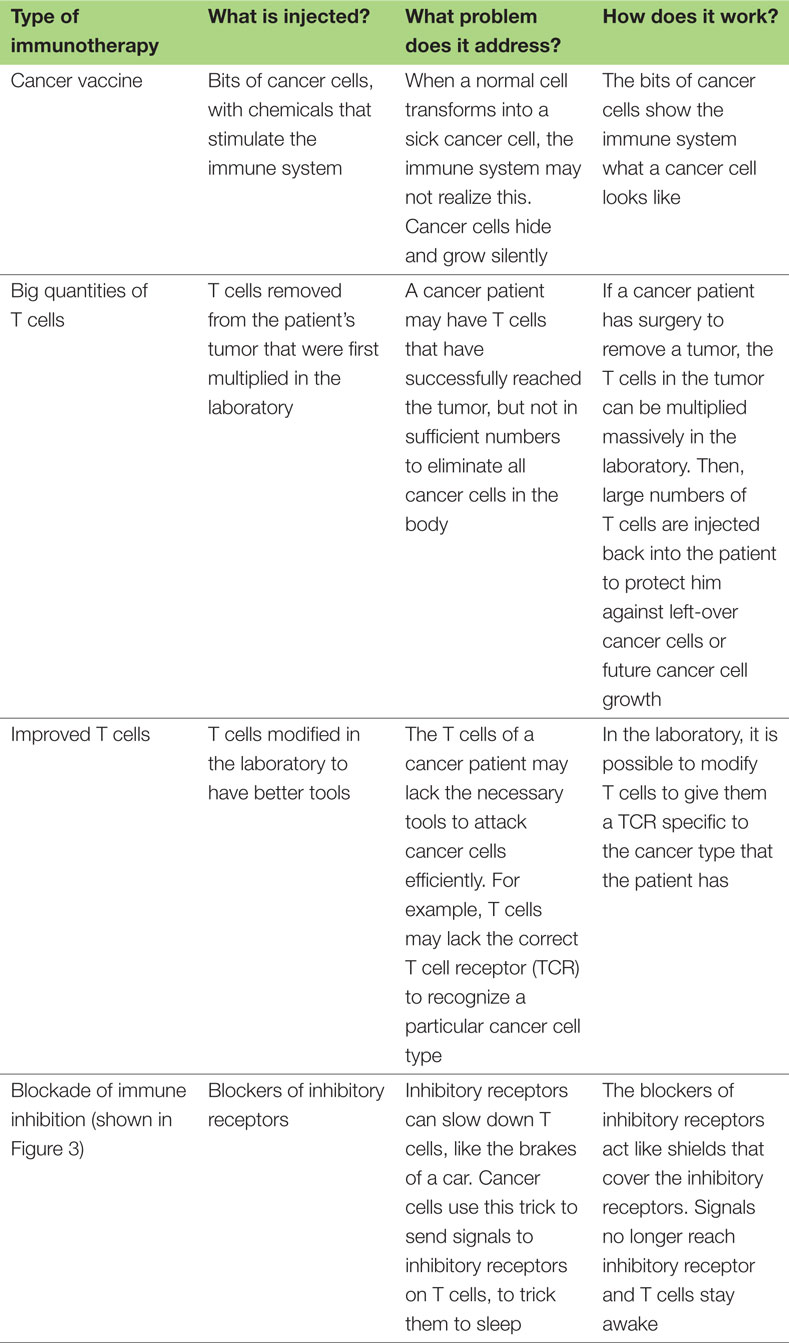
- טבלה 1 - דוגמאות לסוגי אימונותרפיה שונים: מהם וכיצד הם פועלים.
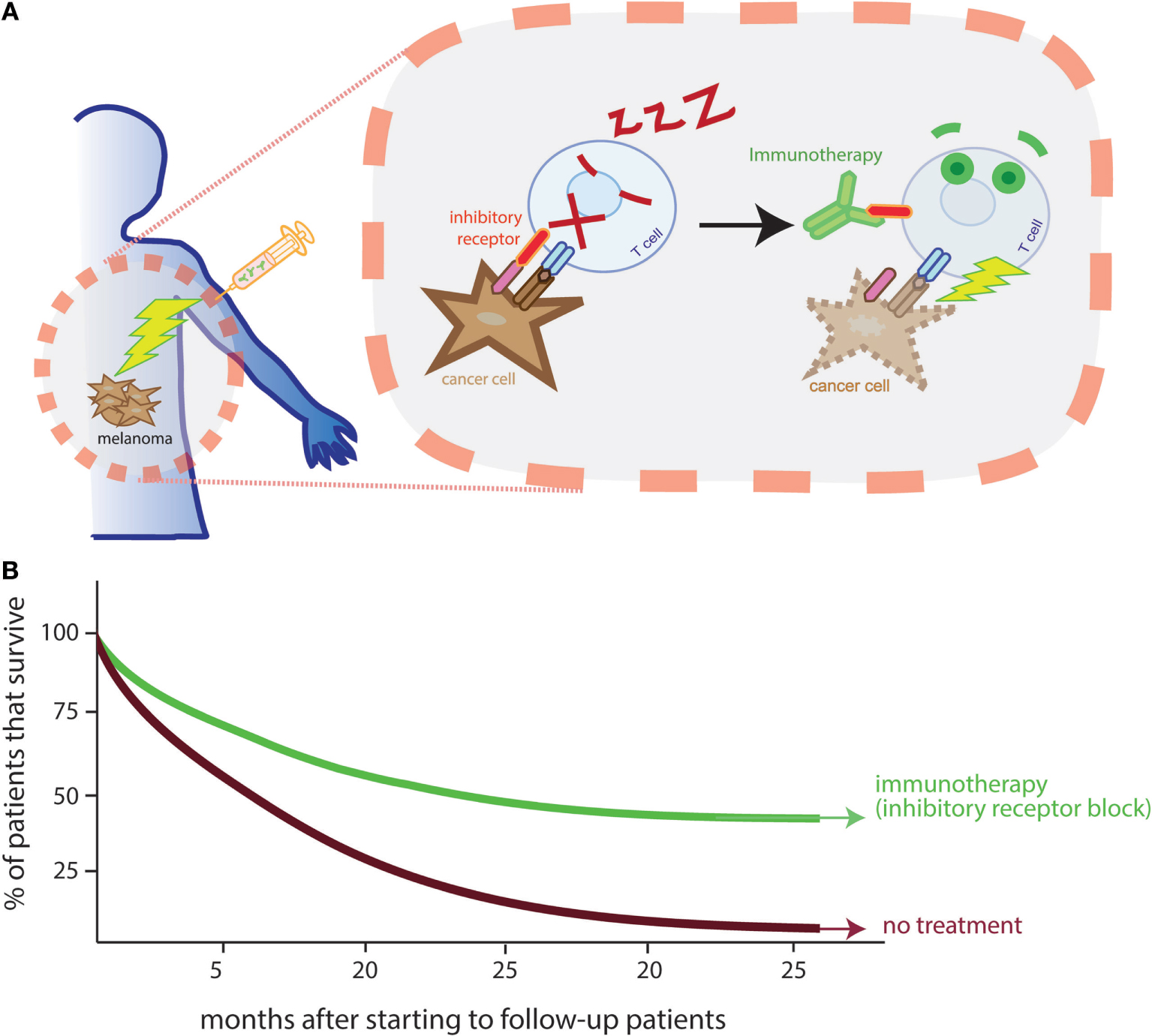
- איור 3 - אימונותרפיה יכולה להעיר את תאיT כך שיהרגו את הגידולים.
- A. באופן טבעי יש על התאים קולטני עיכוב (מוצגים באדום, על שטח פני תא T), הפועלים כמו מעצורים לבקרת מהירותם. תאים סרטניים יכולים לברוח על-ידי שליחת אותות (בוורוד, על שטח פני התא הסרטני) למעצורים האלה, וכך לגרום לתאי T להיכנס לתרדמה. יש אימונותרפיות היכולות לחסום את קולטני העיכוב (בירוק, קשור לקולטני העיכוב), לשחרר את המעצורים ולהעיר את תאי T. B. חולים המטופלים באימונותרפיות שחוסמות את קולטני העיכוב (קו ירוק) שורדים למשך זמן ארוך יותר מאשר ללא טיפול (קו חום) (נתונים אלה נלקחו ממחקר על חולי מלנומה [2]).
תאי T עלולים להגיע לאפיסת כוחות במלחמתם בסרטן, אבל אימונותרפיה יכולה לעורר תאי T ציטוטוקסיים במטרה לסייע בריפוי החולים
אם כך, אם מערכת החיסון שלנו יכולה להרוג סרטן, מדוע בכלל בני אדם חולים בסרטן? התאים הסרטניים מתוחכמים מאוד – הם יכולים לברוח ממערכת החיסון בעזרת תכסיסים שונים. כפי שמוצג באיור 1, תאי T מסיירים בגוף, ובודקים את זהות התאים כדי לדעת אם הם בריאים או זרים. דרך אחת של התאים הסרטניים לחמוק מהתקפת תאי T היא פשוט על-ידי החבאת הפיסות החולות שלהם.
אסטרטגיית התחמקות נוספת שבה משתמשים התאים הסרטניים היא הרדמת תאי T. תכסיס זה נגנב למעשה מתאי גוף בריאים. באופן תקין, כאשר הגוף נלחם בפלישה של נגיף הגורם להצטננות הנפוצה, תאי T הופכים להיות מופעלים והורגים את כל התאים החולים שאליהם פלש הנגיף. ברגע שהנגיפים והתאים המותקפים חוסלו, משהו צריך לספר לתאי T שהם ביצעו את משימתם ושהם צריכים לחזור לנוח. בדיוק כפי שלמכוניות יש מעצורים כדי לשלוט במהירות הנהיגה שלנו, לתאי T יש קולטני עיכוב מיוחדים לשליטה בפעילותם [3]. ללא נוכחות הנגיפים, תאי הגוף הבריאים מאיטים את תאי T המופעלים על-ידי משלוח אות לקולטני העיכוב שלהם. התאים הסרטניים החכמים אשר משתמשים בתכסיס זה יכולים לעשות את אותו הדבר. הם יכולים לשלוח אותות לקולטני העיכוב של תאי T. למעשה, תאי T יכולים להקדיש זמן רב בניסיון להרוג את התאים הסרטניים. בינתיים, התאים הסרטניים שולחים אותות עיכוב ומרדימים את תאי T (איור 3A). כך, לפעמים אצל חולה סרטן יש הרבה תאי T שיכולים לזהות את התאים הסרטניים, אבל אז, התאים הסרטניים משתמשים בתכסיסים כדי לחמוק מהתקפת תאי T. תאים סרטניים יכולים אפילו לחמוק אחרי אימונותרפיה שמפעילה תאי T חדשים על-ידי הרדמת כל תאי T (כולל החדשים)! אבל, סוג אחר של אימונותרפיה יכול לעצור את התכסיס הזה! כיום, יש תרופות חדשות היכולות לחסום את קולטני העיכוב שעל תאי T (איור 3A). בעזרת חוסמים אלה, התאים הסרטניים כבר אינם יכולים להרדים את תאי T. תאי T נותרים פעילים וממשיכים להרוג את התאים הסרטניים. חסימה אימונותרפית זו התגלתה כמוצלחת מאוד – היא ממש מעניקה לחולי סרטן הזדמנות לחיות יותר זמן (איור 2B) [2]. אימונותרפיה חוסמת נהייתה חשובה כל כך שהיא נבחרה על-ידי אחד מכתבי העת המדעיים המובילים, הנקרא “Science” (מדע), כפריצת הדרך של שנת 2013.
מסקנות
למערכת החיסון יש פוטנציאל לחסל סרטן. הטיפולים שמפעילים את מערכת החיסון ומלמדים אותה לזהות תאים סרטניים נקראים אימונותרפיה. היתרון הגדול הוא שמערכת החיסון יכולה לזכור. ברגע שהיא לומדת לתקוף סוג מסוים של סרטן היא יכולה להמשיך לעשות זאת במשך שנים רבות. כיום, יש סוגים אחדים של אימונותרפיות שבהן משתמשים ואותן מפתחים כדי לטפל בחולי סרטן. שיטת טיפול אימונותרפי חדישה עוזרת לחסום את אותות העיכוב ששולחים תאים סרטניים המרדימים את תאי T. אפשר להשתמש באימונותרפיה זו כדי להעיר מחדש את תאי T ולאפשר להם לתקוף מחדש את התאים הסרטניים. בחלק מהחולים, ההשפעה נוגדת הסרטן של אימונותרפיה היא מרשימה, אבל בחולים אחרים עדיין איננו יודעים איך להפעיל את מערכת החיסון ביעילות נגד סרטן. מדענים חוקרים במרץ איך לשפר עוד את האימונותרפיה, בהתבסס על התגלית שמערכת החיסון היא כלי מבטיח מאוד לטיפול בחולי סרטן.
מילון מונחים
סרטן (Cancer): ↑ מחלה המתרחשת כאשר תאים בגוף מאבדים את הבקרה ומתרבים בלי הפסקה. תאים סרטניים עלולים ליצור גושים הנקראים גידולים.
מערכת החיסון (Immune system): ↑ קבוצת מרכיבי הגוף הפועלים להגן על היצור מפלישות וממחלות. מערכת החיסון כוללת את מחסום העור ואת הרקמות הריריות; חומרים הנקראים נוגדנים ותאי דם לבנים הכוללים את תאי T.
אימונותרפיה (Immunotherapy): ↑ טיפולים המבוססים על לימוד מערכת החיסון להילחם במחלה.
תא T ציטוטוקסי (Cytotoxic T cell): ↑ סוג של תא דם לבן שעליו רדארים הנקראים TCR. מטרתו זיהוי ייחודי של תאים חולים כגון תאים נגועים או תאים סרטניים, וחיסולם.
זיכרון חיסוני (Immunological memory): ↑ היכולת של מערכת החיסון ללמוד איך לתקוף חיידק נתון או תא סרטני חולה, ולזכור זאת לעד.
הצהרת ניגוד אינטרסים
המחברים מצהירים כי המחקר נערך בהעדר כל קשר מסחרי או פיננסי שיכול להתפרש כניגוד אינטרסים פוטנציאלי.
מקורות
[1] ↑ Clemente, C. G., Mihm, M. C., Bufalino, R., Zurrida, S., Collini, P., and Cascinelli, N. 1996. Prognostic value of tumor infiltrating lymphocytes in the vertical growth phase of primary cutaneous melanoma. Cancer 77:1303–10. doi: 10.1002/(SICI)1097-0142(19960401)77:7<1303::AID-CNCR12>3.0.CO;2-5
[2] ↑ Hodi, F. S., Chesney, J., Pavlick, A. C., Robert, C., Grossmann, K. F., McDermott, D. F., et al. 2016. Combined nivolumab and ipilimumab versus ipilimumab alone in patients with advanced melanoma: 2-year overall survival outcomes in a multicentre, randomised, controlled, phase 2 trial. Lancet Oncol. 17(11):1558–68. doi: 10.1016/S1470-2045(16)30366-7
[3] ↑ Fuertes Marraco, S. A., Neubert, N. J., Verdeil, G., and Speiser, D. E. 2015. Inhibitory receptors beyond T cell exhaustion. Front. Immunol. 6:310. doi: 10.3389/fimmu.2015.00310