תַקצִיר
חשבו על מה שהמוח שלכם עושה כשאתם מפעילים את הזיכרון שלכם. בתור תרגיל נסו לזכור מה אכלתם אתמול לארוחת צוהריים. ייתכן שתזכרו מיד, אולם מרבית הסיכויים שתצטרכו לחשוב אחורה בזמן על המקום שבו אכלתם את ארוחת הצוהריים, עם מי הייתם, על מה דיברתם או חשבתם וכדומה. בסופו של דבר הזיכרון של ארוחת הצוהריים יופיע מחדש! מה שעשיתם הוא ששִׁחְזרתם את האירוע המסוים, כלומר את הזמן, המיקום וסדרת החוויות החושיות שחוויתם, אשר פרטיו השונים מרכיבים יחד את הזיכרון המורכב כולו. אנו מתייחסים לסוג הזיכרון הזה בתור זיכרון אירועי מאחר שהוא מייצג תרחיש או אירוע מסוים בחיים שלכם. באופן כללי זיכרון אירועי מתייחס לזיכרון של אירועים, ואתם יכולים להיזכר בהם באמצעות “טיול מנטלי בזמן” כלומר, חשיבה לאחור על היכן הייתם ומה עשיתם לצורך שחזור הרכיבים של אירוע מסוים, אשר מאפשרים לכם להעלות בזיכרון את האירוע כולו. במקרים מסוימים זה עשוי להתרחש ללא מאמץ רב (למשל אם אתם רואים סרט שנחרט לכם בזיכרון), ובמקרים אחרים זה עשוי לדרוש מידה רבה יותר של ריכוז ומאמץ. התהליך הזה מהווה את הגרעין של מה שמרבית האנשים מתכוונים אליו כשהם מדברים על “זיכרון”. אולם ישנם סוגים נוספים של זיכרון. זיכרון סֶמַנְטי הוא זיכרון של עוּבדוֹת, כמו למשל השמות של פריטים או ידיעת טמפרטורת הרתיחה של מים. זיכרון נוֹהֳלִי מתייחס לזיכרון שאתם עשויים שלא להיות מודעים אליו, אולם אתם יכולים לממֵּש בפועל – רכיבה על אופניים היא דוגמה אחת לזיכרון נהלי שמשקף כישורים תנועתיים.
מדוע ישנו עיסוק מדעי רב דווקא בזיכרון אירועי? הסיבה לכך היא שישנם מקרים רבים שבהם סוג הזיכרון הזה עשוי להיכשל. כישלון כזה בזיכרון מכֻנה בדרך כלל אַמְנֶזְיָה, או שִׁכָּחוֹן. אחת הדוגמאות השכיחות ביותר לכישלון של זיכרון אירועי נחווית על-ידי אנשים שחולים במחלת האלצהיימר [1]. אלצהיימר הוא סוג מסוים של קִהָיוֹן (או דֶּמֶנְצְיָה,( שהיא בעיה קשה בהרבה מאמנזיה. מטופלים עם דמנציה סובלים מסוגים שונים של בעיות קוגניטיביות כולל אמנזיה, אָפַזְיָה (קושי בהבנה ובשימוש בשפה), קושי בחשיבה מופשטת וקושי בביצוע פעילויות מורכבות. אלצהיימר מתחיל לרוב עם אמנזיה, שמתפתחת בהדרגה במשך שנים עד למצב שבו חלק מאנשים בעלי אלצהיימר כבר אינם מסוגלים לטפל בעצמם. אף על פי שישנן תרופות מסוימות שיכולות לשפר מעט את הסימפטומים של אלצהיימר, השפעתן עדיין קטנה יחסית והן אינן מטפלות בבעיות היסודיות שעומדות בבסיס המחלה.
בעשור האחרון חלה התקדמות משמעותית בהבנת הבסיס הביולוגי של אלצהיימר, וכיום אנשים רבים אופטימיים לגבי האפשרות לפתח טיפול יעיל למחלה. ישנם שני מִבְנים חריגים שמתפתחים במוח במחלת אלצהיימר. המבנה הראשון נקרא (Neurofibrillary tangle), NFT שמתייחס לקשרים הבלתי רצויים בין הסיבים של תאי העצב, שמתפתחים במחלת אלצהיימר ויוצרים “גוש סיבים”). מבנה זה מורכב מחלבון בשם טאו (Tau) שמצטבר בתאי עצב (ראו איור 1A). המבנה השני נקרא פלאק (Plaque), והוא מורכב מחלבון בשם בטה-עמילואיד (β-amyloid, או בקיצורAβ; ראו איור 1B), אשר מופרש בחלל שבין תאי העצב. במשך זמן רב חל ויכוח באשר לסוגיָה אם אחד מהחלבונים או מהמבנים האלה עשוי להיות הסממן הראשון למחלת אלצהיימר, או אפילו המקור שלה. בעוד שאיננו יודעים את התשובה, ישנן ראיות נרחבות שמצביעות על כך שהתפתחות מבנה הפלאק Aβ היא הסממן הראשון של מחלת אלצהיימר. מרבית הראיות האלה מגיעות מהגורמים הגנטיים של המחלה, שאף על פי שהם נדירים ביותר, ידוע שכולם גורמים לייצור מוגבר של חלבון ה-Aβ. עובדה זו עשויה להצביע על כך שייצור מוגבר של Aβ מספיק להתחלת ההתפתחות של מחלת אלצהיימר.
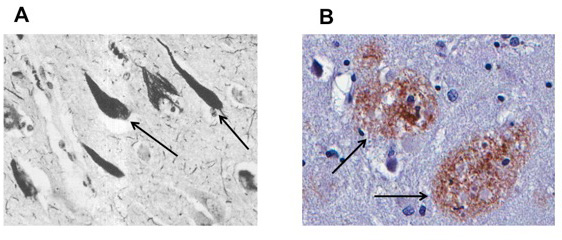
- איור 1 - A. החיצים השחורים מצביעים על תאי העצב שיש בהם את החלבון טאו (שאחראי כאמור להתפתחות של מבני NFT).
- B. החיצים השחורים מצביעים על פלאקים של בטה-עמילואידים (Aβ plaques), אשר מורכבים מהפרשות גדולות של חלבון העמילואיד, המהוות סממן אופייני של מחלת האלצהיימר.
אחת התובנות הראשונות לגבי מקור האלצהיימר הייתה ההבחנה שמבני ה-NFT של חלבון הטאו מרוכזים במיוחד באונה הרקתית האמצעית במוח, באזורים שכוללים את ההיפוקמפוס וחלק מקליפת המוח שנקרא Entorhinal cortex [2]. חלקי המוח האלה פועלים יחד כרכיבי מפתח של מערכת הזיכרון האירועי במוח. עושה רושם שמבנים באונה הרקתית האמצעית חשובים בקשירת היבטים שונים של מה שאנו מכנים זיכרון, כך שאפשר יהיה לשלוף את הזיכרון בשלב מאוחר יותר.
בדוגמה שלנו מתחילת המאמר התחלנו עם השאלה אם אתם זוכרים מה אכלתם אתמול לארוחת צוהריים. ייתכן שזכרתם תחילה את המקום שבו אכלתם (למשל המזנון של בית הספר), ועד שנזכרתם בכל האירוע כבר עלו בזיכרונכם פרטים רבים של אותה החוויה (התאורה שהייתה סביבכם, הצלילים, האנשים והאוכל). ההיפוקמפוס שלכם מעורב בקשירת היבטי החוויה השונים האלה לכדי אירוע אחד שאתם יכולים לשלוף כזיכרון שלכם. כאשר ההיפוקמפוס ניזוק חלה ירידה ביכולות הזיכרון, כאשר נזק בצד השמאלי של הההיפוקמפוס ישפיע לרוב על זיכרון מילולי (של דברים שאתם רואים או קוראים), בעוד שנזק בצד הימני של ההיפוקמפוס ישפיע לרוב על זכרון ויזואלי (דברים שאתם רואים). הנוכחות של מבני NFT של חלבון טאו בהיפוקמפוס וב-Entorhinal cortex ככל הנראה מתערבת בהעברת המידע אל תוך ההיפוקמפוס ומחוץ לו, ולכן גם מתערבת ביכולת לקודד זיכרונות. אפשר להסתכל על ההיפוקמפוס באמצעות סריקת דימות תהודה מגנטית (MRI – Magnetic Resonance Imaging; ראו איור 2A). בסריקות אלה רואים שההיפוקמפוס קטן יותר אצל אנשים עם אלצהיימר ואצל אנשים שיש להם אמנזיה במצב התחלתי יחסית, אך בכל זאת חמוּר. קיים סיכוי גבוה שהאנשים האלה יחוו שלב מוקדם של אלצהיימר.
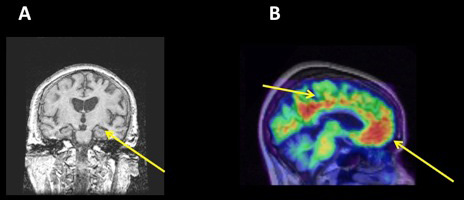
- איור 2 - A. מבט חזיתי של המוח שנלקח באמצעות MRI.
- החץ הצהוב מצביע על האונה הרקתית האמצעית, שהיא קטנה אצל חולים עם אלצהיימר.B. סריקת PET שמראה הצטברות של עמילואיד (באדום, מסומן בחיצים צהובים). האזורים האלה הם חלק מרשת של אזורים מקושרים במיוחד במוח שנקראת Default mode network.
פלאק ה-Aβ משפיע על אזורים שונים במוח יותר מאשר ה-NFT. הפלאק נמצא במיוחד באזורי קליפת המוח של האונות המצחית, הקודקודית והרקתית, אשר מעורבים בתפקודים מנטליים גבוהים (כמו למשל חשיבה מופשטת). כיום אפשר להסתכל על פלאק ה-Aβ באמצעות סריקת טומוגרפיה של פליטת פוזיטרונים (PET) [3]. שיטה זו משתמשת במולקולה רדיואקטיבית אשר אפשר להזריק לדם, ואשר נקשרת לפלאק ה-Aβ במוח. המולקולה המוזרקת מאפשרת קשירה לחלבון Aβ, והרדיואקטיביות מאפשרת לנו לאתֵּר את ההיקשרות הזו באמצעות סורק PET, כך שאנו יכולים למפות את ה-Aβ במוח.
ישנה רשת מסוימת שמושפעת מפלאק ה-Aβ (ראו איור 2B), ומכֻנה Default mode network (DMN בקיצור). רשת זו פעילה במצבים שבהם אינכם מתרכזים במטלה קוגניטיבית ספציפית, אלא חולמים בהקִיץ. רשת זו “נכבית” או נעשית פחות פעילה כשאתם עוסקים בפעילות קוגניטיבית מסוימת, כמו התייחסות לגירוי חיצוני כלשהו. בכמה ניסויים שנערכו נמצא שכאשר אנשים חוו גירוי ראִייתי מסוגים שונים (תמונות, פרצופים וכדומה) רשת ה-DMN נעשתה פחות פעילה, וככל שהיא הייתה פחות פעילה כך הגירוי נזכר טוב יותר. כיום אנו יודעים שחלבון ה-Aβ קשור לדיכוי הפעילות של ה-DMN, שבתורו מתקשר לחוסר תפקוד של הזיכרון.
אם כן, כעת אנו מבינים שני גורמים לכשלים בזיכרון אצל אנשים עם אלצהיימר: הפרשת NFT באונה הרקתית האמצעית והפרשת Aβ ברשת ה-DMN. ניסויים שנערכו באנשים מבוגרים בריאים לגמרי (כלומר שאינם לוקים באמנזיה או באלצהיימר) הראו שינויים באונה הרקתית האמצעית, Aβ ב-DMN ושינויים ברמת הפעילות של ה-DMN. כמה מחקרים מתחילים לבחון את האפשרות להפחית את כמות ה-Aβ במוח באמצעות תרופות מסוימות, כדי למנוע את התפתחות האלצהיימר אצל אנשים מבוגרים. אלה מחקרים יקרים ומסובכים, אולם הם מעוררים תקווה לגבי אפשרות של טיפול מונע למחלה. חשוב יהיה להמשיך לחקור אנשים מבוגרים שמראים סימנים של NFT ושל Aβ במוח, אך טרם מראים סימפטומים של מחלה, כך שנוכל לטפל בהם לפני שהם יחלו. כיום איננו יודעים כיצד לטפל במוחות שכבר ניזוקו, לכן הכיוון של טיפול מונע מהווה את התקווה הגדולה ביותר להתמודדות עם אלצהיימר.
הצהרת ניגוד אינטרסים
המחברים מצהירים כי המחקר נערך בהעדר כל קשר מסחרי או פיננסי שיכול להתפרש כניגוד אינטרסים פוטנציאלי.
מקורות
[1] ↑ Ballard, C., Gauthier, S., Corbett, A., Brayne, C., Aarsland, D., and Jones, E. 2011. Alzheimer’s disease. Lancet 377:1019–31. doi: 10.1016/S0140-6736(10)61349-9
[2] ↑ Braak, H., and Braak, E. 1997. Frequency of stages of Alzheimer-related lesions in different age categories. Neurobiol. Aging 18:351–7. doi: 10.1016/S0197- 4580(97)00056-0
[3] ↑ Rabinovici, G. D., and Jagust, W. J. 2009. Amyloid imaging in aging and dementia: testing the amyloid hypothesis in vivo. Behav. Neurol. 21:117–28. doi: 10.3233/BEN- 2009-0232
