תַקצִיר
חלק מהמטופלים עם מחלות נוירולוגיות (כלומר מחלות שקשורות בהתנהגות בלתי תקינה של תפקודים מוחיים) אינם מגיבים טוב לתרופות הקיימות, ונאלצים לפנות לטיפולים כירורגיים כדי לטפל בתסמינים שהם חווים. מחלת פָּרְקִינְסוֹן לדוגמה, קשורה בנזק באזור מסוים במוח שנקרא גרעיני הבסיס, ומאופיינת ברמות נמוכות מהרגיל של ההורמון דוֹפָּמִין במוח. שינויים אלה בפיזיולוגיה של המוח מקושרים עם תסמינים תנועתיים כמו חוסר יציבות, רעד ואיטיות תגובה, אשר עשויים ליצור מגבלות משמעותיות בתפקוד. למרבה המזל, תרופות כמו לֶבוֹדוֹפָּה (Levodopa) יכולות להשיב באופן חלקי את איזון רמות הדופמין במוח ולהקל על התסמינים התנועתיים של המחלה, בפרט בשלביה המוקדמים. אולם עם התפתחות מחלת הפרקינסון הטיפול התרופתי נעשה פחות ופחות יעיל, ונדרש טיפול נוסף.
גירוי חשמלי של גרעיני הבסיס (כלומר של אותו האזור במוח שפגוע אצל חולי פרקינסון) מֵקֵל על סימפטומים תנועתיים רבים של המחלה. הטיפול כולל הנחת אלקטרודה קבועה בגרעיני הבסיס, כמו גם מיקום קוצב מוחי מתחת לעור החזה של המטופל, אשר מספֵּק את הכוח הנדרש להפיק את הגירוי החשמלי באלקטרודה שבתוך המוח (איור 1). בדרך כלל האלקטרודה מכילה ארבעה מגעים שמספקים סוגים שונים של גירוי חשמלי. לכן ישנן דרכים רבות שבהן רופא יכול לגרות את המוח באמצעות אלקטרודה אחת. ההשפעה של הגירוי החשמלי על התסמינים התנועתיים של מחלת הפרקינסון היא כמעט מיידית. רעד בלתי רצוני בידיים יכול להפסיק בבת אחת, המטופלים רוכשים לעיתים קרובות שליטה טובה יותר על ההליכה שלהם ואיכות חייהם משתפרת. כיום, גירוי מוחי עמוק עבור מחלת פרקינסון ומחלות נוירולוגיות תנועתיות אחרות הוא הליך שגרתי עם תועלות מוכחות. יתרה מזו, היישום שלו לבעיות נוירולוגיות ופסיכיאטריות נוספות נמצא בחקירה נרחבת, והוא בעל תוצאות מבטיחות לטיפול, בין השאר, בדיכאון, בהפרעה טורדנית-כפייתית (OCD – Obsessive-Compulsive Disorder) ובאפילפסיה.
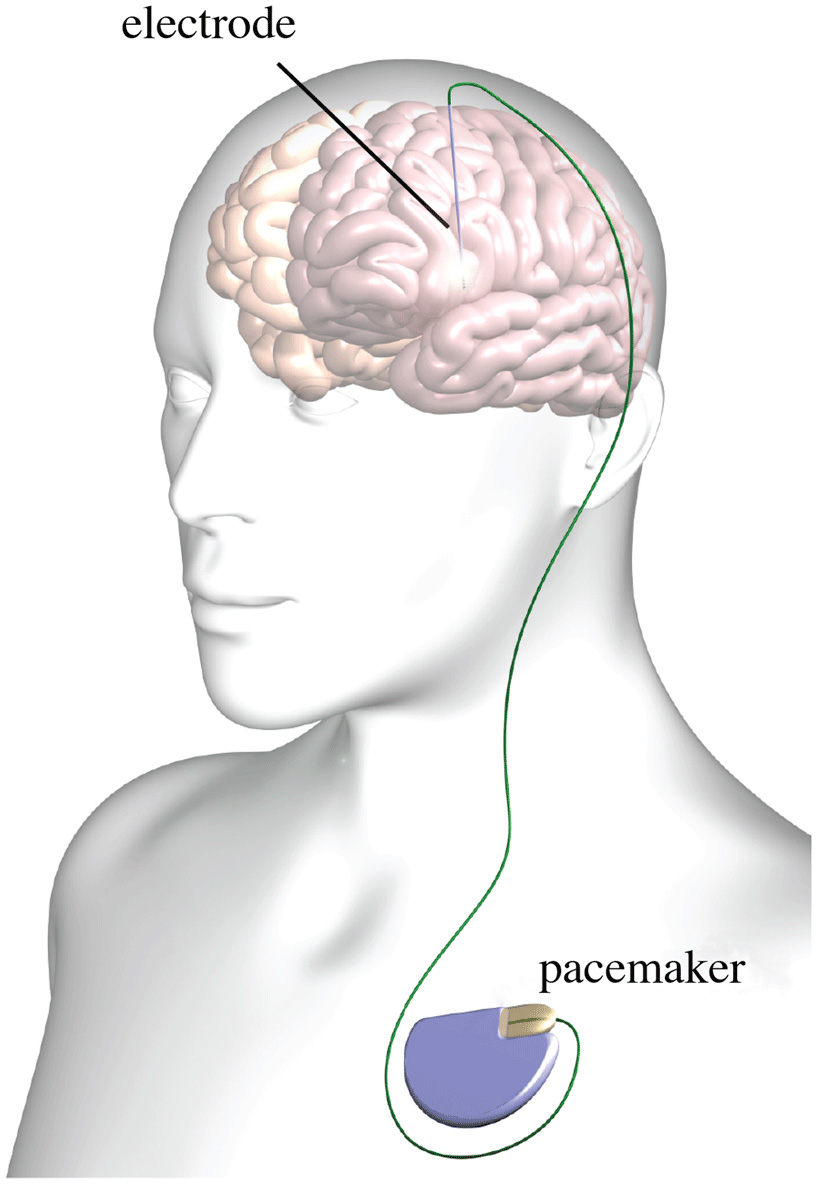
- איור 1 - מערך טיפוסי של מכשירי גירוי מוחי עמוק.
- האלקטרודה (בחלק העליון של האיור) ממוקמת בתוך המוח ומחוברת לקוצב מוחי (מצד ימין למטה) שממוקם באופן קבוע מתחת לעור החזה של המטופל.
למרות התועלת שבו, לגירוי מוחי עמוק עשויות להיות השפעות אשר מִשתנות עם הזמן ובין מטופלים, ולעיתים מופיעות גם תופעות לוואי שליליות. לכן מדענים ורופאים משקיעים מאמצים רבים בשיפור הטיפולים ובהימנעות מתופעות הלוואי. בהתבסס על נתונים רפואיים שנאספו בעשור האחרון, נוסחו הנחיות כלליות לבחירת המטופלים והוגדרו הנחיות לטיפולים זהירים עבור העלאת בטיחות הטיפול במחלת הפרקינסון ובמחלות תנועתיות נוספות. מתברר שההנחיות הכלליות שנוסחו עשויות שלא לאפשר טיפולים מועילים בכשליש מחולי הפרקינסון אשר יכלו להפיק תועלת מגירוי מוחי עמוק. יתרה מזו, ההנחיות הכלליות אינן יכולות לכסות שונוּת רבה בין מטופלים, ושני מטופלים עם תסמינים שונים עשויים לקבל את אותו הטיפול, מה שעשוי להיות פחות יעיל בהשוואה לטיפול שמותאם באופן פרטני למטופל. לכן המחקר שלנו מתמקד כיום בגישה פרטנית למטופל שבּה הטיפול מותאם, בין השאר, לתסמינים המסוימים של המטופל ולהיסטוריה הרפואית שלו.
באופן מסורתי האמינו כי גירוי חשמלי מנטרל את הפעילות של אזור המוח הפגוע. אולם מחקרים עכשוויים מציעים שההשפעה של הטיפול היא מורכבת יותר, וכוללת נטרול של אזורים מסוימים והפעלה של אזורים אחרים. קבוצת המחקר שלנו מחשבת עבור כל מטופל את פיזור הגירוי החשמלי במוח, מעריכה את האזורים המוחיים שמופעלים על-ידי גירוי חשמלי מסוים, ומקשרת בין האזורים המוחיים המופעלים לבין התוצאות בפועל של הטיפול בפרקינסון ותופעות הלוואי שלו (איור 2). בעתיד, רופא יוכל לבחון פרמטרים שונים של גירוי חשמלי (כמו למשל מתח ותדירות) ולקבל, תוך זמן קצר הערכה טובה של השפעותיהם ותופעות הלוואי שלהם, ללא צורך בעירוב נוסף של המטופל. בחינה זו תתבצע באמצעות תוכנת מחשב ייעודית שתוכל לחשב באופן אוטומטי את המערך המוצלח ביותר עבור יעילות מרבּית של הטיפול, ולקצֵּר את זמן הביקור אצל הרופא. אופטימיזציה זו תתבצע בהתאם לתסמינים ולתרופות המסוימים של המטופל. לדוגמה, הגירוי המיטבי עבור חולה עם רעד ביד שמאל יהיה שונה מהגירוי המיטבי עבור חולה עם איטיות תגובה ברגל שמאל. אנו מקווים להחיל את הגישה הזו על מחלות נוספות כבר בעתיד הקרוב.
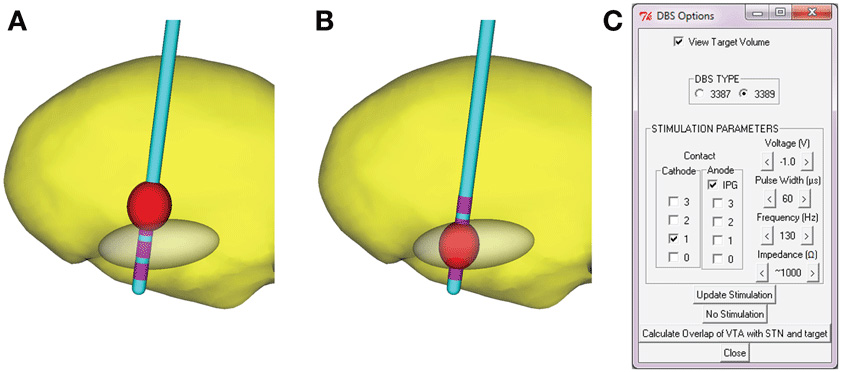
- איור 2 - מודל של ההשפעה של גירוי מוחי עמוק על מוחו של מטופל.
- האזור האדום מייצג את האזור המוחי שיופעל תחת הגירוי החשמלי המסוים שנבחן. גירוי של האזור האפור צפוי להניב את התוצאות הרצויות ביותר. לכן ככל שהחפיפה ביו האזורים האפור והאדום תהיה גדולה יותר, הטיפול יהיה מוצלח יותר. בהמחשה שלנו, מערך הגירוי שמפעיל את רקמת המוח בתוך האזור האפור B. מתועדף על פני מערך הגירוי שמפעיל רקמת מוח אשר נמצאת רֻבּהּ מחוץ לאזור האפור .C .A הפרמטרים השונים שמשפיעים על תוצאות הגירוי החשמלי. דמיינו עד כמה קשה להחליט, ללא הדרכה וניסיון, מהם הערכים אשר יקלו על התסמינים של המטופל.
גישה מעניינת נוספת היא להקליט את הפעילות המוחית של המטופל בעת ביצוע פעילויות תנועתיוֹת, קוגניטיביוֹת (כמו זיכרון, שָׂפָה וכדומה) ופסיכיאטריוֹת, וליצור מַפָּה שמקשרת בין התפקיד לבין מיקומֵי אלקטרודות אפשריים. לאחר מכן האלקטרודה ממוקמת באופן כזה שאזור המטרה מקבל את הגירוי הגדול ביותר. מדענים הציעו להשתמש בגירוי מוחי עמוק רק במקרים שבהם נצפית פעילות מוחית בלתי תקינה ושהוכח שיפור בבחינה של מקרים דומים בבעלי חיים. מחקרים נוספים עדיין נדרשים כדי להבין את טווח התופעות השלם של הגירוי המוחי העמוק.
לסיכום, גירוי חשמלי מוחי עמוק יכול להקל על מחלות נוירולוגיות ופסיכיאטריות שעשויות, אחרת, להיוותר ללא טיפול. מוקד המחקר שלנו כיום הוא בגישה פרטנית למטופל, במטרה למקסֵם את יעילות הטיפול ולמזער את תופעות הלוואי.
הצהרת ניגוד אינטרסים
המחברים מצהירים כי המחקר נערך בהעדר כל קשר מסחרי או פיננסי שיכול להתפרש כניגוד אינטרסים פוטנציאלי.
מקורות
[1] ↑ Butson, C. R., Cooper, S. E., Henderson, J. M., Wolgamuth, B., and McIntyre, C. C. 2011. Probabilistic analysis of activation volumes generated during deep brain stimulation. Neuroimage 54:2096–104. doi: 10.1016/j.neuroimage.2010.10.059
[2] ↑ Eitan, R., Shamir, R. R., Linetsky, E., Rosenbluh, O., Moshel, S., Ben-Hur, T., et al. 2013. Asymmetric right/left encoding of emotions in the human subthalamic nucleus. Front. Syst. Neurosci. 29:69. doi: 10.3389/fnsys.2013.00069
[3] ↑ Frankemolle, A. M., Wu, J., Noecker, A. M., Voelcker-Rehage, C., Ho, J. C., Vitek, J. L., et al. 2010. Reversing cognitive-motor impairments in Parkinson's disease patients using a computational modelling approach to deep brain stimulation programming. Brain 133:746–61. doi: 10.1093/brain/awp315
[4] ↑ Rosin, B., Slovik, M., Mitelman, R., Rivlin-Etzion, M., Haber, S. N., Israel, Z., et al. 2011. Closed-loop deep brain stimulation is superior in ameliorating parkinsonism. Neuron 72:370–84. doi: 10.1016/j.neuron.2011.08.023
[5] ↑ Starr, P. A., Vitek, J. L., and Bakay, R. A. 1998. Ablative surgery and deep brain stimulation for Parkinson's disease. Neurosurgery 43:989–1013. doi: 10.1097/00006123-199811000-00001