תַקצִיר
כשאומרים “חיידקים” חושבים על יצורים חיים קטנטנים, על מחלות ועל גוף האדם. ובאופן כללי – מתכוונים ל“ביולוגיה”. לכן אנשים מופתעים בדרך כלל לגלות שגם פיזיקאים, כמונו, חוקרים חיידקים. פיזיקה היא המדע שמנסה לתאר את העולם בצורה מדויקת בעזרת המתמטיקה וללמוד על תופעות שונות על-ידי ניתוח כמותי, כלומר – מדידות מדויקות. לכן לגישה הפיזיקלית יש מה לתרום גם לתחומים שנראים לא קשורים לפיזיקה. ננסה לספר כאן על חיידקים, על המלחמה בחיידקים גורמי-מחלה ועל אסטרטגיה מעניינת שחיידקים פיתחו כדי לשרוד במלחמה הזו, כפי שהגישה הפיזיקלית עזרה לנו להבין.
כיצד חיידקים בוחרים להתרבות או ללכת לישון?
חיידקים הם יצורים מאוד קטנים, שנמצאים סביבנו, בתוכנו ובעצם כמעט בכל מקום. הם כל כך קטנים עד שאי אפשר לראות אותם בעין, אבל ההשפעה שלהם יכולה להיות גדולה ומורגשת. למשל: חיידקים שנמצאים במעיים שלנו מסייעים לנו לעכל חומרים שונים, חיידקים שחודרים למזון שלנו יכולים לקלקל אותו וחלק מהחיידקים שנכנסים לגוף שלנו, עלולים לגרום למחלות ובהם אנחנו רוצים להילחם.
כדי לספר איך מנסים להילחם באוכלוסייה של מיליארדי חיידקים, צריך ראשית להבין איך הם רבים כל כך, כאשר הכל מתחיל מחיידק אחד שחודר לגוף. כשחיידק נמצא במקום בו יש לו מזון, למשל בתוך גוף של אדם או של בעל חיים, הוא אוכל ומתרבה על-ידי חלוקה: חיידק מתחלק לשני חיידקים זהים, שני החיידקים אוכלים ומתחלקים לארבעה, הארבעה לשמונה וכן הלאה (איור 1 מדגים את הגידול, חיידקים אמתיים לא נראים כך ותוכלו לראות אותם בהמשך באיור 4), כך שמספר החיידקים גדל בקצב מהיר מאוד המכונה “מַעֲרִיכִי”. בסופו של דבר תמיד המזון הזמין לאכילה נגמר ואז החיידקים נכנסים למצב דומה לשינה, בו הם מנסים לבזבז כמה שפחות אנרגיה כדי לשמור על האפשרות שלהם לחזור להתחלק כאשר יגיע שוב מזון לסביבה. המצב החסכוני הזה נקרא בלועזית “מצב סטציונרי”, כלומר “מצב עמיד”, אנחנו נקרא לו תרדמת ואת החיידקים שנמצאים בתרדמת נכנה “רדומים”. כשמזון חדש, למשל סוכר, מגיע לסביבה שבה נמצא חיידק רדום, החיידק מתנהג כמעט כמו ילד רדום שצריך לקום בבוקר, כלומר לוקח לו קצת זמן עד שהוא מפעיל מחדש את המערכות החיוניות לחלוקה, שהוא “כיבה” כדי לחסוך באנרגיה בשלב הרדום. בסוף השלב הזה הוא ער מספיק ומוכן להתחיל לאכול ולהתחלק.
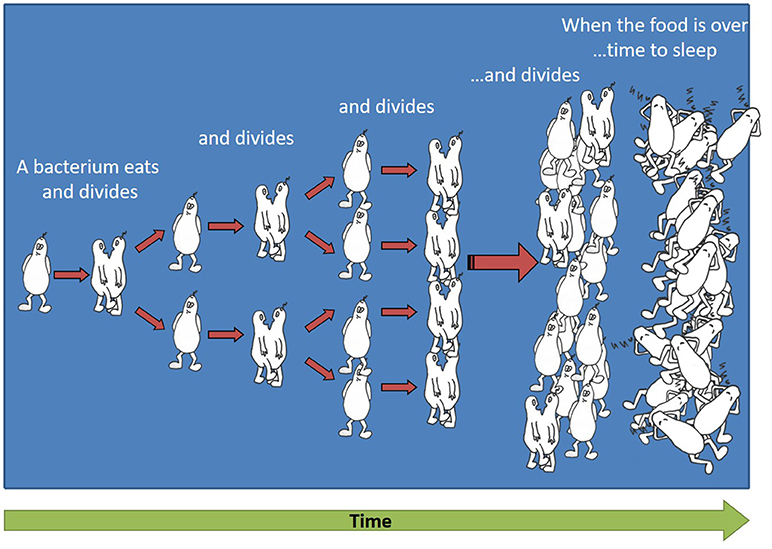
- איור 1 - גידול מעריכי של חיידקים.
- בתהליך של חלוקת תא, חיידק אחד מתחלק לשני חיידקים זהים, שני חיידקים אלה אוכלים ומתחלקים לארבעה חיידקים, ארבעת החיידקים מתחלקים לשמונה, וכן הלאה. בסופו של דבר המזון נגמר והחיידקים הופכים רדומים.
לפעמים עדיף להיות עצלן
כשחודרים לגוף חיידקים גורמי-מחלות, צריך להילחם נגדם: מערכת החיסון המופלאה שלנו מצליחה לרוב לחסל את החיידקים המסוכנים בעצמה, אבל יש מקרים בהם מערכת החיסון לא מצליחה לבד ואז אנחנו חולים ונעזרים באנטיביוטיקה. חומרים אנטיביוטיים הם חומרים הפוגעים בחיידקים באופן בררני (סֶלֶקְטִיבִי), כלומר- אנטיביוטיקה היא חומר שאמור לפגוע בחיידקים ולהרוג אותם, אך בו זמנית לא לפגוע בתאים חיים אחרים שהיא פוגשת- תאי הגוף.
מכיוון שהמערכות המשמשות את החיידק להתרבות על-ידי חלוקה שונות מאוד ממערכות שקיימות בגוף האדם, רבים מהחומרים האנטיביוטיים מכוונים לפגוע במנגנון החלוקה וכך האנטיוביוטיקה היא “ספציפית”- פוגעת באופן בררני בחיידקים.
קורה לפעמים שאנחנו חולים, מקבלים אנטיביוטיקה ומבריאים, אבל אחרי כמה ימים אנחנו מרגישים שוב לא טוב ובבדיקה מתגלה שחלינו מחדש באותה מחלה. בשביל להבין איך המחלה חוזרת אחרי הטיפול, לפעמים אפילו יותר מפעם אחת, עשינו ניסוי שנקרא “ניסוי מבחנה” (מכונה בלועזית “in vitro)” - הסתכלנו על חיידקים מחוץ לגוף של אדם או בעל חיים, בשביל להבין איך הם מתנהגים וכך אולי להבין בהמשך מה קורה בתוך הגוף (“in vivo”). נתנו לחיידקים מזון וראינו שהם מתחלקים ומתרבים ואז הוספנו את החומר האנטיביוטי שנמצא בתוך התרופה לחיידקים שגדלו במבחנה, כלומר, טיפלנו בהם בעזרת אנטיביוטיקה. על כל מה שקרה הסתכלנו בעזרת מיקרוסקופ.
בניסוי הזה ובניסוים נוספים גילינו דבר מעניין ומפתיע: שחלק קטן מהחיידקים נשארים רדומים גם כאשר רוב החיידקים גדלים. זאת אומרת שכאשר נתנו לחיידקים מזון ויצרנו תנאים טובים ומתאימים להתרבות של אוכלוסיית החיידקים, רוב החיידקים הרדומים התעוררו והתחילו, כצפוי, לאכול ולהתחלק. אולם מספר מאוד מאוד קטן מהם נשאר רדום. החיידקים הרדומים האלה מתעוררים הרבה אחרי כל שאר החיידקים ואם האוכל עוד לא נגמר, הם מתחילים לאכול ולהתרבות באופן רגיל, כמו כל אלה שהתעוררו מוקדם יותר [1].
איך לדעתכם זה עזר לנו להבין את החזרה של המחלה אחרי שהטיפול האנטיביוטי הסתיים?
זוכרים שכתבנו שאנטיביוטיקה היא בררנית ופוגעת רק בחיידקים ולא בגוף? ושלכן הרבה סוגי אנטיביוטיקה פוגעים במנגנון החלוקה. לפי זה, אם יש חיידק רדום בזמן שמגיעה האנטיביוטיקה מה יקרה לו? הוא לא מנסה להתחלק ולכן הוא לא יִפָּגַע. כלומר, אם חיידק נשאר במצב רדום הוא יצליח לשרוד את הטיפול האנטיביוטי. באיור 2 ניתן לראות חיידקים רדומים שמתעוררים ומתחילים להתחלק אחרי שמזון חדש הגיע לסביבה. אם אנטיביוטיקה מגיעה לסביבה, היא הורגת את כל המתחלקים ורק חיידקים שנשארו רדומים מצליחים לשרוד.
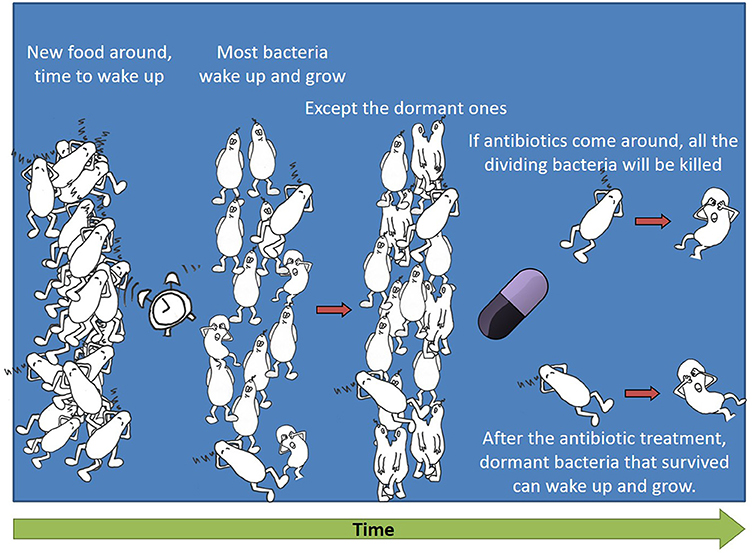
- איור 2 - חיידקים רדומים שורדים טיפול אנטיביוטי.
- חלק מהחיידקים הרדומים מתעוררים ומתחילים להתחלק אחרי שמגיע מזון חדש לסביבה. אם אנטיביוטיקה מגיעה לסביבה, היא הורגת את כל החיידקים המתחלקים ורק חיידקים רדומים שורדים.
אם אנחנו חולים ולוקחים אנטיביוטיקה, כל חיידק שמנסה להתחלק - מת. אבל אם נשארים קצת חיידקים רדומים כאלה, שישנים הרבה זמן ולא מתעוררים במהלך כל ימי הטיפול, הם שורדים. אם חיידק כזה ששרד יתעורר ויתחיל להתחלק, אחרי שהטיפול האנטיביוטי הסתיים, המחלה עלולה לחזור.
מתקן ייחודי למעקב אחר חיידקים תוך כדי טיפול אנטיביוטי
בשביל לגלות את מנגנון השרידות הזה של החיידקים בנינו מערכת מיוחדת המכונה מערכת “מִיקְרוֹפְלוּאִידִית” ומורכבת משלוש שכבות שקופות (מתוארות באיור 3): שכבה ראשונה של תעלות ברוחב מיקרוסקופי, בהן ניתן לשים את החיידקים בתחילת הניסוי. השכבה השנייה היא מעין קרום דק (המכונה מֶמְבְּרָנָה) שיש בו המון חורים קטנטנים, כמו במסננת. הקרום הזה מונח מעל החיידקים וכולא אותם מתחתיו - החורים יותר קטנים מהחיידקים ולכן הם לא יכולים לצאת וכלואים מתחת השכבה המסננת הזו. בשכבה השלישית יש תעלות שבהן ניתן להזרים נוזלים. במהלך הניסוי אפשר להחליף את הנוזל שמוזרם בתעלות וכך לשנות את סביבתם של החיידקים הכלואים במערכת המיקרופלואידית הזו.
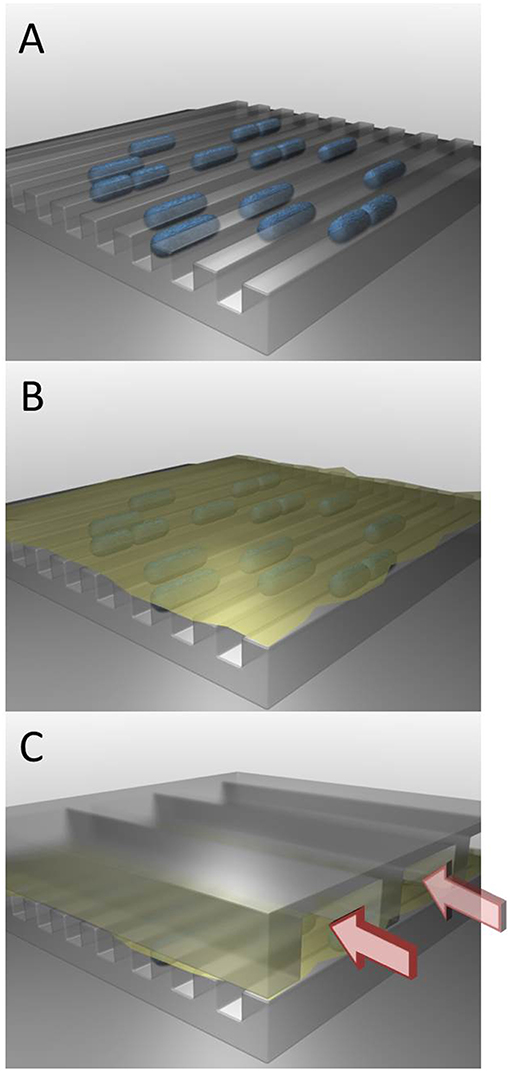
- איור 3 - מערכת מיקרופלואידית לגילוי מנגנון השרידות של חיידקים.
- (A) השכבה הראשונה של המערכת מכילה תעלות דקיקות, בתוכן מניחים את החיידקים (מופיעים באיור בכחול) בתחילת הניסוי. (B) השכבה השנייה במערכת היא ממברנה (מופיעה באיור בצהוב) – מסננת דקה ושקופה – שמכסה את החיידקים וכולאת אותם בתעלות (C) השכבה השלישית של המערכת מכילה תעלות נוספות, גדולות יותר, דרכן נוזלים יכולים לזרום (הזרימה בכיוון החיצים). נוזלים אלה יכולים לעבור דרך הממברנה ולהגיע לחיידקים. כך ניתן לשנות את התנאים לחיידקים, הכלואים בתעלות שבשכבה (A).
את כל המערכת הזו שמנו במיקרוסקופ שנמצא בתוך אינקובטור, הטמפרטורה בו היתה 37 מעלות צלזיוס, כמו בתוך גוף האדם, המיקרוסקופ מחובר למחשב וכך אפשר לצלם את החיידקים ולעקוב אחריהם לאורך זמן. בתחילת הניסוי (איור 4A) הזרמנו נוזל שמכיל מזון לחיידקים, חלקיקי המזון עברו דרך החורים הקטנטנים, החיידקים התעוררו והתחילו לגדול (איורים 4B ו-4C), אחר כך החלפנו את הנוזל והזרמנו נוזל חדש, שהכיל גם מזון וגם אנטיביוטיקה. החיידקים המתחלקים מתו וגם כל חיידק רדום, שהתעורר במהלך השלב הזה, מת כתוצאה מהטיפול האנטיביוטי (איורים 4D ו-4E). בשלב האחרון, כדי לדמות את סוף הטיפול האנטיביוטי, החזרנו את הנוזל שמכיל מזון בלבד וראינו שמבין החיידקים שהיו רדומים ושרדו את כל תקופת הטיפול, יש כאלה שהצליחו להתעורר, להתחלק וליצור אוכלוסייה חדשה של חיידקים (איורים 4F-H).
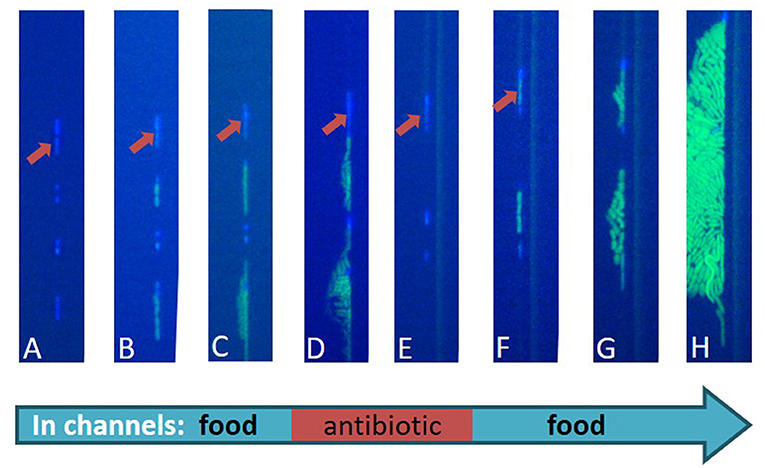
- איור 4 - צילום של חיידקים במהלך הניסוי שתיארנו.
- החיידקים נראים בצבע תכלת בתחילת הניסוי וכאשר הם מתחלקים הם מוצגים בצבע ירקרק, לחיידקים צורה מעט מוארכת והם נפרדים זה מזה. (A) שורה של חיידקים בתוך התעלות המיקרופלואידיות. (B,C) אוכל מוזרם בתעלות וחלק מהחיידקים מתחילים לגדול ולהתחלק. ניתן לראות חיידקים שנשארים רדומים (כמו זה שמסומן בחץ). (D,E) אנטיביוטיקה מוזרמת והורגת את כל החיידקים המתחלקים. היחידים ששורדים הם אלה שהיו רדומים כל זמן הטיפול. (F) לאחר הזרמת האנטיביוטיקה חלק מהחיידקים הרדומים מתחילים להתעורר ולהתחלק. (G,H) אוכלוסיית חיידקים חדשה נוצרה מחיידקים שהיו רדומים ושרדו את כל הטיפול האנטיביוטי.
הבנת האסטרטגיה שעוזרת לחיידקים לשרוד
מעניין לנסות להבין את הסיבות להתנהגות הזו של החיידקים. כל החיידקים בניסוי (ובדרך כלל גם בזיהום שיש בגוף) הם צאצאים של חיידק אחד ראשון ולכן הם מאוד מאוד דומים. אם כולם זהים גנטית וגם היו כל הזמן באותם תנאים ולמרות זאת ההתנהגות שלהם שונה, כנראה יש לזה סיבה טובה. מכיוון שחיידק רוצה שיהיו לו כמה שיותר צאצאים, זאת אומרת להתחלק כמה שיותר פעמים, היינו מנחשים שכשהתנאים טובים, כל החיידקים יתעוררו מיד ויתחילו להתחלק. אבל גילינו שבפועל אוכלוסיית החיידקים כולה מורכבת מקבוצה גדולה של חיידקים ערים, פעילים ומתחלקים ומקבוצה קטנה של חיידקים רדומים. כדי להבין למה, נחשוב מה היתרון של כל אחד מהמצבים. את היתרון של חיידק מתחלק על פני רדום כבר ציינו- יהיו לו יותר צאצאים. אבל מה היתרון של חיידק רדום על פני מתחלק? הניסוי שתיארנו למעלה מדגים את היתרון של חיידק רדום- כשיש אנטיביוטיקה, חיידקים רדומים ישרדו, בעוד המתחלקים ימותו. מסתבר שבטבע יש עוד מצבי “עקה” (מצבים קשים מסוגים שונים שהחיידק צריך להתמודד איתם) בהם לחיידק רדום יש סיכוי גבוה יותר לשרוד.
אז מסתבר מכל זה, שלאוכלוסיית חיידקים יש אסטרטגיה טובה שמאפשרת גם לשרוד לאורך זמן וגם להתרבות ככל האפשר – רוב החיידקים באוכלוסייה גדלים ומתחלקים, מיעוט קטן נשאר רדום ומהווה מעין “עתודה”, אם יהיו תנאים שיהרגו את החיידקים המתחלקים, למשל חשיפה לאנטיביוטיקה, המיעוט הרדום יתעורר וכך אוכלוסיית החיידקים תשקם את עצמה כשהתנאים ישתפרו.
בעזרת מודלים פיזיקליים חישבנו והראינו שמספר החיידקים שנשארים רדומים באוכלוסייה שלמה מתאים לתנאים שבהם החיידקים רגילים לחיות – אם כל הזמן התנאים היו טובים, לא היה צורך בחיידקים רדומים. אם רוב הזמן המצב קשה ויש סיכוי גבוה למות, היה עדיף שיהיו הרבה חיידקים רדומים ושישנו זמן רב ויתעוררו לעיתים רחוקות [2]. אחוז החיידקים הרדומים באוכלוסייה רגילה של חיידקים בטבע, מתאים למצב שבו רוב הזמן התנאים טובים ומאפשרים גידול, מפני שמצבי עקה קיצוניים (כמו אנטיביוטיקה) קורים לעיתים רחוקות, כך שעדיף לכל החיידקים להתחלק ולשמור רק אחוז קטן רדום כ“עתודה” לשעת חירום. כדי לבדוק את המודל הזה, עשינו ניסויים נוספים במעבדה – יצרנו “סביבות חיים” שונות עם תנאים משתנים וראינו שאוכלוסיות החיידקים משתנות ושבכל אוכלוסייה אחוז הרדומים מתאים בסופו של התהליך לתנאים בהם היא חיה. אוכלוסיית חיידקים שנחשפה לאנטיביוטיקה פעמים רבות ולפרקי זמן ארוכים, השתנתה כך שמספר הרדומים בה גדל הרבה יותר מאשר באוכלוסייה “רגילה” והם גם התעוררו לאחר זמן רב. אוכלוסייה שניה שנחשפה לאנטיביוטיקה לפרקי זמן קצרים יותר, השתנתה גם היא לאוכלוסייה עם הרבה רדומים, אך הרדומים שבה התעוררו לאחר זמן קצר יותר [3].
בניסויים נוספים, שלא נתאר כאן, הראינו כי חיידקים עמידים לאנטיביוטיקה נוצרים בקלות רבה יותר באוכלוסייה של חיידקים רדומים [4]. ההבנות שנובעות מהמחקר עד עכשיו, מצביעות על שיטות שעשויות לעזור במניעת הפיכת החיידקים לעמידים – או על-ידי שימוש באנטיביוטיקות שמצליחות להרוג גם חיידקים רדומים, או על-ידי הוספת חומרים שמעירים את החיידקים יחד עם מתן האנטיביוטיקה. שיטות אלה עשויות להיות בעלות חשיבות רבה בשיפור מתן אנטיביוטיקה לחולים באופן שימנע הופעת זיהומים חוזרים וחיידקים עמידים.
נשארנו עם שאלה מעניינת נוספת – איך חיידק יודע “להחליט” אם עליו להתעורר ולהתחיל להתחלק או שהוא זה שצריך להישאר רדום ולהיות ה“עתודה” לשעת חירום? אבל זה כבר סיפור אחר ואתם מוזמנים לנסות לחשוב על כך.
מילון מונחים
חיידקים: ↑ יצורים קטנים מאוד, שלא ניתן לראות בעין. החיידקים מתרבים על-ידי חלוקה. רובם לא מזיקים לאדם, אך חלק מהם יכולים לחולל מחלות.
אנטיביוטיקה: ↑ חומר המשמש כתרופה נגד חיידקים ומתוכנן לפגוע בהם באופן בררני.
בררני (סלקטיבי): ↑ פועל באופן ספציפי. אנטיביוטיקה היא חומר בררני מכיוון שהיא פועל ספציפית כנגד חיידקים, אך לא פוגעת בתאי הגוף שבתוכו הם נמצאים.
אינקובטור: ↑ תא שניתן לשלוט על התנאים בתוכו. ניתן לגדל חיידקים באינקובטור בעל טמפרטורה מתאימה. באינקובטורים מסוימים ניתן לשלוט גם על הלחות ועל תנאים נוספים.
מצב עקה: ↑ מצב בעל תנאים קשים. חיידקים במצב עקה נמצאים בתנאים בהם הם עלולים להיפגע בקלות (דוגמאות למצבי עקה עבור חיידק- טמפרטורה גבוהה מדי, חומציות רבה, נוכחות אנטיביוטיקה).
חיידקים עמידים לאנטיביוטיקה: ↑ חיידקים שהאנטיביוטיקה לא פוגעת בהם. חיידקים רבים כיום עמידים לחלק מסוגי האנטיביוטיקה. קשה יותר לטפל בחולה שנגוע בחיידק עמיד, מכיוון שלא כל סוגי האנטיביוטיקה יהיו יעילים.
הצהרת ניגוד אינטרסים
המחברים מצהירים כי המחקר נערך בהעדר כל קשר מסחרי או פיננסי שיכול להתפרש כניגוד אינטרסים פוטנציאלי.
תודות
תודה לנעמה גפן על איור החיידקים.
מקורות
[1] ↑ Balaban, N. Q., Merrin, J., Chait, R., Kowalik, L., and Leibler, S. 2004. Bacterial persistence as a phenotypic switch. Science 305:1622–5. doi: 10.1126/science.1099390
[2] ↑ Kussell, E., Kishony, R., Balaban, N. Q., and Leibler, S. 2005. Bacterial persistence: a model of survival in changing environments. Genetics 169:1807–14. doi: 10.1534/genetics.104.035352
[3] ↑ Fridman, O., Goldberg, A., Ronin, I., Shoresh, N., and Balaban, N. Q. 2014. Optimization of lag time underlies antibiotic tolerance in evolved bacterial populations. Nature 513:418–21. doi: 10.1038/nature13469
[4] ↑ Levin-Reisman, I., Ronin, I., Gefen, O., Braniss, I., Shoresh, N., and Balaban, N. Q. 2017. Antibiotic tolerance facilitates the evolution of resistance. Science 355:826–30. doi: 10.1126/science.aaj2191
