תַקצִיר
מהו רָעָב? איך אנו יודעים כמה עָלֵינוּ לאכול? מה קורה אם איננו אוכלים מספיק? כדי להתקיים, הגוף האנושי חייב להחזיק מאגרי אנרגיה זמינים בצורת רִקמת שומן. רִקמה זו מדווחת למוח בצורה שוטפת על מלאי המאגרים, באמצעות הורמון בשם לֶפְּטִין. לפטין מגיע לזרם הדם ומשם נכנס אל המוח. כאשר מצטברת כמות גבוהה של הורמון זה, הגוף מקבל פקודה להפסיק לאכול. במצבים כמו הַשְׁמָנָה והיריון המוח רגיש פחות להורמון הלפטין, ולכן הרעָב מתגבר. מדענים רבים עדיין מנסים להבין מהי הסיבה לכך. במעבדה שלנו אנו משׁערים כי בהשמנה ובהיריון חלים שינויים בכלי הדם שאמורים להעביר את ההורמון לאזורים במוח האחראים על מנגנון הרעב. עקב כך נוצרת בגוף אשליה שלפיה המוח מעביר פחות פקודות להפסיק לאכול, וכפֹעַל יוצא אנו משמינים.
הורמונים משפיעים על תחושות הָרָעָב והַשּׂבַע שלנו
אנשים מהרהרים רבות במזון, בהֶקשרים שונים. כמה פעמים במהלך היום אנו חושבים לעצמנו מה כדאי לאכול? האם אנו רוצים שוקולד, חטיף או אולי ארוחה חמה? אנו מקדישים זמן לתכנון הארוחות, וחלקנו תוהים למה קשה לנו לרדת במשקל.
האם נתתם דעתכם למשמעות של להיות רעבים או שְׂבֵעִים, ואיך כל זה קשור למשקל הגוף?
אכילה היא פעולה יומיומית שאותה אנו מְבצעים בפרקי זמן שונים לאורך היום. אך האם עצרתם לחשוב אם הגוף יודע כמה אנו צריכים לאכול? אם כן, כיצד הוא עושה זאת? ומה קורה שעה שאנו אוכלים יותר מדי או פחות מדי?
בעולם שמחוץ לגוף אנו מְתקשרים זה עם זה באמצעות שיחה, התכתבות או סימנים מוסכמים. בגוף, האיברים מְתקשרים ביניהם בעזרת חומרים המכונים ''הוֹרמוֹנים''. כאשר איבר צריך להעביר הודעה לאיבר אחר, הוא יכול להפריש הורמון אל הדם. סוג ההורמון והריכוז שלו בדם הם תוכן ההודעה. הדם נושא את ההורמון לרחבי הגוף, ואיברים אחרים ש'עוקבים' אחר האיבר המפריש מקבלים את המידע. איברים יכולים להפריש ולקלוט כמה סוגי הורמונים, ובאופן זה לנהל ביניהם 'שיחה' ערה. המוח עוקב אחר פעילות איברי הגוף באמצעות חישָׁה של רמות ההורמונים, מגיב להודעות המתקבלות, ושולח אותות עצביים או מפריש בעצמו הורמונים שתפקידם לווסת את פעילות האיברים ואת התנהגותנו.
ישנם הורמונים רבים שמשפיעים על רעב, שובע, כמות האוכל שאנו נדרשים לצרוך כדי להיות שׂבעים, ומתי נהיה רעבים שוב. אחד ההורמונים החשובים בהֶקשר זה הוא לֶפְּטִין. זהו הורמון המופרש מתאי השומן אל הדם ומאותת לשאר הגוף על מצב מאגרי השומן, או לגבי האנרגיה שלנו [1]. רמות נמוכות של לפטין מעידות על כך שמאגרי האנרגיה בגוף מתדלדלים, ולכן הגוף צריך להגיב ולשנות את פעילותו. למשל, להתחיל לאכול. לפטין נקלט באזור במוח המכונה הִיפּוֹתָלָמוּס, שאחראי על מנגנון השליטה והבקרה המרכזי במוח. אזור זה משפיע על גדילה; תחושת לַחַץ; עייפוּת; השעון הביולוגי שלנו, וכן על תחושות צָמָא, רָעָב ושׂבַע. ההיפותלמוס מווסת את הוצאַת האנרגיה באמצעות שינוי קצב התרחשות תהליכים בגוף, כמו כמות האנרגיה שאנו מוציאים במנוחה; תחושת עייפוּת, ומאותת גם על צורך בהכנסַת אנרגיה לגוף על ידי אכילה. באופן זה ההיפותלמוס שומר על משקל גוף תקין ועל אספקת חומרים סדירה לגוף.
מה קורה כשהגוף אינו מגיב להורמון הלפטין?
ישנם מצבים שבהם ההיפותלמוס לא קולט היטב את האות ששולחת רקמת השומן באמצעות לפטין, או לא מפרשׁ זאת בצורה נכונה. מצב של ירידה בתגובת המוח ללפטין מכונה תִּנְגֹּדֶת ללֶפְּטִין [2]. במצב זה, ההיפותלמוס חש רמות נמוכות של לפטין למרות שכמות רקמת השומן ורמות ההורמון תקינוֹת. ההיפותלמוס מפרשׁ שֶׁדֶר לגבי רמות לפטין נמוכות לכאורה, כמצב שבו אין בגוף מספיק שומן. בתגובה, חלה ירידה בקצב חילוף החומרים, ונוצרת תחושת רעב שגורמת לאכילה. לאורך זמן, הגוף ישמין, ורמות הלפטין יעלו עד למצב שההיפותלמוס יפרשׁ כתקין.
מתי נצפית תנגודת ללפטין? בהיריון למשל. במהלך ההיריון חלה ירידה בתגובת המוח ללפטין, המובילה לאכילה מוגברת של האם [3]. תופעה זו רצויה: בתקופת ההיריון הגוף צריך לספֵּק חומרי גלם ואנרגיה לא רק לאם, אלא גם לעֻבָּר הגדֵל ברחם, ולכן הגוף מעלֶה את צריכת המזון של הָאֵם. יצירת תנגודת ללפטין במהלך ההיריון מאפשרת לאם להגדיל את מאגרי השומן כדי להתכונן לעלייה בצרכים האנרגטיים של העובר המתפתח, וכן לקראת צורכי האנרגיה הגבוהים הכרוכים בהֲנָקָה (ראו איור 1).

- איור 1 - היריון מגביר את תחושת הרעב.
- אחת הסיבות לכך היא שבמהלך ההיריון נוצרת עמידוּת של הגוף ללפטין. התמונה יוצרה באמצעות DALL-E.
למעשה, תנגודת ללפטין יוצרת אשליה בהיפותלמוס שלפיה אין לגוף מספיק שומן. אשליה זו מתרחשת גם במצב של הַשְׁמָנָה: למרות שכמות רקמת השומן גדולה, ההיפותלמוס חש שכמות השומן תקינה. הַרְזָיָה מתפרשת כירידה מתחת לכמות השומן הרצויה, דבר שמניע תהליכים הגורמים לעלייה במשקל, ומביא להשמנה מחדש. הדמיון בין שני המצבים, היריון והשמנה, מעלֶה את השאלה: האם במצב של השמנה מופעלים אותם מנגנונים שגורמים לאכילה מוגברת בהיריון?
מדענים כיום אינם מבינים מה עומד מאחורי התפתחות תנגודת ללפטין, לא בהיריון ולא בהשמנה. נושא זה נחקר במגוון מדינות במאמץ לפתור את התופעה החברתית-בריאותית של השמנה, שהייתה לחובקת עולם. ההשׁערות הרווחות הן כי ייתכן שישנם חומרים שהגוף מפריש אשר מעמעמים את פעילות ההורמון; מצבי לחץ גופני ונפשי עשויים להשפיע על הרגישוּת ללפטין, וייתכן שההיפותלמוס עצמו מאבד יכולת חישָׁה בשל התפתחות דלקת מקומית.
כיצד לפטין מגיע אל המוח?
איך הורמון כמו לפטין עושה דרכו למוח? אם ננסה לדמיין איך הורמון נע בזרם הדם ונקלט במוח, אולי תצטייר תמונה של כדור הנישׂא על נהר ומגיע לחופֵי המוח, שם הוא נִשְׁלָה מהנהר על ידי תאי עָצָב (נוֹיְרוֹנִים) חרוצים, שמעבירים את הַמֶּסֶר מרקמת השומן. אולם מסתבר שלמוח, בניגוד לרקמות אחרות בגוף, אין כמעט חופים שבהם ניתן לִמְשׁוֹת את ההורמונים. המוח הוא מִבְצָר המוקף מְצוּקִים ושומרים שלא מאפשרים להורמונים להעביר הודעות.
כלֵי הדם שבתוך המוח, המובילים דם מהגוף אל המוח, אינם מאפשרים לכל חומר, דוגמת הורמון, פשוט להגיע למוח. תכונה זו הופכת את המוח מקום מוגן במיוחד מפני רעלנים, חיידקים ומחוללי מחלות. היכולת למנוע כניסה של חומרים בלתי רצויים מתאפשרת באמצעות כלי דם אטוּמים ייחודיים למוח, שמאפשרים מַעֲבָר מְבֻקָּר של חומרים הנחוצים למוח בלבד, מהדם למוח. מערכת כלי הדם הזו מכונה מחסום דם-מוח. כיצד אם כן יכול ההיפותלומס לחוש את רמות ההורמנים בדם בכל זאת? סמוך להיפותלמוס ישנוֹ אזור קטנטן במוח שנקרא בּליטה תיכונה, שבו כלי הדם בנויים ומְתפקדים מעט אחרת [4]. על דרך הדימוי – בִּמקום מְצוּקים יש שָׁם חוף חולי, שדרכּו ההורמונים מכל הרקמות מוֹסרים הודעות להיפותלמוס, ודרכּו גם מופרשׁים הורמונים לזרם הדם. כלי הדם בבליטה התיכונה אינם אטוּמים, אלא נראים כמו צינור מנוקב שמאפשר להורמונים להיכנס ולצאת. הנקבים האלה מכונים חלוֹניוֹת (או פֵנֶסְטְרוֹת בשפה הלטינית), והקוטר של כל אחד מהם הוא פחות מ-100 נָנוֹמֶטֶר [5]. (ננומטר אחד שווה למיליונית המילימטר), כלומר קטן בערך פי אלף מעובי שׂערה אנושית! אולם, הבליטה התיכונה עלולה להיות גם נקודת תורפה של ההיפותלמוס. כל שינוי בתכונות הבליטה כמו ירידה בצפיפות החלוניות, גודלן או מספרן, ישפיע על יכולת ההיפותלמוס לחוש את רמות ההורמונים בדם, ולהפריש בעצמו הורמונים אל הדם (ראו איור 2).
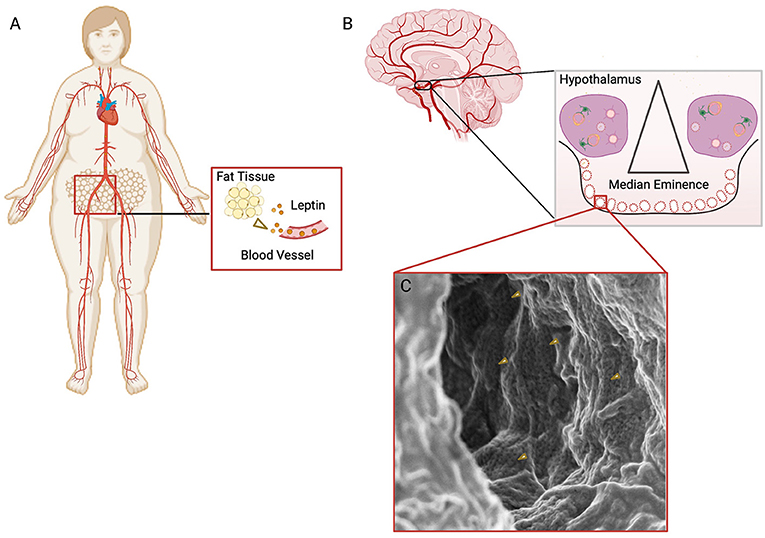
- איור 2 - כיצד הלפטין נכנס למוח?
- (A) רקמת השומן (Adipose Tissue) מפרישה לפטין (Leptin) אל זרם הדם, שעובר בגוף ומגיע בסופו של דבר אל המוח. מקרא: Blood vessel = כלי דם. (B) הדם נושא את הלפטין למוח. ניתן לראות איור של הבליטה התיכונה (Median Eminence), וחלק מההיפותלמוס (Hypothalamus), שבהם עוברים כלי דם מחוררים (Fenestrated Vessel)- אלה הן חלוניות שדרכן נכנס הלפטין (בנקודות הצהובות). בהגדלה של הבליטה התיכונה, אנו רואים צילום שבוצע במיקרוסקופ אלקטרונים סורק, של הצד הפנימי של כלי דם בבליטה זו. הנקודות הכהות מסמלות חורים בכלי הדם (חלקם מסומנים על ידי חיצים צהובים), שהם החלוניות שדרכן יכול הלפטין לעבור אל המוח.
המחקר שאנו עורכים במעבדה
במעבדתנו אנו מתמקדים בשתי שאלות עיקריות: כיצד לפטין מגיע למוח ולהיפותלמוס, והאם מכשולים שבהם הוא נתקל בדרכו להיפותלמוס הם שיוצרים את התנגודת?
ההשערה שלנו היא שתנגודת ללפטין מתפתחת גם כיוון שהחלוניות בבליטה התיכונה מתמעטות. כאשר ישנן פחות חלוניות בכלי הדם, פחות לפטין נכנס להיפותלמוס, ונוצר מצב שבו המוח לא חש את רמות הלפטין האמיתיות שרקמת השומן מפרישה, מה שגורם להשמנה.
זה נשמע מעט מוזר–למה שהחלוניות ייסגרו? אבל יש לכך תקדימים. גם איברים אחרים בגוף, כמו הכּבד, צריכים לקלוט ולהפריש חלבונים, הורמונים וחומרים אחרים אל זרם הדם. כלי הדם המזינים את האיברים הללו משובצים בחלוניות. בתהליך ההזדקנות למשל, כמות החלוניות בכבד יורדת, ושינוי זה משליך על פעילות הכבד [6]. אנו אפילו מכירים הורמונים שמשפיעים על כמות החלוניות. ידוע כי הרמות של חלק מההורמונים הללו משתנות במהלך היריון, בהשמנה וכשאנו מזדקנים.
כדי לחקור את החלוניות, אנו משתמשים במיקרוסקופים מיוחדים מאוד כמו מיקרוסקופ אלקטרונים, שמאפשרים לנו לראות את החלוניות ואת מַעֲבַר מולקולות הלפטין עצמן דרך החלוניות. באמצעות המיקרוסקופ הבחנּוּ בכך שלפטין, שקוטרו כ-10 ננומטר–מיליונית מגודל ציפורן אנושית–עוֹבֵר דרך החלוניות בבליטה התיכונה וכן דרך חלוניות בהיפותלמוס, שלא היה ידוע לפני כן על קיומן! (ראו איור 3).
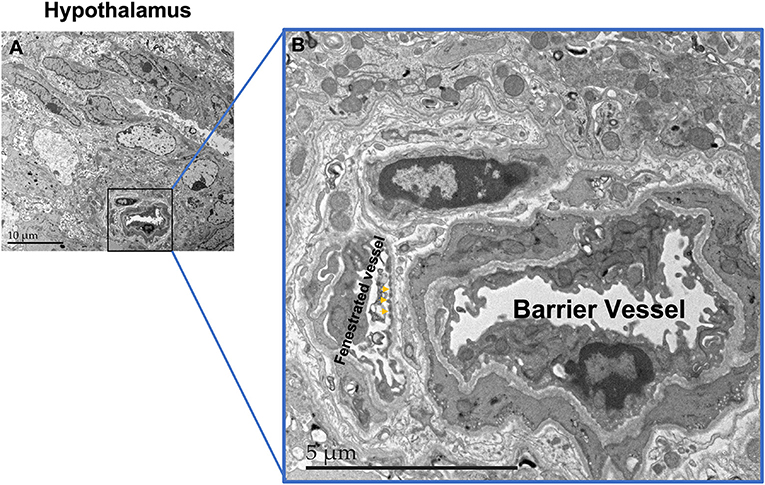
- איור 3 - (A) צילום של ההיפותלמוס באמצעות מיקרוסקופ אלקטרונים חודר.
- הגדלה של 10 מיקרומטר (מליונית המטר, μm) מימין, ושל 5 מיקרומטר משמאל. (B) בחלק הימני של הצילום רואים שני כלי דם: אחד מבוצר (Barrier Vessel) שאינו מאפשר מַעֲבָר, המוצג ככלי דם שלם ואחיד; והשני כלי דם עם חלוניות (Fenestrated Vessel), שחלקן מסומנות בחיצים.
נראה כי היריון האישה גורם לכך שפחות כלי דם בבליטה התיכונה יהיו מנוקבים, כך שסך הכול ישנן פחות חלוניות, וחֵלֶק מההיפותלמוס עלול שלא לקלוט לפטין כלל. ראינו גם כי בחֵלֶק מההיפותלמוס ישנם כמה כלי דם בעלי חלוניות שמספרם יורד בהיריון, מה שמחזֵּק את המחשבה כי פחות הורמון מגיע אל המוח במצבים של תנגודת ללפטין.
מה בעתיד?
ישנהּ חשיבוּת רבה להמשך אפיון של כלי הדם המנוקבים, ועריכת מחקר על אודות הגורמים שמשפיעים על גודל החלוניות, צפיפותן, וכלי הדם שבהם ניתן למצוא אותן בבליטה התיכונה ובהיפותלמוס. זאת לצורך הבנה טובה יותר של התקשורת בין איברים שונים לבין המוח באמצעות הורמונים. בפרט, תוצאות המחקר יסייעו לנו לענות על השאלה שמעסיקה את כולנו מדֵּי יום: לאכול או לא לאכול, וכן על שאלות הנגזרות ממנה כמו כמות המזון שיש לצרוך.
מילון מונחים
הורמון (Hormone): ↑ חומר שמופרש מאיבר כלשהו בגוף אל זרם הדם, ושבאמצעותו מועבר מֶסֶר ביולוגי לאיברים מרוחקים.
לֶפְּטִין (Leptin): ↑ הורמון שמופרש מתאי שומן ומעודד רָעָב כאשר הוא נקלט בהיפותלמוס (ראו הגדרה בהמשך מילון המונחים).
הִיפּוֹתָלָמוּס (Hypothalamus): ↑ אזור במוח שמבקר היבטים בסיסיים בפעילות הגוף כגון רָעָב; צָמָא; לַחַץ; שעון ביולוגי ועוד.
תִּנְגֹּדֶת ללֶפְּטִין (Leptin Resistance): ↑ מצב שבו פוחתת התגובה של איבר מסוים בגוף ללפטין.
מחסום דם-מוח (Blood-Brain Barrier): ↑ תכונות של כלֵי דם במוח המאפשרות לחומרים מסוימים בלבד להיכנס מהדם אל תוך המוח, כדי להגן עליו ולוודא שלא יינזק.
בּליטה תיכונה (Median eminence): ↑ מבנה במוח שבו מצויים כלי דם בעלי חלוניות, הנמצא בסמוך להיפותלמוס.
חלוֹנית (Fenestra): ↑ חור בקוטר 100-50 נָנוֹמָטָר (מיליונית המילימטר) בכלי דם, המאפשר מַעֲבָר חופשי של חומרים מהדם ולתוכו.
הצהרת ניגוד אינטרסים
המחברים מצהירים כי המחקר נערך בהעדר כל קשר מסחרי או פיננסי שיכול להתפרש כניגוד אינטרסים פוטנציאלי.
מקורות
[1] ↑ Friedman, J. M. 2019. Leptin and the endocrine control of energy balance. Nat. Metab. 1:754–64. doi: 10.1038/s42255-019-0095-y
[2] ↑ Izquierdo, A. G., Crujeiras, A. B., Casanueva, F. F., and Carreira, M. C. 2019. Leptin, obesity, and leptin resistance: where are we 25 years later? Nutrients 11:2704. doi: 10.3390/nu11112704
[3] ↑ Gustafson, P., Ladyman, S. R., and Brown, R. S. E. 2019. Suppression of leptin transport into the brain contributes to leptin resistance during pregnancy in the mouse. Endocrinology 160:880–90. doi: 10.1210/en.2018-01065
[4] ↑ Rodríguez, E. M., Blázquez, J. L., and Guerra, M. 2010. The design of barriers in the hypothalamus allows the median eminence and the arcuate nucleus to enjoy private milieus: the former opens to the portal blood and the latter to the cerebrospinal fluid. Peptides 31:757–76. doi: 10.1016/j.peptides.2010.01.003
[5] ↑ Stan, R. V. 2007. Endothelial stomatal and fenestral diaphragms in normal vessels and angiogenesis. J. Cell. Mol. Med. 11:621–43. doi: 10.1111/j.1582-4934.2007.00075.x
[6] ↑ May, D., Djonov, V., Zamir, G., Bala, M., Safadi, R., Sklair-Levy, M., et al. 2011. A transgenic model for conditional induction and rescue of portal hypertension reveals a role of VEGF-mediated regulation of sinusoidal fenestrations. PLoS ONE 6:e21478. doi: 10.1371/journal.pone.0021478
