תַקצִיר
דַּמְיְנוּ שהייתה הודעה חשובה מאוד שנדרשתם להעביר לחֲבֵרָה שלכם במהירוּת הַמְּרבית האפשרית. האם הייתם שולחים לחברתכם מכתב כתוב דרך שירותי הדואר, שהיה מגיע בתוך כמה ימים? או שהייתם שולחים הודעת דואר אלקטרוני, אשר מגיעה כמעט מייד? תפקידוֹ של תא עָצָב (נוֹיְרוֹן) הוא לשלוח הודעות במהירות ברחבי המוח, חוט השדרה, והגוף. בביצוע התפקיד החשוב הזה, תאי עצב מקבלים סיוע מסוגי תאים אחרים, שנקרא אוֹלִיגוֹדֶנְדְרוֹצִיטים. במאמר זה, נתאר כיצד אוליגודנדרוציטים מסייעים לתאי עָצָב לשלוח את הודעותיהם במהירות, וכיצד מדענים מנסים להגן על אוליגודנדרוציטים ולהחליף את האוליגודנדרוציטים שנפגעו במחלות כמו טָרֶשֶׁת נפוצה, או לְאַחַר פגיעה מוחית.
שליחת הודעות ברחבי הגוף
נוֹירונים (תאי עצב) הם כמו הדוָורים של הגוף; אחראים על העברַת הודעות ברחבי המוח והגוף. כדי שיוכל לשלוח את ההודעות האלה, לנוירון יש צורה מיוחדת: שלוחה ארוכה, דמוּית-צינור, שנקראת אַקְסוֹן, אשר נשלחת החוצה לְעַבֶר המטרה שלה (איור 1A). תוכלו לחשוב על אקסונים כמו על כבישים שהדוור צריך לנסוע בהם כדי למסור מכתבים. אולם, לא כל הכבישים או מסלולי המסירה זהים. חלק מהכבישים יכולים להיות ארוכים יותר מאחרים, ובחלקם עשויים להיות מהמוֹרוֹת או פקקים, שעלולים להאט את משלוח הדואר. זה יכול להוות בעיה אם יש לכם הודעה חשובה מאוד שהצד השני צריך לקבל באופן כמעט מיידי.
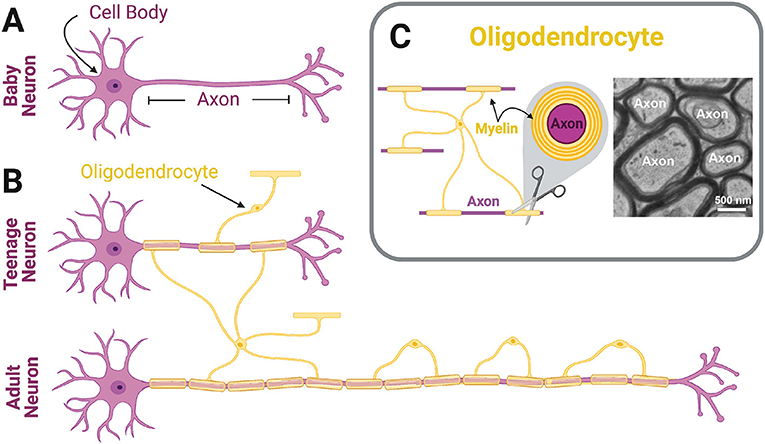
- איור 1 - ציפוי הָאַקְסוֹנִים במִיאָלִין.
- (A) אצל תינוקות (Baby), תאי עצב אינם מצוּפים במִיאָלִין (Myelin) כְּלָל. (B) בהדרגה, כאשר ילדים גדֵלים, אוליגודנדרוציטים (Oligodendrocyte) מצפים את האקסונים (Axon) במיאלין. (C) אוליגודנדרוציט אחד יכול לְצפות במיאלין אקסונים רבים בבת אחת. אם הייתם חותכים נוירון המצופה במיאלין, הייתם רואים את המיאלין מלופף סביב האקסון בשכבות. מימין, תוכלו לראות תמונה אמיתית של מיאלין מלופף סביב אקסונים.
מקרא:
Teenage = גיל ההתבגרות
Adult = מבוגר
Cell body = גוף התא.
במטרה להאיץ את מהירוּת שליחת ההודעות, תאי עצב חוֹברים לתאים מיוחדים שנקראים אוֹלִיגוֹדֶנְדְרוֹצִיטִים. כאשר תאי עצב מקבלים סיוע מאוליגודנדרוציטים, הם יכולים לשלוח הודעות במהירות הַבָּזָק, אפילו אם האקסונים שלהם ארוכים מאוד. המילה אוליגודנדרוציט נשמעת קצת מוזר, אך השֵּׁם מתאר את תפקידו המיוחד של תא מסוג זה. כמו מילים רבות בביולוגיה, מקור המילה ביוונית, ומשמעותה 'תא עם כמה ענפים'. לאוליגודנדרוציט אחד יכולים להיות עד 50 ענפים שונים [1]. כל ענף נשלח החוצה במטרה לתפוס אקסון (איור 1B). לאחר מכן, האוליגודנדרוציט מלפֵּף את הענף שלו סביב לאקסון שוב ושוב, כמו בגלגול של שטיח (איור 1C) [2]. החומר שמלופף סביב לאקסון נקרא מִיאָלִין, והפעולה שבה אוליגודנדרוציט כורך את המיאלין שלו סביב לאקסון נקראת מִיאָלִינִיזַצְיָה.
כאשר תינוק נולד, תאי העצב שלו אינם מקבלים כל סיוע מאוליגודנדרוציטים (איור 1A) [3 ,2]. מוחו של התינוק פועל, אך ההודעות שלו נשלחות מעט לאט, וחלקן עשויות 'להיאבד בדואר'. כאשר אנו גדֵלים, אוליגודנדרוציטים מתחילים לפרושׂ את ענפיהם כדי להתלפף סביב לאקסונים במוח. כשזה קורה, תאי העצב נעשים מהירים יותר ויותר בשליחת הודעות. בסופו של דבר, כשאנו מגיעים לגילֵי 30-25, כל האקסונים שזקוקים לסיוע מהאוליגודנדרוציטים יצופּו במיאלין (איור 1B) [4]. ברגע שתאי עצב ואוליגודנדרוציטים חוברים זה לזה, תאי העצב יכולים לתקשר במהירות אדירה, כמו לחיצה על פונקציית 'שְׁלַח' בדואר האלקטרוני.
מהו מיאלין בדיוק, וכיצד הוא מסייע לתאי עצב לשלוח הודעות מהר יותר? מיאלין מורכב מחומר שומני שמספֵּק לו את הַיְּכֹלֶת לבודד תאי עצב, כמו ציפוי פלסטיק סביב חוט מתכת בכבלי חשמל. הבידוד שמיאלין מספֵּק שומר על ההודעה בתוך תא העצב בזמן שהיא מתקדמת לאורך האקסון. אם לאקסון אין ציפוי מיאלין, ההודעה בסופו של דבר תדלוף החוצה או תיחלש כשתתקדם לאורך האקסון. אם חלק גדול מדי מההודעה חסר כשהיא מגיעה לקצה האקסון, ההודעה עלולה להיות בלתי ניתנת לשליחה, או לא שלמה! אם כן, נוסף על האצַת שליחת ההודעות, מיאלין חיוני לשמירה על הודעות במצב קריא ומדויק בעת מסירתן.
שליחת הודעות כל היום כרוכה בעבודה רבה. במהלך היום הדוורים שלנו צריכים לשתות מים ולאכול כדי להבטיח שיש להם מספיק אנרגיה כדי לבצע את כל שליחויותיהם. גם תאי עצב דורשים תמיכה תזונתית רבּה מאחר שאף הם עובדים כל הזמן. כיוון שאוליגודנדרוציטים מצויים במגע כל כך קרוב עם תאי עצב, הם התאים האידיאליים כדי לסייע להבטיח שתאי העצב מקבלים את כל המזון והמים שהם צריכים. אם כן, נוסף על הסיוע במסירת הודעות, אוליגודנדרוציטים מספְּקים לתאי העצב את התמיכה התזונתית שהם זקוקים לה כדי להמשיך לשלוח הודעות [3].
פגיעה בתאי עצב ותיקונם
ישנם דברים רבים שעשויים למנוע מאוליגודנדרוציטים לסייע לתאי עצב (איור 2) כפי שכבר למדתם, לתא עצב בוגר בריא יהיה מיאלין שעטוף סביב לאקסון שלו. במחלות כמו מחלת אלצהיימר, תאי עצב נעשים חולים מאוד ומתחילים למות, בתהליך שנקרא נִוּוּן. כאשר תא עצב מתנוון, המיאלין מתחיל ליפול מהאקסון, והאקסון עובר תהליך של דֶּה-מיאליניזציה. טרשת נפוצה היא דוגמה למחלה של דה-מיאליניזציה, שבּה אקסונים מאבדים את המיאלין שלהם. אם אובדן האוליגודנדרוציטים חמוּר, גם תאי העצב יתחילו להתנוון [5 ,2]. אם אקסון נפגע או נחתך, אף הוא עלול לעבור דה-מיאליניזציה ולמות [1]. מדענים סבורים כי תאי עצב ואוליגודנדרוציטים כל כך תלויים זה בזה, עד שאם תא אחד מתחיל למות, לעיתים קרובות גם לתא האחר יקרה אותו הדבר [6].
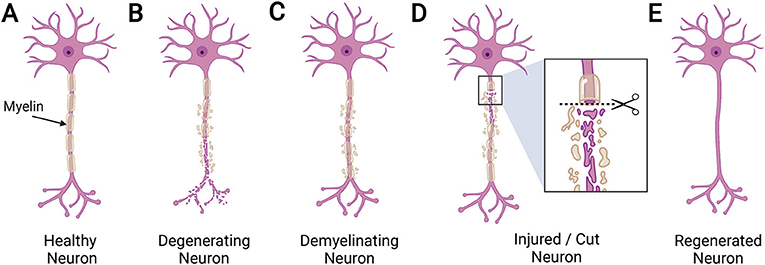
- איור 2 - תהליכי ניוון של תאי עצב ופגיעה בהם, לצד תהליכי התחדשות.
- (A) תא עצב תקין (Healthy neuron), בריא ומצופה במיאלין (Myelin), במוח בוגר. (B) כאשר תא עצב שמצופה במיאלין מתנוון (Degenerating), הן האקסון הן המיאלין מתפרקים ומתים. (C) אם אוליגודנדרוציטים חולים או מתים, מיאלין נופל מהאקסון בתהליך שנקרא דה-מיאליניזציה (Demyelinating). תהליך זה יכול להתרחש בטרשת נפוצה. (D) אם האקסון נחתך (Cut) או שתא העצב נפגע (Injured), הן האקסון הן המיאלין מתפרקים ומתים. (E) תאי עצב יכולים לגדול מחדש, או להתחדש (Regenerate), אך לתאי עצב שהתחדשו אין מיאלין על האקסונים שלהם.
כאשר תא עצב גדֵל מחדש או מתקֵּן את האקסון שלו, אנו מכנים תהליך זה התחדשות. הואיל ותאי עצב חיוניים כל כך לתקשורת של המוח, מדענים עמלו על התחדשות אקסונים לְאַחַר פגיעה או מחלה. אך אפילו כשמדענים גורמים לתאי עצב להתחדש, תאי העצב הללו אינם מצופים מיאלין על ידי אוליגודנדרוציטים, מה שמוֹנע מתאי העצב החדשים שתוקנו לבצע את חובות התקשורת שלהם. במקרים מסוימים, תאי עצב חדשים ימותו ללא תמיכתם של אוליגודנדרוציטים [3].
מדענים מנסים להגן על אוליגודנדרוציטים ולגדלם מחדש כך שתאי עצב חדשים יוכלו לעבור שוב מיאליניזציה, ותפקודי המוח ישוחזרו. אחד הדברים המדהימים לגבי אוליגודנדרוציטים הוא שהם יכולים להחליף את עצמם במהלך חייו של אדם. בהינתן העבודה הָרַבָּה שאוליגודנדרוציטים מְבצעים, קל להבין את הצורך להחליפם מִדֵּי פעם. למרבה המזל, המוח מכיל אוליגודנדרוציטים תינוקות, שמכונים תאי אב של אוליגודנדרוציטים. כאשר אוליגודנדרוציט זקן זקוק להחלפה, ראשית, תא אב של אוליגודנדרוציט יתחלק במטרה לייצר עוד תאים מסוג זה. תאי האב החדשים יתחילו להתפתח לאוליגודנדרוציטים לא בוגרים. בשלב זה יהיו להם ענפים, אך הם עדיין לא יבצעו מיאליניזציה. עם הזמן, אוליגודנדרוציטים לא בוגרים ימשיכו להתפתח, עד שיהיו לאוליגודנדרוציטים בוגרים המְּבצעים מיאליניזציה (איור 3) [7].
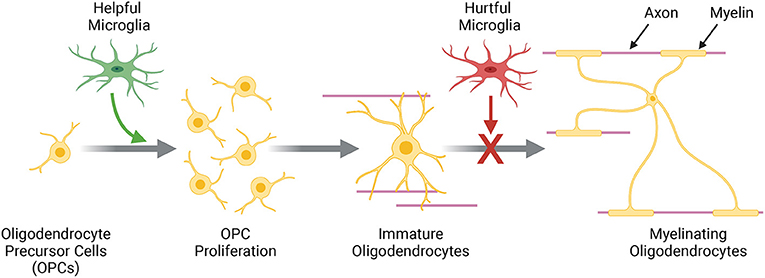
- איור 3 - פעילותם של תאי אב של אוליגודנדרוציטים.
- אוליגודנדרוציטים תינוקות, שמכונים תאי אב של אוליגודנדרוציטים (OPCs), הופכים לאוליגודנדרוציטים בוגרים שמְבצעים מיאליניזציה (Myelinating). כאשר תאי אב של אוליגודנדרוציטים מקבלים אות מתא מִיקְרוֹגְלִיָיה 'מועיל' (Helpful Microglia), תאי האב של אוליגודנדרוציטים ראשית מִתרבים (proliferation). התאים החדשים האלה נעשים אוליגודנדרוציטים לא בוגרים (Immature oligodendrocy tes), שיש להם ענפים, אך עדיין אינם מצפים אקסונים במיאלין. בסופו של דבר, אוליגודנדרוציטים לא בוגרים נעשים אוליגודנדרוציטים בוגרים שמבצעים מיאליניזציה, ויכולים לְצפות מגוון אקסונים במיאלין. אולם, תאי מיקרוגלייה 'מזיקים' (Hurtful Microglia), או הנתונים בלחץ, עלולים לשלוח אותות שמשאירים אוליגודנדרוציטים כלואים בשלב הלא בוגר.
מה עוצר אוליגודנדרוציטים חדשים מלסייע לתאי עצב?
אף על פי שאנו יודעים כי התפתחות תאי אב של אוליגודנדרוציטים לאוליגודנדרוציטים שמְבצעים מיאליניזציה היא אפשרית ומתרחשת באופן טבעי, איננו יודעים כיצד לאתחל את התהליך הזה לאחר פגיעה או מחלה. בנסיבות אלה, בדרך כלל ישנן בעיות גם עם תאים אחרים במוח – לא רק עם תאי עצב ואוליגודנדרוציטים. עבודה עכשווית שביצעו מדענים הראתה כי תאים במוח שנקראים מִיקְרוֹגְלִיָיה, אשר מְתפקדים כ'אספני הזבל' בתוך המוח, הם מַפְתֵּחַ ליצירת אוליגודנדרוציטים חדשים. מיקרוגלייה מתקדמים לאורך המוח וחוט השדרה, ומחפשים אחרי 'אשפה' שצריך להיפטר ממנה – כמו תאים מתים או תאים שאינם מְתפקדים כראוי. תאי מיקרוגלייה גם שולחים אותות לתאים אחרים, לרבות אוליגודנדרוציטים, ומוסרים להם שמשהו לא תקין במוח, או שהכול בסדר ואפשר לחדֵּשׁ את הפעילויות הרגילות. כאשר תאי מיקרוגלייה נתקלים בפגיעה גדולה או באזור במוח שניזוק, הם יכולים להפוך פעילים מדי מכל הדברים שאינם פועלים כשורה.
מחקר חדש מצביע על כך שאחרי פגיעה או מחלה, ישנם הן תאי מיקרוגלייה 'מועילים' והן תאי מיקרוגלייה 'מזיקים', ושני הסוגים יכולים להשפיע על אוליגודנדרוציטים (איור 3) [9 ,8]. בתחילה, תאי מיקרוגלייה 'מועילים' מורים לתאי אב של אוליגודנדרוציטים כי ישנם תאי עצב חדשים שצריך לְצפּות במיאלין. האות הזה שמתקבל מתאי מיקרוגלייה 'מועילים', מביא לעלייה במספר תאי אב של אוליגודנדרוציטים [6]. אולם, עם הזמן, תאי המיקרוגלייה ה'מועילים' עלולים להפוך לתאי מיקרוגלייה 'מזיקים'. תוכלו לְדַמּוֹת כי אם אתם מוקפים בקביעוּת על ידי דברים שאינם פועלים כשורה או מתקלקלים, ייתכן שתהפכו מעט לחוצים. במהלך הזמן שלוקח לתאי אב של אוליגודנדרוציטים להפוך לאוליגודנדרוציטים לא בוגרים, תאי מיקרוגלייה נעשים מוּצָפִים מאוד. כה מוצפים, עד שהם מתחילים להנחות את האוליגודנדרוציטים הלא בוגרים להפסיק להתבגר, ולא להפוך לאוליגודנדרוציטים שמְבצעים מיאליניזציה [8].
במטרה לִמנוע ממיקרוגלייה לעצור את התבגרותם של אוליגודנדרוציטים, מדענים פיתחו תרופה שמסירה באופן זמני כמעט את כל תאי המיקרוגלייה מהמוח [9]. תרופה זו מנחה תאי מיקרוגלייה 'מזיקים' להרוס את עצמם, ומחסלת את מַרבית תאי המיקרוגלייה במוח, אך לא את כולם. הירידה החדה במספרם של תאי המיקרוגלייה ה'מזיקים' מספיקה כדי לאפשר לאוליגודנדרוציטים לא בוגרים לסיים להתפתח, וללפף את המיאלין שלהם סביב אקסונים חדשים [8]. ברגע שאקסונים חדשים מצופים במיאלין על ידי אוליגודנדרוציטים שזה עתה התבגרו, התרופה כבר לא נדרשת, וניתן להפסיק ליטול אותה. כאשר התרופה מוּסרת, תאי מיקרוגלייה מתחילים להחליף את עצמם [9]. הבעיה בתרופה הזו היא שאיננו רוצים שאנשים יישארו ללא תאי מיקרוגלייה, אפילו אם זה לתקופה קצרה בלבד. תאי מיקרוגלייה חיוניים לשמירה על המוח פנוי מ'אשפה' ומִתָּאים שניזוקו, ולכן אם אנשים חווים פגיעת ראש נוספת בזמן נטילת התרופה, לא יהיו תאי מיקרוגלייה 'מועילים' שיוכלו לנקות את האזור. לפיכך, מדענים עובדים כיום על יצירת תרופות חדשות שעוצרות תאי מיקרוגלייה 'מזיקים' ממניעת הייצור של אוליגודנדרוציטים שמְבצעים מיאליניזציה, תוך שהן מאפשרות לתאי מיקרוגלייה לבצע את תפקידיהם המועילים האחרים.
מסקנות
תאי עצב ואוליגודנדרוציטים פועלים יחד כדי לוודא שהודעות נשלחות כמה שיותר מהר ברחבי המוח והגוף. כאשר המוח נפגע או חולה, הן תאי עצב הן אוליגודנדרוציטים עלולים למות – מה שגורם לכשלים חמורים בתקשורת. במיליוני מטופלים עם פגיעות בחוט השדרה או עם טרשת נפוצה, כִּשְׁלֵי התקשורת האלה עלולים לגרום לאנשים לאבד את יכולתם ללכת, או לדבּר, או לִחיות חיים רגילים. מסיבה זו, מדענים עומלים קשה במטרה לחדֵּש תאי עצב ואוליגודנדרוציטים לאחר התרחשות הפגיעות או המחלות הללו. תגלית של טיפולים חדשים המסייעים לאוליגודנדרוציטים לבצע שוב מיאליניזציה ולתמוך בתאי עצב, יכולה לסייע בשיפור איכות חייהם של מטופלים רבּים.
מילון מונחים
תא עצב (Neuron): ↑ סוג תא שנמצא במוח ובחוט השדרה, מתמחה בתקשורת ברחבי הגוף.
אקסון (Axon): ↑ שלוחה ארוכה, דמוית-צינור, המאפשרת לתא עצב לתקשר עם חלקים רחוקים של המוח והגוף.
אוליגודנדרוציט (Oligodendrocyte): ↑ תא עם ענפים אשר מלפֵּף מיאלין סביב לאקסונים.
מיאלין (Myelin): ↑ קרום תא (מֶמְבְּרָנָה) שומני שעוטף תאי עצב, אשר נוצר מאוליגודנדרוציטים.
ניוון (Degeneration): ↑ מוות של אקסונים כתוצאה מפגיעה או מחלה.
התחדשות (Regeneration): ↑ גדילה מחדש של תא או חלק מתא, כמו למשל האקסון של תא עצב.
תא אב של אוליגודנדרוציט (Oligodendrocyte Precursor Cell, OPC): ↑ אוליגודנדרוציט תינוק שיכול לגדול ולהפוך לאוליגודנדרוציט בוגר.
מיקרוגלייה (Microglia): ↑ תא שפועל כמו 'איש הזבל' של המוח, ומסיר את ה'אשפה' שמיוצרת על ידי תאים מתים או תאים שאינם מְתפקדים כראוי.
הצהרת ניגוד אינטרסים
המחברים מצהירים כל המחקר נערך בהעדר כי קשר מסחרי או פיננסי שיכול להתפרש כניגוד אינטרסים פוטנציאלי.
תודות
האיורים נוצרו באמצעות תוכנת BioRender (http://biorender.com). תודה לסוקרים הצעירים ול-Susan Debad על הפיכת כתב היד הזה נגישׁ יותר לקהל הצעיר! TS נתמכה על ידי מענק מחקר T32 מ-NEI (המכון לחינוך בתחום מדעי המוח, T32EY007145), ומענק מחקר F32 מ-NEI (F32EY032779).
מקורות
[1] ↑ Baumann, N., and Pham-Dinh, D. 2001. Biology of oligodendrocyte and myelin in the mammalian central nervous system. Physiol Rev. 81:871–927. doi: 10.1152/physrev.2001.81.2.871
[2] ↑ Kuhn, S., Gritti, L., Crooks, D., and Dombrowski, Y. 2019. Oligodendrocytes in development, myelin generation and beyond. Cells. 8:1–23. doi: 10.3390/cells8111424
[3] ↑ Stadelmann, C., Timmler, S., Barrantes-freer, A., and Simons, M. 2019. Myelin in the central nervous system: structure, function, and pathology. Physiol Rev. 99:1381–431. doi: 10.1152/physrev.00031.2018
[4] ↑ Fields, R. D. 2008. White matter matters. Brain Sci. 298:54–61. doi: 10.1038/scientificamerican0308-54
[5] ↑ Skaper, S. D. 2019. Oligodendrocyte Precursor Cells as a Therapeutic Target for Demyelinating Diseases. 1st ed. Cambridge, MA: Elsevier B.V. doi: 10.1016/bs.pbr.2019.03.013
[6] ↑ Franklin, R. J. M., and Ffrench-Constant, C. 2008. Remyelination in the CNS: from biology to therapy. Nat Rev Neurosci. 9:839–55. doi: 10.1038/nrn2480
[7] ↑ Pease-Raissi, S. E., and Chan, J. R. 2021. Building a (w)rapport between neurons and oligodendroglia: reciprocal interactions underlying adaptive myelination. Neuron 109:1258–1273. doi: 10.1016/j.neuron.2021.02.003
[8] ↑ Wang, J., He, X., Meng, H., Li, Y., Dmitriev, P., Tian, F., et al. 2020. Robust myelination of regenerated axons induced by combined manipulations of GPR17 and microglia. Neuron. 108:876–86.e4. doi: 10.1016/j.neuron.2020.09.016
[9] ↑ Li, Q., and Barres, B. A. 2018. Microglia and macrophages in brain homeostasis and disease. Nat Rev Immunol. 18:225–42. doi: 10.1038/nri.2017.125
