תַקצִיר
כן, אנו יכולים לאכלס בגופנו ריריות מסוכנות שנקראות ביופילמים. הם יכולים לגרום לזיהומים חמוּרים בכל מקום בגופנו. הם מכילים חיידקים שמתחבאים וחיידקים רדומים במטריצת הגנה. זה גורם להם להיות קשים מאוד לטיפול. הם אוהבים להידבק לחומרים מושתלים כמו פְּרוֹתֶזוֹת (תוֹתבוֹת) או קָטֶטֶר (צַנְתָּר). הם יכולים לחיות גם בשיניכם, באוזניכם, ואפילו לעיתים בריאוֹתיכם. למרבה המזל, חוקרים מודעים מאוד לבעיה הזו. הם עורכים ניסויים עם פתרונות מגוונים במטרה לנסות להרוס את הביופילמים האלה. האם אתם סקרנים לגבי הרעיונות המבריקים שלהם? אז תעקבו אחרינו ותלמדו עוד על האופן שבו ביופילמים גורמים לכם לחלות, וכיצד אנו יכולים להילחם בהם.
חיידקים הם אורגניזמים חיים קטנים. הם רבּים הרבה יותר מבני אדם על כדור הארץ. ישנם יותר חיידקים במיליליטר אחד של מים מאשר בני אדם על כדור הארץ! הם יכולים לאכלס את הסביבה, אולם גם את גוף האדם. בעודם ניצבים מול עולם גדול כל כך, הם צריכים למצוא אסטרטגיות לשרוד.
האם אתם מכירים את האִמְרָה “ביחד, אנו חזקים יותר”? מיקרובים יודעים זאת!
כדי לשרוד טוב יותר, מרבית מינֵי החיידקים מסוגלים להתאסף בחברות שנקראות ביופילמים1. בביופילמים, חיידקים משחקים משחק מחבואים. הם מייצרים שמיכת הגנה שנקראת מַטְרִיצָה. היא מכילה סוכרים, חלבונים וחומצות גרעין [1]. ביופילמים שונים מאוד ממה שאנו מכנים “תרביות פלנקטוֹניוֹת”. אלה מכילות חיידקים מבודדים ששוחים בחופשיות בנוזל, כמו פלנקטון בים. בסביבה, ביופילמים נוצרים בכל מקום: על צינורות, על שלדי סירות, על אבנים ואפילו במעיינות מים חמים. בגוף האנושי, הם יכולים להתחבר לאיברים, וביתר קלות, הם יכולים להתחבר לחומרים מושתלים. אם הם מכילים חיידקים פתוגנים, הם מהווים גורם מרכזי לזיהומים כרוניים.
מדוע ביופילמים חשובים בפתולוגיות אנושיות?
חיידקים אוהבים להתחבר לכל מקום בגופנו [2] (איור 1). האם אתם מכירים פלאק דנטלי? זהו חומר רירי שנוצר על השיניים שלכם בין ביקורים אצל רופא השיניים. הוא מכיל תערובת של חיידקים וחלבונים מהרוק שלכם. אתם יכולים להסיר אותו על ידי צחצוח שיניים קבוע, אחרת החיידקים בתוך הפלאק ממצקים את הביופילם. בסוף, אתם תסבלו מזיהום של החניכיים ומחורים בשיניים. היגיינה טובה וטיפולים תכופים אצל רופא השיניים יסייעו לכם לשמור על בריאות טובה של שיניכם! ביופילמים גם יכולים להיווצר בהרבה מקומות אחרים ולגרום לזיהומים כרוניים. הזיהומים האלה עשויים להשתפר כשאתם נוטלים אנטיביוטיקה. אולם הם מתחילים מחדש אחרי שאתם מפסיקים את הטיפול.
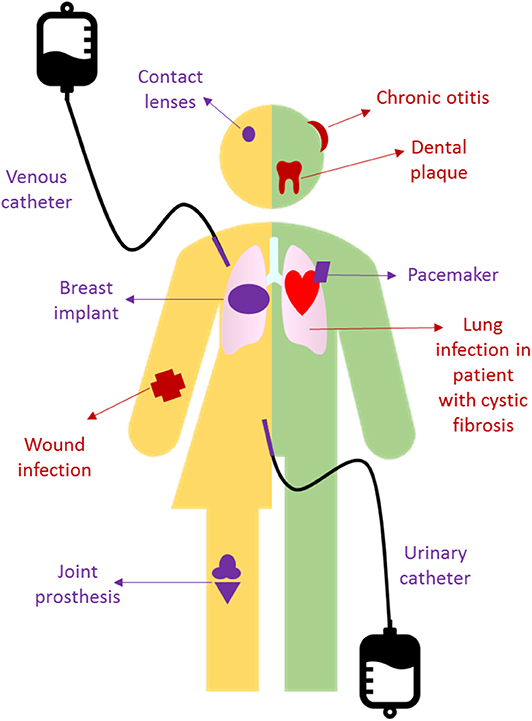
- איור 1 - כמה דוגמאות לזיהומים שקשורים בביופילמים.
- באדום, זיהומים שמתפתחים על רקמות גופנו. בסגול, זיהומים שמתפתחים על חומרים מושתלים.
כמה דוגמאות לזיהומים כאלה? זיהומים כרוניים באוזניים (אוֹטיטיס) אם אתם הולכים לעיתים קרובות לבריכה, או זיהומים בריאוֹת אצל ילדים עם מחלה גנטית שנקראת ציסטיק פיברוזיס2. ילדים מסכנים! הליחה בריאוֹתיהם היא רירית, וחיידקים מוצאים אותה נוחה מאוד למחיה. מזיהומים כאלה קשה מאוד להיפטר. זו בעיה גדולה. המטופלים יעברו טיפולים תכופים ונרחבים עם אנטיביוטיקות, אולם החיידקים יגנו על עצמם ויתפתחו. בסופו של דבר, הם יהפכו עמידים לטיפול ובסוף, האנטיביוטיקות כבר לא יעבדו ולא יצליחו להילחם בזיהום.
מרבית המכשירים שנמצאים בשימוש ברפואה מציעים מקומות מחסה מושלמים להתפתחות של ביופילמים. חשבו על הביקור האחרון שלכם לסבא וסבתא בבית החולים. ככל הנראה היו להם קָטֶטֶרִים תוך-ורידיים כדי להעביר תרופות לתוך דמם, או נַקָּזִים אחרים. אולי גם היו להם פרותזות של מִפְרָקִים שהושתלו באגן או בברך כאשר המפרק שלהם יצר כאבים גדולים מדי. המשטחים המלאכותיים האלה מאוכלסים בקלות על ידי חיידקים. החיידקים נקשרים בחוזקה אל המשטחים האלה. לאחר מכן, הם מתחילים להתחלק במהירות ולייצר מטריצה. על גבי המכשירים האלה, ביופילמים גדלים בצורות מורכבות מאוד. חיידקים יסתגלו בהדרגה לסביבתם החדשה. הם כבר לא יגיבו לאנטיביוטיקות. בסוף, האפשרות היחידה שיש לרופאים תהיה להסיר את המכשיר ולהחליפו במכשיר חדש, במידת האפשר. כמובן, זה יחסית קל כשהמכשיר הוא קטטר פשוט. אולם הסרת שֶׁתֶל, כמו למשל פרותזה באגן או בברך, היא תהליך מורכב. לעיתים קרובות זה דורש ניתוחים רבים, והסבים שלכם ככל הנראה לא ממש יאהבו זאת!
מדוע זיהומים שקשורים בביופילמים עמידים לאנטיביוטיקה?
ביופילם הוא כמו מחילה מוגנת שבה החיידקים רדומים. המטריצה יוצרת מחסום כנגד אנטיביוטיקה. אולם מחסום ההגנה הזה גם מגביל את החדירה של חמצן ומזון. חיידקים שממוקמים בעומק הביופילם יתחילו לרעוב. הם מאיטים את חילוף החומרים שלהם3, כאילו שהם ישנים (איור 2, פאנל שמאלי). חייל ישן קל יותר להרוג מחייל ערני. אולם זה לא נכון עבור כל החיידקים! הרבה אנטיביוטיקות פועלות על חיידקים שמתחלקים באופן פעיל, וזה לא יכול להתרחש כאשר החיידקים ישנים בביופילם. התופעה הזו נקראת “עמידוּת” (או סבילוּת) לאנטיביוטיקה. בניגוד לעמידות לאנטיביוטיקה, סבילות מתהפכת כאשר חיידקים עוזבים את הביופילם [3]. אולם סבילות גם תורמת לכישלון הטיפול. אנו זקוקים לכמות גדולה פי 1,000 של אנטיביוטיקה כדי להרוג חיידקים בביופילמים מאשר בתרביות פלנקטוניות. לכן, האנטיביוטיקה שנרשמת על ידי הרופא שלך לא תעבוד! אלא אם תקחו פי 1,000 כדורים... אולם האם אתם באמת מוכנים לבלוע כל כך הרבה כדורים? ואפילו אם יכולתם לעשות זאת, מינונים כל כך גדולים היו גורמים לכם לחלות! האם הייתם רוצים שיהיה לכם כאב בטן חזק מאוד, שלשול, או כאב ראש? או אפילו גרוע מכך, האם הייתם רוצים להרוס את הכליות, את הכבד, או את תאי הדם שלכם? לא!
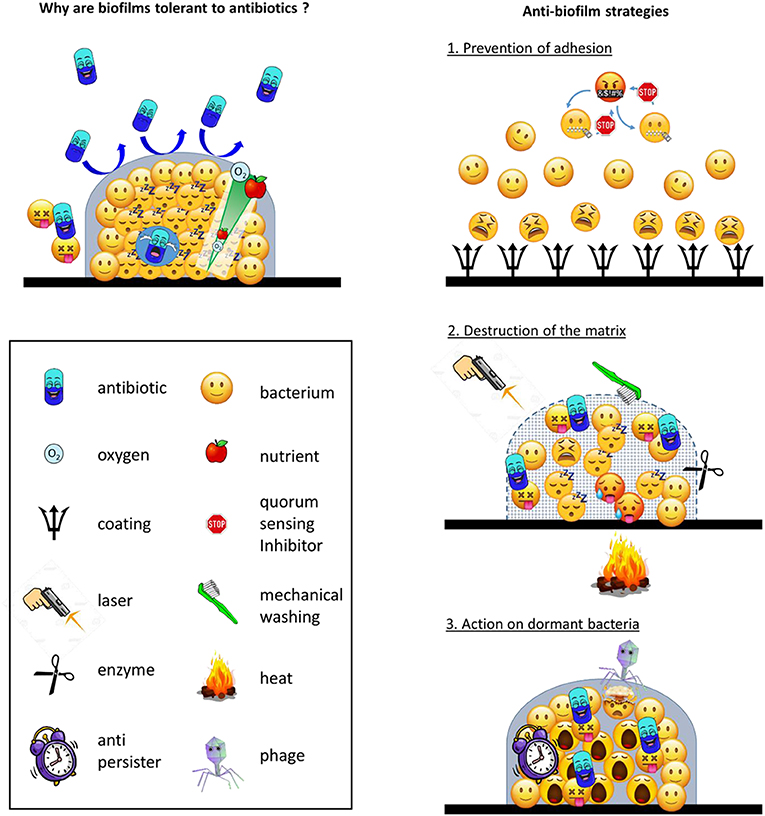
- איור 2 - משמאל: מדוע ביופילמים עמידים לאנטיביוטיקה.
- מימין: אסטרטגיות ללחימה בזיהומים שקשורים לביופילמים.
אלה אסטרטגיות טיפוליות יכולות לשמש אותנו כנגד ביופילמים?
אתם מבינים כעת שאנטיביוטיקות לא עובדות כנגד ביופילמים. אנו צריכים לדמיין אסטרטגיות אחרות להילחם בביופילמים. זה אחד הנושאים הראשיים שזוכים למחקר אינטנסיבי בימים אלה [4]. אתם יכולים לחשוב על שלושה סוגי גישות (איור 2, פאנלים ימניים).
ראשית, מניעה טובה יותר מריפוי! אנו יכולים לנסות למנוע היווצרות של ביופילם. זה רעיון טוב עבור ביופילמים שנוצרים על חומרים מושתלים. אנו יכולים לְצַפּוֹת את המשטח של השתל עם חומרים שמונעים את ההתחברות של חיידקים. אתם יכולים לקבל את האפקט הזה עם ציפוי כסף, למשל. עם החומר האצילי הזה בגופכם, אתם כעת יכולים להיות יקרי ערך ביותר! אנו גם יכולים למלא את המכשיר המושתל עם כמויות גדולות של אנטיביוטיקה. האנטיביוטיקה תהיה מוכנה לפעול על חיידקים לפני שהם יתחילו לישון. לדוגמה, אנו יכולים להשתמש בסוג של מֶלֶט, שמלא בחרוזי אנטיביוטיקה, כדי לשקם שֶׁבֶר בעצם. אנו גם יכולים לשטוף קטטר עם תמיסת אנטיביוטיקה מרוכזת. מרבית הגישות האלה כבר נמצאות בשימוש בקליניקות. לחלופין, אנו יכולים להתערב במערכת התקשורת שחיידקים משתמשים בה. היא נקראת חִישַׁת מניין [5]. היא מכילה מולקולות שמיוצרות על ידי חיידקים, והיא מורגשת על ידי שכניהם, כאילו שהם מחייכים לנוכח בושם טוב. ללא הטלפון הנייד שלכם, אינכם יכולים להתקשר לחבריכם. ללא חישת מניין, חיידקים לא יכולים למצוא אחד את השני כדי להתחיל לבנות את הביופילם.
שנית, אנו יכולים לנסות להרוס את המטריצה. זה יכול לסייע לאנטיביוטיקה להגיע לחיידקים שמתחבאים. המטרה הזו יכולה להיות מושגת באמצעות אנזימים. הם יחתכו את החומרים שנמצאים במטריצה לפיסות קטנות, ממש כמו אם הייתם פורמים את האפוד שלכם – אתם יותר חשופים ושבריריים, לא כן? אנו גם יכולים לשטוף את הביופילם באמצעות לחץ גבוה ממכשיר בשם Karcher (מכשיר לניקוי באמצעות לחץ גבוה), או שאנו יכולים לנסות שיטות מרשימות אחרות כמו למשל שוקים בלייזר, זרמים חשמליים, או אפילו חום. זה עשוי להיראות כמו מדע בדיוני! ובמובן מסוים ברברי וכואב! אולם היו ערים לכך שחלק מהשיטות האלה כבר משמשות רופאי שיניים או מנתחים בזמן שאתם ישנים בחדר הניתוח...
שלישית, אנו יכולים לנסות לעורר את החיידקים הַיְּשֵׁנִים. זו לא מטלה קלה. אנו צריכים לגלות מולקולות “אנטי-עקשניות”. אלה יסייעו לאנטיביוטיקה להרוג חיידקים ישנים. המולקולה האנטי-עקשנית הראשונה התגלתה לפני כמה שנים בלבד [6]. היא מפעילה מערכת שעון מעורר אצל החיידקים. כאשר השעון מצלצל, הגיע הזמן לקום! מולקולות אחרות כאלה מחוררות את המעטפה החיידקית. מה יקרה אם תפתחו את כל החלונות בביתכם? מצד אחד, אוויר קר מבחוץ ייכנס לחדר ויעורר אתכם. משמעות הדבר היא שחיידקים כבר לא ישנים. מצד אחר אבקנים יוכלו להיכנס ולגרום לעיניכם לגרד אם אתם אלרגים אליהם. עבור חיידקים, משמעות הדבר היא שאנטיביוטיקות יכולות להיכנס לתא ולפגוע בהם. המולקולות האנטי-עקשניות האלה עדיין נבחנות במעבדות. הן עדיין לא נמצאות בשימוש לרפא אנשים. גישה מדהימה אחרת משתמשת בנשקים ביולוגיים. בקטריופאג’ים [7] הם וירוסים של חיידקים. הם גורמים לחיידקים לחלות, אולם לא לבני אדם. חלק מהם גם מייצרים אנזימים שיכולים להרוס את המטריצה. משמעות הדבר היא שהם יכולים לפגוע בשתי מטרות בבת אחת!
מה לגבי העתיד?
מרבית האסטרטגיות החדשות האלה עדיין נמצאות בפיתוח. הרבה עבודה נדרשת כדי לוודא שהן פעילוֹת ופועלות כמו שצריך. דאגה נוספת היא הסיכון שהאסטרטגיות האלה עלולות להיות רעילות. אולם אנו מתקדמים בקצב קבוע. חלק מהטיפולים נוסו לאחרונה על מטופלים! לדוגמה, בקטריופאגים היו בשימוש, והצליחו לטפל בפעוט שהיה לו זיהום חמוּר בכבד.
האם אתם מעוניינים להצטרף לקבוצת חוקרים ולעבוד על הנושאים האלה? אנו מצפים לראותכם במעבדות שלנו בעתיד הקרוב!
אתם יכולים למצוא מידע נוסף בכתבת פרונטירז – מדע לצעירים הזו [5, 7].
מילון מונחים
מטריצה (Matrix): ↑ תערובת של חומרים שבתוכם חיידקים משובצים, והם תומכים בארכיטקטורה הגלובלית של הביופילם.
אנטיביוטיקה (Antibiotic): ↑ חומר שמסוגל למנוע גדילה חיידקית, או אפילו יותר מכך, להרוג חיידקים.
קטטר (Catheter): ↑ צינורית דקה שיכולה להיות מוכנסת לגוף כדי להזריק תרופות לדם או לְנַקֵּז נוזלים (כמו למשל שתן ומוּגלה).
נקזים (Drains): ↑ צינורות שמושתלים במטרה להסיר הצטברויות של נוזלים מהגוף (למשל בסוף של הליך ניתוח).
חילוף חומרים (Metabolism): ↑ השרשרת השלמה של תגובות כימיות שמתרחשת בתא ותומכת בחיים (יצירת אנרגיה, הרכבה של מולקולות שנדרשות כאבני בניין לתאים).
עמידות לאנטיביוטיקה (Antibiotic Resistance): ↑ רכישה על ידי חיידקים של מנגנון שגורם להם להיות בלתי רגישים לאנטיביוטיקה (לדוגמה, הֶרֶס של אנטיביוטיקה, שינוי של אנטיביוטיקת מטרה).
אנזים (Enzyme): ↑ חלבון שמסוגל להפוך מולקולה אחת לאחרת, לדוגמה בתוצרי פירוק.
הצהרת ניגוד אינטרסים
המחברים מצהירים כי המחקר נערך בהעדר כל קשר מסחרי או פיננסי שיכול להתפרש כניגוד אינטרסים פוטנציאלי.
תודות
המחברים רוצים להודות לקמילה, לשרלוט ולוולנטיין (בנות 14-12) על שקראו והעירו על המאמר הזה.
הערות שוליים
1 ↑https://kids.frontiersin.org/article/10.3389/frym.2016.00014
2 ↑https://kids.frontiersin.org/article/10.3389/frym.2019.00106
3 ↑https://kids.frontiersin.org/article/10.3389/frym.2019.00045
מקורות
[1] ↑ Costerton, J. W., Stewart, P. S., and Greenberg, E. P. 1999. Bacterial biofilms: a common cause of persistent infections. Science 284:1318–22. doi: 10.1126/science.284.5418.1318
[2] ↑ Lebeaux, D., Ghigo, J. M., and Beloin, C. 2014. Biofilm-related infections: bridging the gap between clinical management and fundamental aspects of recalcitrance toward antibiotics. Microbiol. Mol. Biol. Rev. 78:510–43. doi: 10.1128/MMBR.00013-14
[3] ↑ Yan, J., and Bassler, B. L. 2019. Surviving as a community: antibiotic tolerance and persistence in bacterial biofilms. Cell Host Microbe 26:15–21. doi: 10.1016/j.chom.2019.06.002
[4] ↑ Suresh, M. K., Biswas, R., and Biswas, L. 2019. An update on recent developments in the prevention and treatment of Staphylococcus aureus biofilms. Int. J. Med. Microbiol. 309:1–12. doi: 10.1016/j.ijmm.2018.11.002
[5] ↑ Costantino, V., and Esposito, G. 2018. Do you know that microbes use social networks? Front. Young Minds 6:31. doi: 10.3389/frym.2018.00031
[6] ↑ Conlon, B. P., Nakayasu, E. S., Fleck, L. E., LaFleur, M. D., Isabella, V. M., Coleman, K., et al. 2013. Activated ClpP kills persisters and eradicates a chronic biofilm infection. Nature 503:365–70. doi: 10.1038/nature12790
[7] ↑ Gutiérrez, D., Fernández, L., Martínez, B., Rodríguez, A., and García, P. 2016. Bacteriophages: the enemies of bad bacteria are our friends! Front. Young Minds 4:30. doi: 10.3389/frym.2016.00030

