תַקצִיר
שינה היא חלק חשוב מהבריאות והמצב התקין הכללי. בלי שינה תקינה, פעולת המוח נעשית מעורפלת ואנחנו נוטים לשכוח דברים. גם חלקים אחרים בגוף מתחילים לפעול באופן לא יעיל. למשל, שינה לא תקינה עלולה לחולל שינויים במערכת החיסונית או בחילוף החומרים, והשינויים האלה עלולים לגרום למחלות או להחמיר מחלות קיימות. למרות כל מה שכבר ידוע לנו, אנחנו עדיין לא מבינים לעומק את כל הגורמים לשיבושי שינה. כיום כבר ידוע לכול שעישון מזיק לבריאות, וממצאים רבים תומכים בהשערה שילדים של אימהות המעשנות בהיריון סובלים מבעיות שינה. בעיות שינה עלולות לגרום למחלות או לשבש את חיי הילד כשיגדל. מאמר זה עוסק בשלוש שאלות: 1. איך יודעים אלה חלקים במוח אחראיים על שינה, ואיך מודדים את זמן השינה ואיכותה אצל בעלי חיים? 2. איך סיגריות משַנות את תפקוד המוח והגוף? 3. איך עלול עישון של האם לשנות את איכות השינה אצל ילדיה, אפילו כשכבר בגרו?
אילו חלקים במוח אחראיים על שינה?
במשך זמן רב, זו הייתה תעלומה, ועד היום המדענים עדיין עסוקים בצירוף פיסות מידע זו לזו. רק במהלך מלחמת העולם הראשונה (1919-1914) התחיל להתברר אלה חלקי מוח שולטים בשינה. רופא בשם קונסטנטין פוֹן אֶקונומו הבחין שמטופלים מסוימים שלו, עם פגיעה בחלק האחורי של האזור במוח בשם “היפותלמוס” ישנים כל היום – ולעומת זאת לאחרים, שנפגעו בחלק הקדמי של ההיפותלמוס, קשה מאוד להירדם. עד היום לא ברור מה גורם לפגיעות כאלה! ד“ר אקונומו העלה השערה שהתָאים בחלק הקדמי של ההיפותלמוס מסייעים לשינה, ואילו באחורי – מסייעים לערוּת. בשנים מאוחרות יותר הצליחו חוקרים לזהות בדיוק אילו תאים באזורים אלה אחראיים על היבטים שונים של שינה, וגם הצליחו להשפיע במעבדה על פעילות התאים האלה.
בעקבות הממצאים של ד”ר אקונומו החלו מדענים אחרים להשתמש באלקטרודות כדי לעקוב אחר פעילות מוחית אצל בעלי חיים ולשנות אותה. אלקטרודה היא פיסת מתכת המוליכה חשמל, ומשמשת ליצירת מגע עם חֵלק לא-מתכתי של מעגל חשמלי. מכיוון שהמוח מתָקשר באמצעות אותות חשמליים, אפשר למדוד את שינויי המתח החשמלי (הפרש הפוטנציאל החשמלי בין שתי נקודות) בין חלקיו השונים וכך להבין יותר מה קורה בו. אחת השיטות לעקוב אחרי פעילות המוח בעזרת מדידה של המתח החשמלי היא אֶלֶקטרוֹאֶנצוֹפָלוֹגרָפיה (EEG) (איור 1). בשיטה זו מצמידים לקרקפת או למוח שתי אלקטרודות או יותר, ומודדים את ההפרש בין המטענים החשמליים של הנקודות. שני מדענים בשם ד“ר ג'וסֶפֶּה מוֹרוּצי וד”ר הוֹרֶס מאגוּן ערכו בסוף שנות הארבעים ניסויי EEG, וגילו בחלק התחתון של המוח קבוצת תאים המשפיעה על הערוּת. היא קיבלה את השם “מערכת ההפעלה הרשתית”. החוקרים גירו את התאים האלה במוח של חתול תוך כדי בדיקת EEG, וגילו שהמתח החשמלי באזור פּחָת כאשר החתול התעורר. כלומר, מספיק לעקוב אחר שינויי המתח החשמלי במוח כדי לדעת אם בעל חיים (או אדם) ישן או ער! תגלית עוד יותר מעניינת היא שאפשר גם לדעת אם מדובר בשינה עמוקה או קלה. לכן, EEG היא שיטה שימושית ביותר לבדוק ולחקור שינה אצל בעלי חיים ובני אדם.
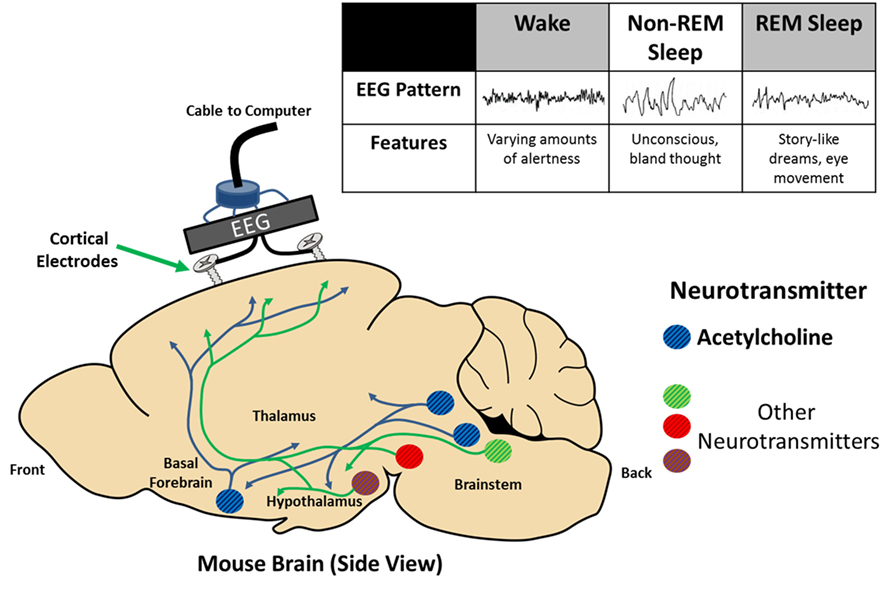
- איור 1 - מעקב אחרי פעילות המוח באמצעות אֶלֶקטרוֹאֶנצֶפָלוֹגרַפיה (EEG).
- כאן משורטט מוח עכבר במבט מהצד. מושתלות בו שתי אלקטרודות (דומות לברגים). המתח החשמלי ביניהן נמדד ויוצר אותות EEG שונים, כפי שאתם רואים בטבלה: משמאל לימין – מצב ערוּת; שינה ללא תנועות עיניים מהירות; ושינה עם תנועות עיניים מהירות. באיור מסומנים מוליכים עצביים שונים (נקודות צבעוניות) המעורבים בערוּת ובשינה – ביניהם אצטילכולין. המוליכים העצביים האלה מיוצרים על-ידי תאים במקומות שונים במוח, אבל נשלחים למקומות אחרים במוח שם הם נקשרים לקולטנים המתאימים.
בעקבות הממצאים האלה זוהו חומרים מסוימים, הנקראים מוליכים עִצבִּיים, שמשפיעים על שינה וערוּת. מולקולות אלה מפעילות תאים בהיפותלמוס ובמערכת ההפעלה הרשתית. המולקולות הללו מיוצרות על-ידי תאי מוח (נוירונים), ומעבירות מסרים כימיים לתאים אחרים כדי לשנות את פעולתם. אחד המוליכים העצביים הנפוצים ביותר במוח ובגוף נקרא אָצֶטילכוֹלִין [1]. מייצרים אותו סוגים רבים של נוירונים, כולל אלה הקשורים לשינה ולערוּת. אצטילכולין משפיע על התאים על-ידי כך שהוא נקשר למולקולה הנמצאת על התא ונקראת קוֹלטָן אָצֶטילכוֹלִין. המנגנון של ההיקשרות דומה לזה של מפתח במנעול (איור 2). האצטילכולין המיוצר בתאים מסוימים בגזע המוח הוא הכרחי לסוג שינה הנקרא שינה עם תנועות עיניים מהירות (REM). בשינה כזאת, העיניים “מתרוצצות” ובבדיקת EEG נרשם גרף דומה לזה שנרשם בזמן ערוּת (אף על פי שזו שינה עמוקה!). מקובל להניח ששינה עם תנועות עיניים מהירות קשורה לחלימה, כי כשמעירים אדם מיד אחרי שינה כזאת, הוא מספר שחלם. אם מזריקים לגזע המוח של בעל חיים את התרופה “קַרְבָּכוֺל”, המְחקָה את פעולת האצטילכולין, היא גורמת לשינה עם תנועות עיניים מהירות. גם לאצטילכולין המיוצר באזור הנקרא “המוח הקדמי הבסיסי” יש השפעה חזקה על שינה, ופגיעה בתאים באזור זה יכולה לשבש אותה קשות. הכול טוב ויפה, אבל איפה הסיגריות נכנסות לתמונה?
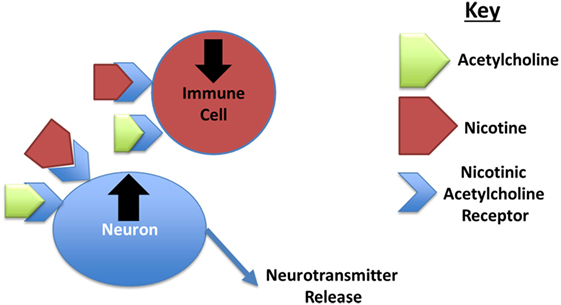
- איור 2 - השפעה של ניקוטין.
- ניקוטין משנה את ההתנהגות של תאי מוח (נוירונים) ותאים חיסוניים, על-ידי כך שהוא נקשר לקולטני אצטילכולין ניקוטיניים. באיור רואים איך ניקוטין (חץ אדום) או אצטילכולין (חץ ירוק) יכולים להיקשר באמצעות קולטן (חץ כחול) לתא חיסוני, ולדכא את פעילותו – או להיקשר לנוירון ולהמריץ אותו לפעול ולשחרר מוליכים עצבִּיים. המוליכים העצביים משפיעים על מגוון תחומים, ביניהם שינה ותפקוד של מערכת החיסון.
איך משנות סיגריות את תפקוד המוח והגוף?
בעשן סיגריות יש אלפי מרכיבים שונים עם השפעות שונות. ניקוטין הוא החומר העיקרי שגורם לסיגריות להיות ממכרות. זהו קוטל-חרקים טבעי, שצמחים ממשפחת הסולניים מייצרים כדי שחרקים לא יאכלו אותם. אחד הצמחים האלה הוא צמח הטבק. ניקוטין מחקֶה את האופן שבו אצטילכולין נקשר לקולטנים מסוימים, ולכן הוא מסוגל להפעיל רבים מהתאים שאותם מפעיל האצטילכולין. קולטנים כאלה נקראים “קולטני אצטילכולין ניקוטיניים”, והם נמצאים על תאים שונים בגוף ובמוח. ניקוטין הוא קטלני לחרקים, אבל על בני אדם יש לו השפעה מעוררת וממכרת. מכיוון שהקולטנים נמצאים על תאים רבים ושונים בכל הגוף, יש לניקוטין השפעות רבות ומגוונות על מערכות גוף שונות. למשל, כשהוא נקשר לקולטני אצטילכולין הוא יכול לשנות את התפקוד של תאים בהיפותלמוס ובאזורים אחרים במוח האחראיים על שינה וערוּת. אם הגירוי חזק מדיי, הוא עלול לשנות את ההתנהגות של התאים לאורך זמן, כך שההשפעה תימשך גם כשאין ניקוטין בסביבה. ניקוטין משפיע לא רק על המוח אלא גם על תאים אחרים בגוף. למשל, לתאים רבים במערכת החיסון יש קולטנים ניקוטיניים. כשהניקוטין נקשר אליהם, הוא מדכא בדרך כלל את פעולתם, וייתכן שזו הסיבה שמעשנים נוטים יותר לחלות.
עישון בזמן ההיריון מגדיל את הסיכון של התינוק לסבול כילד וכמבוגר מבעיות בריאותיות רבות ושונות, ביניהן בעיות שינה. אבל לא ידוע אם חשיפה לניקוטין (או לחומרים אחרים בסיגריות) בשלב מוקדם בחיים גורמת לבעיות שינה אצל ילדים של אימהות מעשנות. חשוב לברר אם החשיפה לניקוטין משפיעה ישירות על השינה, ואם כן, איך זה קורה. כך תהיה לנו הבנה משופרת של הפרעות שינה ושל דרכים למנוע את השפעותיהן השליליות.
על עכברים ואנשים
אי אפשר לערוך ניסויים על נשים הרות כדי לבדוק איך ניקוטין משפיע על בעיות שינה, כי ידוע שניקוטין פוגע בעובּר. במקרים כאלה עורכים לפעמים ניסויים בעכברים כדי לענות על שאלות ביולוגיות. לעכברים יש הרבה מן המשותף עם בני אדם, והם מגיבים באופן דומה לתרופות ולחומרים רבים. לכן עכברי מעבדה היו מודל מתאים מאוד לחקר השאלה אם שימוש בניקוטין במשך ההיריון משפיע ישירות על השינה אצל צאצאי העכברים, אפילו אחרי שהתבגרו.
הניסוי כלל עכברות בהיריון, שקיבלו במשך כל ההיריון מי שתייה עם תמיסת ניקוטין וסוכר (בקבוצת הניסוי) או תמיסה של סוכר בלבד (בקבוצת הביקורת) [2]. לניקוטין יש טעם רע ולכן הוספנו לו סוכר. קצב הגדילה של עכברים שונה מזה של בני אדם, ולכן הניקוטין ניתן עד שהעכברונים שנולדו היו בני שלושה שבועות. אחר כך הוא הופסק, ובמשך שאר זמן הניסוי קיבלו כל העכברים מי שתייה רגילים. כלומר, העכברונים היו חשופים לניקוטין רק בשלב מוקדם מאוד בהתפתחותם (פרק זמן מקביל לתינוקות אנושיים שאִמָם מעשנת). כשהעכברונים גדלו (בגיל 10 שבועות בערך, מקביל לגיל 15-13 שנה אצל בני אדם) עקבו החוקרים במכשירי EEG אחר דפוסי השינה שלהם. כעבור כמה ימים הם אתגרו את מערכות השינה שלהם בכך שמנעו מהם להירדם במשך חמש שעות (מצב דומה למצב של בני אדם הנשארים ערים עד מאוחר מאוד), ובדקו איך הם מתאוששים מהקושי. התברר שעכברים שנחשפו לניקוטין יָשנו יותר מעכברים אחרים, גם באופן כללי וגם בתגובה למחסור בשינה.
לבסוף אתגרו החוקרים את המערכות החיסוניות של העכברים באמצעות מולקולה הנקראת ליפּוֹפּוֹליסָכַריד (LPS). זהו חלק של חיידק מסוים, שהוא בלתי-מזיק אבל מערכת החיסון מגיבה אליו כמו אל זיהום חיידקי אמיתי. התגובה החיסונית עצמה גורמת להרגשה רעה ולעייפות, שכדי להתאושש מהן דרושה שינה מרובה. החוקרים ידעו שניקוטין משפיע על המערכת החיסונית, ולכן רצו לבדוק אם חשיפה לניקוטין בתחילת החיים תשפיע על השינה במצב כזה. התברר שעכברים שקיבלו ניקוטין בראשית חייהם ישנו שינה פחות עמוקה בתגובה לליפוסכריד מאשר עכברים שלא נחשפו לניקוטין (איור 3).
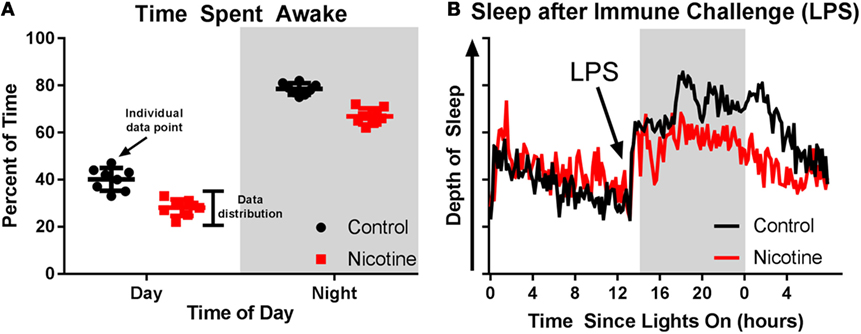
- איור 3 - עכברים שנחשפו לניקוטין בשלב מוקדם יָשנוּ שעות רבות יותר.
- A. כל נקודה מראה את אחוז זמן הערוּת של עכבר אחד במשך היום (אזור לבן) והלילה (אזור אפור). הנקודות האדומות מייצגות עכברים שנחשפו לניקוטין, והשחורות – עכברים מקבוצת הביקורת, שלא נחשפו לניקוטין. שימו לב להתפלגות הנתונים ולהבדל הגדול בזמן הערוּת בין היום לבין הלילה (עכברים הם בעלי חיים ליליים, ולכן הם ערים רוב הלילה). B. רישום של בדיקת EEG המראה שעכברים שנחשפו לניקוטין (גרף אדום) יָשנוּ שינה יותר פחות עמוקה בתגובה ל-LPS מאשר עכברים אחרים (גרף שחור). החץ מראה באיזה שלב ניתן לעכברים LPS, והאזור האפור מתייחס לשעות שבהן האור היה כבוי.
נתונים אלה מצביעים על כך שחשיפה לניקוטין בשלבים המוקדמים של החיים גרמה לעכברים לישון יותר, וכן לשינה רדודה יותר לאחר תגובה חיסונית כאשר העכברים גדלו.
מה המסקנות האפשרות?
מהו, לדעתכם, ההסבר להבדלים האלה בשינה לאחר תגובה חיסונית? החוקרים חושבים שזו תוצאה משינויים ארוכי-טווח בקולטני אצטילכולין ניקוטיניים מסוימים – אלה שנמצאים על תאי מוח השולטים בשינה ובערוּת. אם הקולטנים האלה מופעלים על-ידי ניקוטין בתקופה מסוימת בחיים, התאים עלולים למות או שהאותות הרגילים הנשלחים בזמן התפתחות עלולים להשתבש. איזה ניסוי כדאי לבצע בשלב הבא כדי לבדוק אם זה אכן מה שקרה? סביר להניח שעכברים אלה יָשנו פחות עמוק אחרי תגובה חיסונית מפני שהניקוטין דיכא את המערכת החיסונית שלהם.
בנוסף להשערה שהעלינו, יש כמה סיבות אפשריות אחרות לכך שהשינה משתנה אפילו בבגרות אחרי חשיפה מוקדמת לניקוטין. בניסוי, הניקוטין הרי ניתן לעכברות בהיריון, שטיפלו אחר כך בגוריהן בשלושת השבועות הראשונים לחייהם. ייתכן שהניקוטין שיבש את היכולת של העכברות לטפל בהם כראוי, וזה השפיע על הצאצאים לאורך טווח. כיווּן מחקר אחר קשור להשפעה הידועה של הניקוטין על הנשימה ועל תאי מוח השולטים בה. ייתכן שהשינויים בשינה נובעים מכך. אילו ניסויים אפשר לערוך כדי לברר אם הניקוטין השפיע על יכולת העכברות לטפל בצאצאים, או על הנשימה של העכברים שנחשפו? אפשר, למשל, לערוך ניסוי שבו חושפים את העכברות לניקוטין כמו בניסויים הקודמים, ובוחנים את הטיפול שלהן בגורים. תוצאות הניסויים תומכות בהשערה שחשיפה לניקוטין בשלב מוקדם בחיים יכולה להשפיע על שינה לטווח הארוך ואף בשנות הבגרות. מכיוון ששינה חשובה כל כך לבריאות, הממצאים האלה יכולים לחזק עוד יותר את מאמצי הרופאים לפעול נגד שימוש בניקוטין בזמן ההיריון, מכיוון שהוא גם גורם לבעיות שינה אצל ילדים ומבוגרים.
מילון מונחים
אֶלֶקטרוֹאֶנצֶפָלוֹגרָפיה (EEG; Electroencephalogram): ↑ שיטת מדידה של פעילות מוחית, כולל שינה וערוּת, אצל בני אדם ובעלי חיים. על ידי מדידת שינויים במתח החשמלי במוח, אפשר לעקוב אחרי פעילותו.
מוֹליכים עִצבּיים (Neurotransmitters): ↑ מסָרים נוֹירוכִימיים שהנוירונים (תאי המוח) שולחים כדי לתקשר עם תאים אחרים ועל-ידי כך לשנות את התנהגותם. כמה מהמוליכים העצביים הידועים ביותר הם אצֶטילכוֹלין, דוֹפַּמין, סֶרוטונין, ונוֹראפּינֶפרין.
אָצֶטילכוֹלִין (Acetylcholine): ↑ מוליך עצבּי חשוב הקשור לשינה ולערוּת, וכן לתפקוד מערכת החיסון.
קוֹלטָן (Receptor): ↑ אתר מסוים על פני תא בגוף, שאליו יכולות להיקשר מולקולות מסוימות (כמו אצטילכולין או ניקוטין). כל קולטן מתאים רק לסוג מסוים של מולקולות, כמו מנעול למפתח. כשמולקולה נקשרת לקולטן, התא משנה את התנהגותו. קולטני אצטילכולין ניקוטיניים הם סוג מסוים של קולטנים, היכולים לקשור גם אצטילכולין וגם ניקוטין.
שינה עם תנועות עיניים מהירות (REM sleep): ↑ מצב שינה פעיל, שברישומי בדיקת EEG נראה דומה למצב של ערוּת. מקובל להניח שמתרחשת בו חלימה. אצטילכולין הוא חומר חשוב לקיומה של שנת REM אצל עכברים כמו גם אצל בני אדם.
ניקוטין (Nicotine): ↑ החומר המעורר והממכר העיקרי בסיגריות. ניקוטין מחקֶה את פעולת האצטילכולין בתאים רבים בגוף, בכך שהוא נקשר לקולטני אצטילכולין ניקוטיניים.
ליפּוֹפּוֹליסָכַריד (Lipopolysaccharide, LPS): ↑ חלק של חיידק, שאינו מזיק לכשעצמו, אך גורם לתגובה חיסונית חריפה אצל בני אדם וחיות. באמצעות LPS אפשר לחקור איך מערכת החיסון עצמה תורמת לשינויי התנהגות אופייניים למחלות, כמו שינה מרובה, דיכאון, ופעילות חברתית מופחתת.
הצהרת ניגוד אינטרסים
המחברים מצהירים כי המחקר נערך בהעדר כל קשר מסחרי או פיננסי שיכול להתפרש כניגוד אינטרסים פוטנציאלי.
מקורות
[1] ↑ Scammell, T. E., Arrigoni, E., and Lipton, J. O. 2017. Neural circuitry of wakefulness and sleep. Neuron 93, 747–65. doi: 10.1016/j.neuron.2017.01.014
[2] ↑ Borniger, J. C., Don, R. F., Zhang, N., Boyd, R. T., and Nelson, R. J. 2017. Enduring effects of perinatal nicotine exposure on murine sleep in adulthood. Am. J. Physiol. 313, R280–89. doi: 10.1152/ajpregu.00156.2017

